
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Ковалентные связи с участием атома углеродаСодержание книги
Поиск на нашем сайте В основном состоянии атом углерода С (1s22s22p2) имеет два неспаренных электрона, за счет которых могут образовать только две общие электронные пары. Однако в большинстве своих соединений углерод четырехвалентен. Это объясняется тем, что атом углерода, поглощая небольшое количество энергии, переходит в возбужденное состояние, в котором он имеет 4 неспаренных электрона, т.е. способен образовывать четыре ковалентные связи и принимать участие в формировании четырех общих электронных пар: 6С 1s22s22p2
Энергия возбуждения компенсируется образованием химических связей, которое происходит с выделением энергии. Атомы углерода обладают способностью к образованию трех видов гибридизации электронных орбиталей (sp3, sp2, sp) и образованию между собой кратных (двойных и тройных) связей (табл. 2.2). Таблица 2.2 Типы гибридизации и геометрия молекул
Простая (одинарная) s- связь осуществляется при sp3 -гибридизации, при которой все четыре гибридных орбитали равноценны и имеют направленность в пространстве под углом 109°29’ друг к другу и ориентированы к вершинам правильного тетраэдра (рис. 2.8).
Рис. 2.8. Образование молекулы метана СН4 Если гибридные орбитали углерода перекрываются с шарообразными s -орбиталями атома водорода, то образуется простейшее органическое соединение метан СН4 − предельный углеводород. Большой интерес представляет изучение связей атомов углерода между собой и с атомами других элементов. Рассмотрим строение молекул этана, этилена и ацетилена. Углы между всеми связями в молекуле этана почти точно равны между собой (рис. 2.9) и не отличаются от углов С − Н в молекуле метана. Следовательно, атомы углерода находятся в состоянии sp3 -гибридизации.
Рис. 2.9. Молекула этана С2Н6 Гибридизация электронных орбиталей атомов углерода может быть и неполной, т.е. в ней могут участвовать две (sp2 -гибридизация) или одна (sp -гибридизация) из трех р -орбиталей. В этом случае между атомами углерода образуются кратныесвязи (двойная или тройная). Углеводороды с кратными связями называются непредельными или ненасыщенными. Двойная связь (С=С) образуется при sp2 -гибридизации. В этом случае у каждого из атомов углерода одна из трех р -орбиталей не участвует в гибридизации, в результате образуются три sp2 -гибридные орбитали, расположенные в одной плоскости под углом 120° друг к другу, а негибридная 2 р -орбиталь располагается перпендикулярно этой плоскости. Два атома углерода соединяются между собой, образуя одну s-связь за счет перекрывания гибридных орбиталей и одну p-связь за счет перекрывания р -орбиталей. Взаимодействие свободных гибридных орбиталей углерода с 1 s -орбиталями атомов водорода приводит к образованию молекулы этилена С2Н4 (рис. 2.10) – простейшего представителя непредельных углеводородов.
Рис. 2.10. Образование молекулы этилена С2Н4 Перекрывание электронных орбиталей в случае p-связи меньше и зоны с повышенной электронной плотностью лежат дальше от ядер атомов, поэтому эта связь менее прочная, чем s-связь. Тройная связь образуется за счет одной s-связи и двух p-связей. Электронные орбитали при этом находятся в состоянии sp-гибридизации, образование которой происходит за счет одной s - и одной р -орбиталей (рис. 2.11). Две гибридные орбитали располагаются под углом 180° относительно друг друга, а оставшиеся негибридные две р -орбитали располагаются в двух взаимно перпендикулярных плоскостях. Образование тройной связи имеет место в молекуле ацетилена С2Н2 (см. рис. 2.11).
Рис. 2.11. Образование молекулы ацетилена С2Н2 Особый вид связи возникает при образовании молекулы бензола (С6Н6) – простейшего представителя ароматических углеводородов. Бензол содержит шесть атомов углерода, связанных между собой в цикл (бензольное кольцо), при этом каждый атом углерода находится в состоянии sp2-гибридизации (рис. 2.12).
Рис. 2.12. sp2 – орбитали молекулы бензола С6Н6 Все атомы углерода, входящие в молекулу бензола расположены в одной плоскости. У каждого атома углерода в состоянии sp2-гибридизации имеется еще одна негибридная р-орбиталь с неспаренным электроном, которая образует p-связь (рис. 2.13). Ось такой р -орбитали расположена перпендикулярно плоскости молекулы бензола. Все шесть негибридных р -орбиталей образуют общую связывающую молекулярную p-орбиталь, а все шесть электронов объединяются в p-электронный секстет. Граничная поверхность такой орбитали расположена над и под плоскостью углеродного s-скелета. В результате кругового перекрывания возникает единая делокализованная p-система, охватывающая все углеродные атомы цикла (рис. 2.13). Бензол схематически изображают в виде шестиугольника с кольцом внутри, которое указывает на то, что имеет место делокализация электронов и соответствующих связей.
Рис. 2.13. Ионная химическая связь Ионная связь − химическая связь, образованная в результате взаимного электростатического притяжения противоположно заряженных ионов, при котором устойчивое состояние достигается путем полного перехода общей электронной плотности к атому более электроотрицательного элемента. Чисто ионная связь есть предельный случай ковалентной связи. На практике полный переход электронов от одного атома к другому атому по связи не реализуется, поскольку каждый элемент имеет большую или меньшую (но не нулевую) ЭО, и любая химическая связь будет в некоторой степени ковалентной. Такая связь возникает в случае большой разности ЭО атомов, например, между катионами s -металлов первой и второй групп периодической системы и анионами неметаллов VIА и VIIА групп (LiF, NaCl, CsF и др.). В отличие от ковалентной связи, ионная связь не обладает направленностью. Это объясняется тем, что электрическое поле иона обладает сферической симметрией, т.е. убывает с расстоянием по одному и тому же закону в любом направлении. Поэтому взаимодействие между ионами независимо от направления. Взаимодействие двух ионов противоположного знака не может привести к полной взаимной компенсации их силовых полей. В силу этого у них сохраняется способность притягивать ионы противоположного знака и по другим направлениям. Следовательно, в отличие от ковалентной связи, ионная связь характеризуется также ненасыщаемостью. Отсутствие у ионной связи направленности и насыщаемости обуславливает склонность ионных молекул к ассоциации. Все ионные соединения в твердом состоянии имеют ионную кристаллическую решетку, в которой каждый ион окружен несколькими ионами противоположного знака. При этом все связи данного иона с соседними ионами равноценны. Металлическая связь Металлы характеризуются рядом особых свойств: электро- и теплопроводностью, характерным металлическим блеском, ковкостью, высокой пластичностью, большой прочностью. Эти специфические свойства металлов можно объяснить особым типом химической связи, получившей название металлической.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-12-11; просмотров: 440; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.119 (0.007 с.) |

 6С* 1s22s12p3.
6С* 1s22s12p3. 1
1






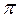 -связи в молекуле бензола С6Н6
-связи в молекуле бензола С6Н6


