
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Работа и теплота. Первое начало термодинамикиСодержание книги
Поиск на нашем сайте
Внутренняя энергия газа (и другой термодинамической системы) может изменяться в основном за счет двух процессов: совершения над газом работы
DQ = DU + DA. (10.3) Уравнение (10.3) представляет собой содержание первого начала (закона) термодинамики. Словами его можно выразить следующим образом: количество тепла DQ, сообщенное системе, идет на приращение внутренней энергии системы DU и на совершение системой работы DA над внешними телами. Следует отметить, что в равенстве (10.3) величина U является функцией состояния и однозначно определяется термодинамическими параметрами состояния. Величины Q и A не есть функции состояния. Они зависят не только от начального и конечного состояния системы, но и от пути изменения ее состояния. Из равенства (10.3) следует, что единицей измерения тепла служит джоуль. Работа газовых изопроцессов
dA = pdV (10.4) суммируют все элементарные работы для этого газового процесса. Полная работа A = где V1 - начальный объем газа, V2 - его конечный объем. Применим формулу (10.5) для расчета работы изопроцессов. 1. Рассмотрим изохорический процесс. Для этого процесса объем газа V = const, dV = 0 и A = 0. Газ не совершает работу. Первое начало термодинамики (10.3) будет иметь вид DQ = DU, т.е. все тепло, сообщенное газу, пойдет на его нагревание. 2. Рассмотрим изобарический процесс. Так как давление не изменяется, то его как постоянную величину можно вынести из под знака интеграла (10.5). Получим A = p(V2 - V1) или с учетом уравнения Менделеева-Клапейрона pV = (m /m)RT, записанного для начального и конечного состояний, получим выражение для работы изобарического процесса A = (m /m)R(T2 - T1). (10.6) 3. Рассмотрим изотермический процесс. Так как температура постоянна, то внутренняя энергия идеального газа не изменяется: DU = 0. Первое начало термодинамики (10.3) будет иметь вид DQ = DA, т.е. все тепло, подведенное к системе, будет затрачено на совершение ею работы. Используя уравнение состояния идеального газа (10.6) и учтя, что T = const, запишем выражение (10.5) для работы изотермического процесса в виде A =
|
|||||
|
Последнее изменение этой страницы: 2016-12-11; просмотров: 339; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.191.210.103 (0.01 с.) |

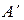 и сообщением ему количества тепла Q. Так как состояние газа может одинаково изменяться от совершенной над ним работы
и сообщением ему количества тепла Q. Так как состояние газа может одинаково изменяться от совершенной над ним работы  Исторически развитие термодинамики было связано с необходимостью теоретического объяснения работы теплового двигателя. При сжигании топлива выделялось определенное количество тепла, и некоторая часть его DQ (рис.10.2) передавалась рабочему телу (обычно газу). Газ нагревался, и его внутренняя энергия увеличивалась на величину DU. Расширяясь, газ совершал работу DA. Отсюда принято считать DQ > 0, когда термодинамическая система получает тепло, и DA > 0, когда эта система совершает работу. Огромная совокупность опытных фактов с учетом законов сохранения показывала, что в термодинамической системе, в которой протекают тепловые и механические процессы, всегда должно выполняться равенство
Исторически развитие термодинамики было связано с необходимостью теоретического объяснения работы теплового двигателя. При сжигании топлива выделялось определенное количество тепла, и некоторая часть его DQ (рис.10.2) передавалась рабочему телу (обычно газу). Газ нагревался, и его внутренняя энергия увеличивалась на величину DU. Расширяясь, газ совершал работу DA. Отсюда принято считать DQ > 0, когда термодинамическая система получает тепло, и DA > 0, когда эта система совершает работу. Огромная совокупность опытных фактов с учетом законов сохранения показывала, что в термодинамической системе, в которой протекают тепловые и механические процессы, всегда должно выполняться равенство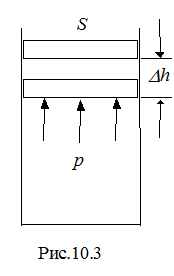 Пусть газ заключен в цилиндрический сосуд, закрытый плотно пригнанным и легко скользящим поршнем (рис.10.3). При расширении газ будет совершать работу DA = FDh, где F - сила, с которой газ действует на площадь поршня S; Dh - перемещение поршня при расширении газа. Приращение объема газа DV = SDh. Подставляя силу F = pS и DV в выражение для работы, получим DA = pDV. При расширении газа работа будет положительной, при сжатии - отрицательной. Если давление газа при совершении работы изменяется, то находят работу при каждом элементарном изменении объема
Пусть газ заключен в цилиндрический сосуд, закрытый плотно пригнанным и легко скользящим поршнем (рис.10.3). При расширении газ будет совершать работу DA = FDh, где F - сила, с которой газ действует на площадь поршня S; Dh - перемещение поршня при расширении газа. Приращение объема газа DV = SDh. Подставляя силу F = pS и DV в выражение для работы, получим DA = pDV. При расширении газа работа будет положительной, при сжатии - отрицательной. Если давление газа при совершении работы изменяется, то находят работу при каждом элементарном изменении объема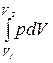 , (10.5)
, (10.5)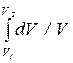 = (m /m)RT ln(V2 /V1). (10.7)
= (m /m)RT ln(V2 /V1). (10.7)


