
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Внутренняя энергия идеального газаСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте Важной величиной в термодинамике является внутренняя энергия тела. Любое тело кроме механической энергии может обладать запасом внутренней энергии, которая связана с механическим движением атомов или молекул, составляющих тело, а также с их взаимодействием. Для идеального газа его внутренняя энергия является энергией молекулярно-кинетического движения атомов или молекул этого газа. Средняя кинетическая энергия поступательного движения молекулы согласно равенству (10.10) зависит только от температуры и равна E = 3kT /2. Скорость молекул связана со своими составляющими по осям x, y и z соотношением Числом степеней свободы механической системы называется количество независимых величин, с помощью которых может быть задано положение системы. Для одноатомного газа, например гелия, каждый атом однозначно определяется заданием трех координат. Поэтому для одноатомного газа число степеней свободы i = 3. Энергией вращательного движения одноатомная молекула практически не обладает, так как ее масса сосредоточена в ядре. В силу хаотичности движения атомов средние значения энергии, приходящиеся на каждую степень свободы движения, будут одинаковыми и равными третьей части от энергии поступательного движения, т.е. равными kT/2. Полная средняя энергия поступательного движения молекулы может быть представлена в виде eпост = i kT/2. Если молекула газа состоит из трех или более атомов, то при хаотических соударениях молекул энергия поступательного движения молекул будет переходить в энергию вращательного движения молекул и наоборот. В результате этого получается, что средние энергии поступательного и вращательного движения многоатомных молекул одинаковы. Вращение многоатомной молекулы может происходить относительно трех независимых осей и его можно описать с помощью трех угловых величин. Поэтому вращательное движение имеет также три степени свободы движения. Полное число степеней свободы движения молекул многоатомного газа i = iпост + iвр = 3 + 3 = 6. Причем полную кинетическую энергию многоатомной молекулы можно записать в виде e = i kT/ 2. (10.1) Полученный результат Максвелл обобщил в принципе равного распределения энергии: в системе, состоящей из большого числа частиц, механическая энергия распределяется поровну между их степенями свободы движения.
Для киломоля идеального газа, содержащего NA число молекул, внутренняя энергия в соответствии с выражением (10.1) определяется соотношением Um = NA i kT/2 или Um = i RT /2, (10.2) где R - универсальная газовая постоянная. Выражение (10.2) показывает, что внутренняя энергия киломоля является функцией лишь от температуры газа. Для произвольной массы газа m получим U = i(m/m)RT/2, где m - моль газа. В реальном газе между молекулами действуют силы притяжения, которые при расширении газа будут совершать работу. Поэтому его внутренняя энергия будет зависеть не только от температуры, но и от объема. Для реального газа внутренняя энергия будет являться функцией только от температуры и объема: U = f(T,V). Если реальный газ вернется в некоторое прежнее состояние, то его внутренняя энергия будет иметь прежнее значение.
|
||
|
Последнее изменение этой страницы: 2016-12-11; просмотров: 539; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.156 (0.008 с.) |

 . Умножая это равенство на m/2, получим
. Умножая это равенство на m/2, получим 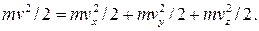 . Из последнего равенства следует, что кинетическая энергия поступательного движения молекул складывается из трех независимых составляющих, связанных с осями координат. Поэтому говорят, что молекула имеет три степени свободы движения.
. Из последнего равенства следует, что кинетическая энергия поступательного движения молекул складывается из трех независимых составляющих, связанных с осями координат. Поэтому говорят, что молекула имеет три степени свободы движения. Эксперимент подтверждает этот принцип. Например, двухатомная молекула в среднем обладает энергией вращательного движения относительно лишь двух осей вращения y и z (рис.10.1), и поэтому обладает двумя степенями свободы вращательного движения. Общее число степеней свободы движения двухатомной молекулы i = i пост+ i вр= 3 + 2 = 5.
Эксперимент подтверждает этот принцип. Например, двухатомная молекула в среднем обладает энергией вращательного движения относительно лишь двух осей вращения y и z (рис.10.1), и поэтому обладает двумя степенями свободы вращательного движения. Общее число степеней свободы движения двухатомной молекулы i = i пост+ i вр= 3 + 2 = 5.


