Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Внутренняя энергия реального газаСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
Внутренняя энергия реального газа складывается из кинетической энергии теплового движения его молекул (определяет внутреннюю энергию идеального газа, равную CVT; см. § 53) и потенциальной энергии межмолекулярного взаимодействия. Потенциальная энергия реального газа обусловлена только силами притяжения между молекулами. Наличие сил притяжения приводит к возникновению внутреннего давления на газ (см. (61.1)):
Работа, которая затрачивается для преодоления сил притяжения, действующих между молекулами газа, как известно из механики, идет на увеличение потенциальной энергии системы, т. е. dA = p'dVm = d∏,или
(постоянная интегрирования принята равной нулю). Знак минус означает, что молекулярные силы, создающие внутреннее давление р', являются силами притяжения (см. § 60). Учитывая оба слагаемых, получим, что внутренняя энергия моля реального газа
растет с повышением температуры и увеличением объема. Если газ расширяется без теплообмена с окружающей средой (адиабатический процесс, т. е. dQ = 0 ) и не совершает внешней работы (расширение газа в вакуум, т. е. dА = 0),то на основании первого начала термодинамики (dQ = (U2 – U1) + dA) получим, что
Следовательно, при адиабатическом расширении без совершения внешней работы внутренняя энергия газа не изменяется. Равенство (63.2) формально справедливо как для идеального, так и для реального газов, но физический смысл его для обоих случаев совершенно различен. Для идеального газа равенство Ut = U2означает равенство температур (T1 = T2), т. е. при адиабатическом расширении идеального газа в вакуум его температура не изменяется. Для реального газа из равенства (63.2), учитывая, что для моля газа
Так как V2 > V1 (то Т1 > Т2,т. е. реальный газ при адиабатическом расширении в вакуум охлаждается. При адиабатическом сжатии в вакуум реальный газ нагревается.
Эффект Джоуля — Томсона
Если идеальный газ адиабатически расширяется и совершает при этом работу, то он охлаждается, так как работа в данном случае совершается за счет его внутренней энергии (см. § 55). Подобный процесс, но с реальным газом — адиабатическое расширение реального газа с совершением внешними силами положительной работы— осуществили английские физики Дж. Джоуль (1818—1889) и У. Томсон (лорд Кельвин, 1824—1907).
Рис. 93
Рассмотрим эффект Джоуля — Томсона. На рис. 93 представлена схема их опыта. В теплоизолированной трубке с пористой перегородкой находятся два поршня, которые могут перемещаться без трения. Пусть сначала слева от перегородки газ под поршнем 1 находится под давлением p1, занимает объем V1при температуре T1, а справа газ отсутствует (поршень 2 придвинут к перегородке). После прохождения газа через пористую перегородку в правой части газ характеризуется параметрами р2, V2, Т2. Давления p1 и p2поддерживаются постоянными (р1 > р2). Так как расширение газа происходит без теплообмена с окружающей средой (адиабатически), то на основании первого начала термодинамики
Внешняя работа, совершаемая газом, состоит из положительной работы при движении поршня 2 (A2 = p2V2)и отрицательной при движении поршня 1 (A1 = p1V1),т. е. dА = А2 —А1. Подставляя выражения для работ в формулу (64.1), получаем
Таким образом, в опыте Джоуля — Томсона сохраняется (остается неизменной) вели чина U+pV. Она является функцией состояния и называется энтальпией. Ради простоты рассмотрим 1 мольгаза. Подставляя в формулу (64.2) выражение (63.3) и рассчитанные из уравнения Ван-дер-Ваальса (61.2) значения p1V1 и p2V2 (символ «m» опять опускаем) и производя элементарные преобразования, получаем
Из выражения (64.3) следует, что знак разности (Т2 – T1)зависит от того, какая из поправок Ван-дер-Ваальса играет большую роль. Проанализируем данное выражение, сделав допущение, что p2 ≈ p1 и V2 ≈ V1 1) а ≈ 0 — не учитываем силы притяжения между молекулами, а учитываем лишь размеры самих молекул. Тогда
т. е. газ в данном случае нагревается; 2) b ≈ 0— не учитываем размеров молекул, а учитываем лишь силы притяжения между молекулами. Тогда
т. е. газ в данном случае охлаждается; 3) учитываем обе поправки. Подставив в выражение (64.3) вычисленное из уравнения Ван-дер-Ваальса (61.2) значение р1 имеем
т. е. знак разности температур зависит от значений начального объема V1и начальной температуры T1. Изменение температуры реального газа в результате его адиабатического расширения, или, как говорят, адиабатического дросселирования — медленного прохождения газа под действием перепада давления сквозь дроссель (например, пористую перегородку), называется эффектом Джоуля — Томсона. Эффект Джоуля — Томсона принято называть положительным, если газ в процессе дросселирования охлаждается (DT < 0), и отрицательным, если газ нагревается (DT > 0). В зависимости от условий дросселирования для одного и того же газа эффект Джоуля — Томсона может быть как положительным, так и отрицательным. Температура, при которой (для данного давления) происходит изменение знака эффекта Джоуля — Томсона, называется температурой инверсии. Ее зависимость от объема получим, приравняв выражение (64.4) нулю:
Кривая, определяемая уравнением (64.5), — кривая инверсии — приведена на рис. 94. Область выше этой кривой соответствует отрицательному эффекту Джоуля — Томсона, ниже — положительному. Отметим, что при больших перепадах давления на дросселе температура газа изменяется значительно. Так, при дросселировании от 20 до 0,1 МПа и начальной температуре 17° С воздух охлаждается на 35° С.
Рис. 94
Эффект Джоуля — Томсона обусловлен отклонением газа от идеальности. В самом деле, для моля идеального газа pVm=RT, поэтому выражение (64.2) примет вид
откуда следует, что T1= T2.
Сжижение газов
Превращение любого газа в жидкость — сжижение газа — возможно лишь при температуре ниже критической (см. § 62). При ранних попытках сжижения газов оказалось, что некоторые газы (С12, СО2, NH3) легко сжижались изотермическим сжатием, а целый ряд газов (О2, N2, hz, Не) сжижению не поддавался. Подобные неудачные попытки объяснил Д. И. Менделеев, показавший, что сжижение этих газов производилось при температуре, большей критической, и поэтому заранее было обречено на неудачу. Впоследствии удалось получить жидкий кислород, азот и водород (их критические температуры равны соответственно 154,4, 126,1 и 33 К), а в 1908 г. нидерландский физик Г. Камерлинг-Оннес (1853—1926) добился сжижения гелия, имеющего самую низкую критическую температуру (5,3 К). Для сжижения газов чаще применяются два промышленных метода, в основе которых используется либо эффект Джоуля — Томсона, либо охлаждение газа при совершении им работы. Схема одной из установок, в которой используется эффект Джоуля—Томсона, — машины Линде* — представлена на рис. 95. Воздух в компрессоре (К) сжимается до давления в десятки мегапаскаль и охлаждается в холодильнике (X) до температуры ниже температуры инверсии, в результате чего при дальнейшем расширении газа наблюдается положительный эффект Джоуля — Томсона (охлаждение газа при его расширении). Затем сжатый воздух проходит по внутренней трубе теплообменника (ТО) и пропускается через дроссель (Др), при этом он сильно расширяется и охлаждается. Расширившийся воздух вновь засасывается по внешней трубе теплообменника, охлаждая вторую порцию сжатого воздуха, текущего по внутренней трубе. Так как каждая следующая порция воздуха предварительно охлаждается, а затем пропускается через дроссель, то температура понижается все больше. В результате 6—8-часового цикла часть воздуха (» 5%), охлаждаясь до температуры ниже критической, сжижается и поступает в дьюаровский сосуд (ДС) (см. § 49), а остальная его часть возвращается в теплообменник.
Рис. 95
Второй метод сжижения газов основан на охлаждении газа при совершении им работы. Сжатый газ, поступая в поршневую машину (детандер), расширяется и совершает при этом работу по передвижению поршня. Так как работа совершается за счет внутренней энергии газа, то его температура при этом понижается. Академик П. Л. Капица предложил вместо детандера применять турбодетандер, в котором газ, сжатый всего лишь до 500—600 кПа, охлаждается, совершая работу по вращению турбины. Этот метод успешно применен Капицей для сжижения гелия, предварительное охлаждение которого производилось жидким азотом. Современные мощные холодильные установки работают по принципу турбодетандера.
|
||||
|
Последнее изменение этой страницы: 2016-04-19; просмотров: 1023; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.218.108.8 (0.008 с.) |

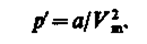
 , откуда
, откуда
 (63.1)
(63.1)

 (63.3)
(63.3)
 (64.1)
(64.1) (64.2)
(64.2) 4.3)
4.3)

 (64.4)
(64.4) (64.5)
(64.5)