
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Уравнение Клапейрона — МенделееваСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
Как уже указывалось, состояние некоторой массы газа определяется тремя термодинамическими параметрами: давлением р, объемом V и температурой Т. Между этими параметрами существует определенная связь, называемая уравнением состояния, которое в общем виде дается выражением
где каждая из переменных является функцией двух других. Французский физик и инженер Б. Клапейрон (1799—1864) вывел уравнение состояния идеального газа, объединив законы Бойля — Мариотта и Гей-Люссака. Пусть некоторая масса газа занимает объем V1, имеет давление p1и находится при температуре T1. Эта же масса газа в другом произвольном состоянии характеризуется параметрами р2, V2, Т2(рис. 63). Переход из состояния 1 в состояние 2 осуществляется в виде двух процессов: 1) изотермического (изотерма 1 — 1¢, 2) изохорного (изохора 1¢ - 2).
Рис. 63
В соответствии с законами Бойля — Мариотта (41.1) и Гей-Люссака (41.5) запишем:
Исключив из уравнений (42.1) и (42.2) p¢1, получим
Так как состояния 1 и 2 были выбраны произвольно, то для данной массы газа величина pV/T остается постоянной, т. е.
Выражение (42.3) является уравнением Клапейрона, в котором В — газовая постоянная, различная для разных газов. Русский ученый Д. И. Менделеев (1834—1907) объединил уравнение Клапейрона с законом Авогадро, отнеся уравнение (42.3) к одному молю, использовав молярный объем Vm. Согласно закону Авогадро, при одинаковых р и Т моли всех газов занимают одинаковый молярный объем Vm, поэтому постоянная B будет одинаковой для всех газов. Эта общая для всех газов постоянная обозначается R и называется молярной газовой постоянной. Уравнению
удовлетворяет лишь идеальный газ, и оно является уравнением состояния идеального газа, называемым также уравнением Клапейрона — Менделеева. Числовое значение молярной газовой постоянной определим из формулы (42.4), полагая, что моль газа находится при нормальных условиях (р0= 1,013×105 Па, T0 = 273,15 К, Vm = 22,41×10-3 мэ/моль): R = 8,31 Дж/(моль×К). От уравнения (42.4) для моля газа можно перейти к уравнению Клапейрона — Менделеева для произвольной массы газа. Если при некоторых заданных давлении и температуре один моль газа занимает молярный объем Vm, то при тех же условиях масса m газа займет объем V= (т/М)× Vm, где М — молярная масса (масса одного моля вещества). Единица молярной массы — килограмм на моль (кг/моль). Уравнение Клапейрона — Менделеева для массы т газа
где v=m/M — количество вещества. Часто пользуются несколько иной формой уравнения состояния идеального газа, вводя постоянную Больцмана:
Исходя из этого уравнение состояния (42.4) запишем в виде
где NA/Vm = n— концентрация молекул (число молекул в единице объема). Таким образом, из уравнения
следует, что давление идеального газа при данной температуре прямо пропорционально концентрации его молекул (или плотности газа). При одинаковых температуре и давлении все газы содержат в единице объема одинаковое число молекул. Число молекул, содержащихся в 1 м3 газа при нормальных условиях, называется числом Лошмндта*:
Основное уравнение Молекулярно-кинетической теории Идеальных газов
Для вывода основного уравнения молекулярно-кинетической теории рассмотрим одно атомный идеальный газ. Предположим, что молекулы газа движутся хаотически, число взаимных столкновений между молекулами газа пренебрежимо мало по сравнению с числом ударов о стенки сосуда, а соударения молекул со стенками сосуда абсолютно упругие. Выделим на стенке сосуда некоторую элементарную площадку D S (рис. 64) и вычислим давление, оказываемое на эту площадку. При каждом соударении молекула, движущаяся перпендикулярно площадке, передает ей импульс m0v - (- т0) = 2 т0v, где m0 — масса молекулы, v — ее скорость. За время D t площадки D S достигнут только те молекулы, которые заключены в объеме цилиндра с основанием D S и высотой vDt (рис. 64). Число этих молекул равно nDSvDt (n— концентрация молекул).
Рис. 64
Необходимо, однако, учитывать, что реально молекулы движутся к площадке DS под разными углами и имеют различные скорости, причем скорость молекул при каждом соударении меняется. Для упрощения расчетов хаотическое движение молекул заменяют движением вдоль трех взаимно перпендикулярных направлений, так что в любой момент времени вдоль каждого из них движется 1/3 молекул, причем половина молекул - 1/6 - движется вдоль данного направления в одну сторону, половина — в противоположную. Тогда число ударов молекул, движущихся в заданном направлении, о площадку D S будет l/6 nDSvDt. При столкновении с площадкой эти молекулы передадут ей импульс
Тогда давление газа, оказываемое им на стенку сосуда,
Если газ в объеме V содержит N молекул, движущихся со скоростями v1,v2,..., vn, то целесообразно рассматривать среднюю квадратичную скорость
характеризующую всю совокупность молекул таза. Уравнение (43.1) с учетом (43.2) примет вид
Выражение (43.3) называется основным уравнением молекулярно-кинетнческой теории идеальных газов. Точный расчет с учетом движения молекул по всевозможным направлениям дает ту же формулу.
Учитывая, что n=N/V, получим где Е — суммарная кинетическая энергия поступательного движения всех молекул газа. Так как масса газа m=Nm0, то уравнение (43.4) можно переписать в виде
Для одного моля газа т = М (М — молярная масса), поэтому
где Fm — молярный объем. С другой стороны, по уравнению Клапейрона — Менделеева, pVm = RT. Таким образом,
откуда
Так как M = m0NA — масса одной молекулы, а NА — постоянная Авогадро, то из уравнения (43.6) следует, что
где k=R/NA— постоянная Больцмана. Отсюда найдем, что при комнатной температуре молекулы кислорода имеют среднюю квадратичную скорость 480 м/с, водорода — 1900 м/с. При температуре жидкого гелия те же скорости будут соответственно 40 и 160 м/с. Средняя кинетическая энергия поступательного движения одной молекулы идеального газа
(использовали формулы (43.5) и (43.7)) пропорциональна термодинамической температуре и зависит только от нее. Из этого уравнения следует, что при Т=0 <e0> = 0, т. е. при 0 К прекращается поступательное движение молекул газа, а следовательно, его давление равно нулю. Таким образом, термодинамическая температура является мерой средней кинетической энергии поступательного движения молекул идеального газа, и формула (43.8) раскрывает молекулярно-кинетическое толкование температуры.
|
|||||
|
Последнее изменение этой страницы: 2016-04-19; просмотров: 1048; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.118.24.176 (0.01 с.) |



 (42.1) (42.2)
(42.1) (42.2)
 (42.3)
(42.3) (42.4)
(42.4) (42.5)
(42.5)

 (42.6)
(42.6)


 (43.1)
(43.1) (43.2)
(43.2)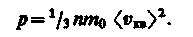 (43.3)
(43.3) (43.4) (43.5)
(43.4) (43.5)


 (43.6)
(43.6)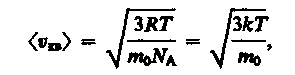 (43.7)
(43.7) (43.8)
(43.8)


