
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Решение. Из уравнения менделеева – клапейронаСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
PV= получим плотность:
Откуда, подставив численные значения, имеем:
Пример 3. Найти молярную массу воздуха, считая, что он состоит из одной части кислорода и трех частей азота.
Решение. Воздух, являясь смесью идеальных газов, тоже представляет собой идеальный газ, и к нему можно применить уравние Менделеева–Клапейрона: PV= Для каждого компонента смеси (кислорода и азота) имеем:
где По закону Дальтона Рвозд = Сложив (2) и (3), получим ( или на основании закона Дальтона PV= Сравнив (1) и (5) с учетом того, что mвозд =m
Откуда
Подставив в (6) равенство m
Пример 4. Плотность некоторого газа равна 6·10-2 кг/м3, а среднеквадратичная скорость молекул – 500 м/с. Найти давление, которое газ оказывает на стенку сосуда. Решение. В основном уравнении молекулярно- кинетической теории –
Произведение nm выражает массу молекул, содержащихся в единице объема вещества, и следовательно, равно плотности ρ газа. Таким образом,
Пример 5. 6,5 г водорода, температура которого 270 С, расширяется вдвое при постоянном давлении за счет притока тепла извне. Найти: а) изменение внутренней энергии; б) количество теплоты, сообщенной газу; в) работу расширения. (Мв=2×10-3 кг/моль). Решение. Вычислим значения молярных теплоемкостей водорода, учитывая, что молекулы водорода – двухатомные, а число i степеней свободы равно пяти:
Cр =Cv + R=20,8·103 + 8,31·103 =29,1·103 Дж/моль×К. Используя условие задачи и уравнение для изобарического процесса
найдем температуру газа после расширения: Т2 = Вычислим изменение внутренней энергии и количество тепла:
На основании первого начала термодинамики найдем работу расширения газа: А=Q–∆U=28,4·103–20,3·103 Дж=8,1·103 Дж.
Пример 6. Воздух, занимавший объем V1=10 л при давлении Р1=100 кПа, был адиабатически сжат до объема V2 =1 л. Под каким давлением Р2 находится воздух после сжатия? Решение. Поскольку совершается адиабатический процесс, для решения используем уравнение адиабаты в виде
Отсюда следует, что
Показатель Пуассона –
где i=5, так как считаем воздух состоящим в основном из двухатомных молекул. Подставив в формулу для P2 численные значения величин, получим: P2 = В итоге логарифмирования имеем
Пример 7. Тепловая машина работает по обратному циклу Карно. Температура теплоотдатчика Т1=500 К. Определить термический кпд цикла и температуру Т2 теплоприемника тепловой машины, если за счет каждого килоджоуля теплоты, полученной от теплоотдатчика, машина совершает работу А=350Дж. Решение. Термический кпд тепловой машины показывает, какая доля теплоты, полученной от теплоотдатчика, превращается в механическую работу:
где А – работа, совершаемая рабочим телом; Q1 – теплота, полученная от теплоотдатчика. По формуле η=
зная η цикла, можно определить температуру охладителя Т2 :
Произведем вычисления:
Пример 8. Один моль газа совершает цикл, состоящий из 2-х изохор и 2-х изобар (см. рисунок). Температуры, соответствующие состояниям 1 и 3, –Т1 и Т3. Определить работу, совершенную газом за цикл, если известно, что точки 2 и 4 лежат на одной изотерме.
V1 V2 V
Решение. Состояние 1 характеризуется параметрами p1,V1,T1, состояние 2– параметрами p2,V2 ,T2 , состояние 3 – соответственно p3,V3,T3, состояние 4 – p4,V4,T4 (T4 = T2; V1=V2; V3=V4). Из рисунка видно, что А = (Р2 – Р1) (V3 –V1), (1) так как работа за цикл численно равна площади прямоугольника 1-2-3-4. Поскольку T4 = T2, то Р2 V1 = Р1 V3. (2) Из уравнения Менделеева-Клапейрона для 1 моля газа: Р1 V1 = RT1 Р2 V3 = RT3. Откуда
Как следует из уравнения (2),
Тогда
2.3. ЗАДАНИЯ
Вариант 1 1. Подсчитать число молекул, содержащихся в углекислом газе массой 100 г. Найти массу молекулы и концентрацию молекул при нормальных условиях. Плотность газа при нормальных условиях равна 1,94 кг/м3 . 2. Какое давление на стенки сосуда оказывает кислород, если скорость его молекул равна 400 м/с, а в 1 см3 – 2,7·1019 молекул? 3. Плотность газа в баллоне газонаполненной электрической лампы равна 0,9 кг/м3. При горении лампы давление в ней возросло с 80 кПа до 110 кПа. Насколько увеличилась при этом среднеквадратичная скорость молекул газа? 4. До какой температуры при постоянном давлении 105 Па надо нагреть кислород, чтобы его плотность стала равна плотности водорода при том же давлении и температуре 200 К? 5. Для нагревания газа массой 1 кг на 1К при постоянном давлении требуется 912 Дж теплоты, а при постоянном объеме – 649 Дж теплоты. Какой это газ? 6. Определить, во сколько раз среднеквадратичная скорость пылинки массой 1,75·10-12 кг, взвешенной в воздухе, меньше среднеквадратичной скорости движения молекул воздуха. 7. Найти формулу некоторого соединения углерода с водородом, если известно, что это вещество массой 0,66 г в газообразном состоянии при температуре 270С в объеме 1 дм3 создает давление 105 Па. 8. В сосуде при давлении 105 Па и температуре 270 С находится смесь азота, кислорода и гелия, массы которых равны. Найти плотность смеси газов. 9. В вертикальном цилиндре под тяжелым поршнем находится кислород массой 2 кг. Для повышения температуры кислорода на 5 К ему было сообщено 9160 Дж теплоты. Найти удельную теплоемкость кислорода ср, работу, совершаемую им при расширении и увеличении его внутренней энергии. Молярная масса кислорода 0,032 кг/моль. 10. Одноатомный идеальный газ находятся в баллоне объемом 10 л при давлении 105 Па. Какова внутренняя энергия газа? 11. В закрытом сосуде находится 3 моля гелия при температуре 270 С. На сколько процентов увеличится давление в сосуде, если газу сообщить 3 кДж теплоты?
Вариант 2 1. Какая масса углекислого газа СО2 растворена в бутылке с лимонадом объемом 0,5 л, если на одну молекулу газа приходится 5,56×105 молекул воды? 2. Из баллона со сжатым газом вследствие неисправности вентиля вытекал газ. Какая часть газа осталась в баллоне, если первоначально при температуре 27°С манометр показывал 60 атм, а через некоторое время при температуре 12°С – 19 атм? 3. Средняя энергия молекулы одноатомного идеального газа равна 0,038 эВ (1эВ =1,6×10-19 Дж). Давление газа равно 0,2 МПа. Найти число молекул в одном кубическом метре газа. 4. При некоторой температуре молекулы кислорода имеют среднеквадратичную скорость 460 м/с. Какова при этой температуре среднеквадратичная скорость молекул азота? 5. При давлении 2×106 Па идеальный газ занимает объем 5 литров. В результате изотермического расширения его объем увеличился на 1 л, а концентрация молекул стала равной n=3,62×1026 м-3. При какой температуре протекал этот процесс? 6. Два сосуда, наполненных воздухом при давлениях соответственно Р1 =0,8 МПа и Р2 =0,6 МПа, имеют объемы V1 =3л и V2 =5л. Сосуды соединяют трубкой, объемом которой можно пренебречь по сравнению с объемами сосудов. Найти установившееся давление в сосудах. Температуру считать постоянной. 7. Аэростат объемом 300 м3 наполняется молекулярным водородом при температуре 300 К и давлении 105 Па. Какое время будет наполняться оболочка аэростата, если из баллонов каждую секунду переходит в аэростат 25 г водорода? До заполнения газом оболочка аэростата водорода не содержала. Газ считать идеальным. 8. Три баллона емкостями V1 =3 л, V2 =7 л, V3 =5 л наполнены соответственно кислородом (до давления р1=2 атм), азотом (р2=3 атм) и углекислым газом (р3=0,6 атм) при одной и той же температуре. Баллоны соединяют между собой, причем образуется смесь той же температуры. Найти давление смеси. 9. В цилиндре объемом V1 =190 см3 под поршнем находится газ при температуре Т1=323 К. Найти работу расширения газа при нагревании его на ∆Т=100 К. Масса поршня m = 120 кг, его площадь S = 50 см 2. Атмосферное давление р0 =0,1 МПа. 10. Некоторая масса газа, занимающего объем V1 = 0,01 м 3, находится при давлении р1 =0,1 МПа и температуре Т1 = 300 К. Газ нагревается вначале при постоянном объеме до температуры Т2 = 320 К, а затем при постоянном давлении до температуры Т3 = 350 К. Найти работу, совершаемую газом, при переходе из состояния 1 в состояние 3. 11. Коэффициент полезного действия цикла Карно равен 0,3. При изотермическом расширении газ получил от нагревателя 200 Дж энергии. Определить работу, совершаемую при изотермическом сжатии. Вариант 3 1. Какое давление на стенки сосуда производят молекулы газа, если масса газа 3 г, объем 50 л, а средняя скорость молекул 500 м/с? 2. Радоновые ванны содержат N=1,8×106 атомов радона на объем воды V=1дм3. На сколько молекул воды приходится один атом радона? 3. Определить плотность смеси газов, находящихся при давлении 1 МПа и температуре 270С. Смесь состоит из 5 киломолей азота, 1,5 киломолей кислорода и 0,5 киломоля углекислого газа. 4. Закрытый сосуд заполнен смесью газов, состоящей из неона, масса которого 4 г, и аргона, масса которого 1 г. Газы считать идеальными. Определить удельную теплоемкость этой смеси газов. 5. В неплотно закрытом баллоне объемом V =10-2 м3 при температуре Т= 239К и давлении р=10 МПа находился водород. Сколько водорода было потеряно, если из оставшегося водорода может образоваться вода массой m=0,5кг? 6. В воздухе взвешена пылинка массой m=1,242×10-20 кг. Температура воздуха Т=300 К. Подсчитать среднеквадратичную скорость пылинки и ее кинетическую энергию. 7. Какую работу совершает кислород массой m = 0,32 кг при изобарном нагревании на ∆Т=20 К? 8. Какова температура Т газа, находящегося под давлением р=0,5 МПа, если в сосуде объемом V =1,5 л содержится N = 1,8×1024 молекул? 9. Некоторая масса газа находится в баллоне объемом V = 1л. После выпуска части газа из баллона давление в нем уменьшилось на ∆р=56 кПа, а масса баллона с газом уменьшилась на ∆m= 2 г. Температура газа при этом не изменилась. Найти плотность r0 газа при нормальном давлении р0 =0,1 МПа и температуре опыта. 10. Один киломоль газа при изобарическом расширении совершает работу А=831 кДж. В исходном состоянии объем газа V1 =3 м3 , а температура Т1=300 К. Каковы параметры р2,V2,T2 после расширения? 11. Температура нагревателя 2270 С. Определите кпд идеального двигателя и температуру холодильника, если за счет каждого килоджоуля теплоты, полученного от нагревателя, двигатель совершает 350 Дж механической работы. Вариант 4 1. В сосуде при температуре 1000С и давлении 4×105 Па находится 2 м3 смеси кислорода и сернистого газа. Определить парциальное давление компонентов, если масса сернистого газа 8 кг. 2. Плотность неизвестного газа равна 0,09кг/м3 . При этом в объеме 0,1 м3 содержится 2,7×1024 молекул. Какой это газ? Определите его молярную массу. 3. В закрытом сосуде находится смесь азота массой 56 г и кислорода массой 64 г. Определить изменение внутренней энергии этой смеси, если ее охладили на 200 С. 4. Какова удельная теплоемкость при постоянном объеме некоторого двухатомного газа, если плотность этого газа при нормальных условиях равна 6,3 кг/м3 ? 5. Найти среднюю длину пробега молекулы азота при 00 С и давлении 10-3 мм рт.ст. 6. Вычислить плотность водорода, если известно, что число его молекул в сосуде вдвое больше числа Авогадро, а объем сосуда равен 40 л. 7. Баллон с предохранительным клапаном содержит водород при температуре 150С и давлении 105 Па. При нагревании баллона до температуры 370С через клапан выходит водород массой 6 кг, вследствие чего давление не изменяется. Определить объем баллона. 8. Какая работа совершается при изотермическом расширении водорода массой 823 г, взятого при температуре 214 К, если его объем увеличился в 7 раз? 9. Во сколько раз изменится среднеквадратичная скорость молекул идеального газа при увеличении его объема в 2 раза? Давление газа при этом увеличится в 3 раза, масса неизменна. 10. Водород массой 40 г, имевший температуру 300 К, адиабатически расширяется; при этом объем газа возрастает втрое. Затем при изотермическом сжатии объем газа уменьшается в 2 раза. Определить полную работу, совершенную газом, и конечную температуру газа. Построить график процесса. 11. Газ совершает цикл Карно; 2/3 теплоты, полученной от нагревателя, отдается охладителю. Температура охладителя 280 К. Определить температуру нагревателя.
Вариант 5 1. Молекула кислорода, ударившись о стенку сосуда, передала ей импульс ∆р=5,06×10-23 кг×м/с. Найти температуру газа в сосуде, если скорость данной молекулы была направлена под углом a = 300 к стенке и равнялась удвоенной среднеквадратичной скорости. 2. Некоторая масса водорода находится при температуре Т1 =200 К и давлении р1 =0,4кПа. Газ нагревают до температуры Т2 =10000 К, при которой молекулы водорода практически полностью распадаются на атомы. Найти давление р2 газа, если его объем и масса остались без изменения. 3. В закрытом воздухе объемом 61 л находятся равные массы аргона и азота при нормальных условиях. Какое количество теплоты нужно сообщить этой газовой смеси, чтобы нагреть ее на 600 С? 4. В теплоизолированном цилиндре с поршнем находится азот массой m=0,2 кг при температуре t1=200 C. Азот, расширяясь, совершает работу А= 4,47 кДж. Найти изменение внутренней энергии азота ΔU и его температуру t2 после расширения. Удельная теплоемкость азота при постоянном объеме – Сv =745 Дж/кг×К 5. Сосуд разделен пополам полупроницаемой перегородкой. Объем каждой части – 1 л. В левую половину введены водород массой 2 г и азот массой 28 г. Справа от перегородки – вакуум. Какое давление установится в обеих частях сосуда, если перегородка пропускает только водород, а температура остается постоянной и равной 373 К? 6. Объем газа при адиабатическом сжатии уменьшился в 10 раз, а давление увеличилось в 21,4 раза. Определить соотношение удельной теплоемкости при постоянном давлении и удельной теплоемкости при постоянном объеме. 7. Один киломоль одноатомного идеального газа находится при температуре Т1 =400К и под давлением р1=106 Па. В результате изохорического процесса внутренняя энергия газа изменилась на ΔU= –12,5×105 Дж. Определить параметры конечного состояния газа (V2; p2; T2). 8. Некоторая масса газа, занимающего объем V1 =0,01 м3 , находится под давлением р1 =1×105 Па (при температуре T1 =300К). Газ нагревают при постоянном объеме до температуры T2 =320К, а затем при постоянном давлении – до температуры T3 =350К. Найти работу, совершаемую газом, при переходе из состояния 1 в состояние 3. 9. Кислород, занимающий при давлении 1 МПа объем 5 л, расширился в 3 раза. Определить конечное давление и работу, совершенную газом, если процесс – адиабатический. 10. Кислород массой 10 г находится под давлением 0,3 МПа и при температуре 100 С. После нагревания при постоянном давлении газ занял объем 10 л. Найти количество теплоты, полученное газом, и энергию теплового движения молекул газа до и после нагревания. 11. Газ совершает цикл Карно. Температура охладителя 170 С. Как изменится кпд цикла, если температура нагревателя повысилась от 127 до 4470 С?
Вариант 6 1. В баллоне емкостью 10 л содержится окисел азота (NO) под давлением 8 атм. Определить массу газа и массу его молекулы. Температура 15°С. 2. Из баллона со сжатым газом вследствие неисправности вентиля вытекал газ. Какая часть газа осталась в баллоне, если первоначально при температуре 27°С манометр показывал давление 60 атм, а через некоторое время при температуре 12°С – 19 атм? 3. В сосуде, объем которого 1 л, содержится 5 г идеального газа под давлением 500 гПа. Определить среднеквадратичную скорость молекул газа. 4. Удельная теплоемкость газа при постоянном давлении равна 912 Дж/кг×К, а при постоянном объеме 649 Дж/кг×К. Определить молекулярный вес газа и число степеней свободы его молекул. 5. Определить среднюю кинетическую энергию поступательного движения молекул газа, находящегося под давлением 0,3 Па. Концентрация молекул равна 1013 см-3. 6. Найти среднюю длину свободного пробега молекул азота при 0°С и давлении 10-3 мм рт. ст. Диаметр молекулы принять равным 0,3 мм. 7. 2,18 кг двухатомного газа находится под давлением 7,8·105 Па и имеет плотность 6,28 кг/м3. Найти энергию теплового движения молекул газа при этих условиях. 8. При изотермическом расширении водорода массой 1 г объем увеличился в 2 раза. Определить работу расширения и количество тепла, переданного телу. Температура водорода 300 К. 9. В баллоне, объем которого равен 10 л, находится гелий под давлением 105 Па и при температуре 27°С. После того как из баллона была взята проба массой 10 г, давление в баллоне понизилось до 0,9·105 Па. Определить температуру гелия, оставшегося в баллоне. 10. Кислород массой 2 кг занимает объем 1 м3 и находится под давлением 0,2 МПа. Газ был нагрет сначала при постоянном давлении до объема 3 м3, а затем при постоянном объеме до давления 0,5 МПа. Найти изменение внутренней энергии газа, совершаемую им работу и теплоту, переданную газу. Построить график процесса. 11. Двигатель работает как машина Карно и за цикл получает от нагревателя 3 кДж тепла. Температура нагревателя 600 К, температура холодильника 300 К. Найти совершившуюся за цикл работу и количество теплоты, отдаваемое при этом холодильнику. Вариант 7 1. Оценить концентрацию свободных электронов в натрии, полагая, что на один атом приходится один свободный электрон. Плотность натрия ρ=970 кг/м3. 2. Баллон объемом 0,015 м3 содержит 7·10-3 кг азота и 4,5·10-3 кг водорода при температуре 27°С. Определить давление смеси. 3. Средняя квадратичная скорость молекул некоторого газа равна 480 м/с при температуре 296 К. Сколько молекул содержится в 10-ти г этого газа? 4. Для повышения температуры газа, имеющего массу 20 кг и молярную массу 0, 028 кг/моль, на 50 К при постоянном давлении необходимо затратить количество теплоты 0,5 МДж. Какое количество теплоты следует отнять от этого газа при постоянном объеме, чтобы его температура понизилась на 50 К? 5. В баллоне, объем которого 719 м3, находится газ, состоящий из смеси углекислого газа и паров воды. Температура газа 513°С. Число молекул углекислого газа 8,35·1022, число молекул паров воды 5,87·1022. Вычислить давление газовой смеси. 6. Найти концентрацию молекул кислорода, если его давление равно 0,2 МПа, а средняя квадратичная скорость молекул 700 м/с. 7. Одному молю двухатомного газа сообщили 20 Дж тепла, в результате чего газ нагрелся на несколько градусов при постоянном объеме. Какое количество тепла нужно сообщить метану массой 30 г, чтобы нагреть его на такое же число градусов при постоянном давлении? 8. Одноатомный идеальный газ изотермически расширился из состояния с давлением 106 Па и объемом 1 л вдвое. Найти внутреннюю энергию газа в конечном состоянии. 9. Температура воздуха в комнате объемом 70 м3 была 280 К. После того как протопили печь, температура поднялась до 296 К. Найти работу воздуха при расширении, если давление постоянно и равно 100 кПа. 10. При изобарическом нагревании от температуры 20°С до температуры 50°С газ совершает работу в 2,5 кДж. Определить число молекул, участвующих в этом процессе. 11. Одноатомный идеальный газ, первоначально занимающий объем 2 м3, изохорически перевели в состояние, при котором его давление увеличилось на 0,2 МПа. Какое количество теплоты сообщили газу?
Вариант 8 1. В сосуде объемом 10 л находится 2·1023 молекул газа. Какова температура газа, если давление в сосуде равно 0,12 МПа? 2. В баллоне находится газ массой 10 кг при давлении 10 МПа. Какую массу взяли из баллона, если давление стало равным 2,5 МПа? Температуру газа считать постоянной. 3. На сколько процентов увеличится среднеквадратичная скорость молекул водяного пара при повышении его температуры от 370С до 400С? 4. Вычислить величину отношений удельных теплоемкостей для газовой смеси, состоящей из 5-ти киломолей кислорода и 6-ти киломолей углекислого газа. Газы считать идеальными. 5. Кинетическая энергия поступательного движения молекул азота, находящегося в баллоне объемом 6,68 м3, равна 7,9·104 Дж, а среднеквадратичная скорость его молекул составляет 7·103 м/с. Найти массу азота в баллоне. 6. Кислород, взятый при температуре 270 С, изобарически сжали до объема, в 5 раз меньшего первоначального. Определить работу внешней силы при сжатии, если масса газа равна 160 г. 7. Температура воды массой 1 кг повышается на 1 К. Найти увеличение внутренней энергии, приходящееся на одну молекулу. Удельная теплоемкость воды равна 4,2 8. Водород, находившийся под давлением 0,1 МПа, был сжат адиабатически до давления 0,3 МПа. Каково будет давление, если сжатый газ (без изменения объема) охладить до первоначальной температуры? Начертить в координатах «объем - давление» графики процессов. 9. Водород массой 2 кг при температуре 300 К охлаждают изохорически так, что его давление падает в 3 раза. Затем водород изобарически расширяют. Найти работу газа, если его конечная температура равна начальной. 10. Кислород массой 2 кг занимает объем 1 м3 и находится под давлением 0,2 МПа. При нагревании газ расширяют в условиях постоянного давления до объема 3 м3, а затем его давление увеличивают до 0,5 МПа при неизменном объеме. Найти изменение внутренней энергии газа, совершенную им работу и теплоту, переданную газу. Построить график процесса. 11. При совершении цикла Карно газ получил от нагревателя 16,8 кДж энергии и совершил 5,8 кДж работы. Во сколько раз температура нагревателя выше температуры холодильника?
Вариант 9 1. Из открытого стакана за 5 суток полностью испарилось 50 г воды. Сколько в среднем молекул вылетало с поверхности воды за 1 с? 2. Гелий находится при температуре 270 С. Кинетическая энергия теплового движения всех молекул газа Ек=10 Дж. Определить число молекул. 3. При температуре 300 К плотность газа равна 1,2 кг/м3, а среднеквадратичная скорость молекул составляет 500 м/с. Найти концентрацию молекул газа. 4. Тонкий резиновый шар радиуса 2 см заполнен воздухом при температуре 200С и давлении 0,1 МПа. Каков будет радиус шара, если его опустить в воду с температурой 40 С на глубину 20 м? 5. Определить плотность смеси, состоящей из 4 г водорода, 32 г кислорода, при температуре 70 С и давлении 93 кПа. 6. Азот массой 10 г расширяется изотермически при температуре -200 С, при этом давление меняется от 202 до 101 кПа. Определить работу расширения, изменение внутренней энергии азота и количество сообщенной ему теплоты. 7. Газ массой 12 г занимает объем 4 л при температуре 70 С. После нагревания при постоянном давлении его плотность стала равной 0,6 кг/м3. До какой температуры нагрели газ? 8. 10,5 г азота изотермически расширяется при температуре 370 С от давления 10 Па до 10-2 Па. Найти работу, совершаемую газом при расширении. 9. Азот, находившийся при температуре 400 К, подвергли адиабатическому расширению, в результате которого его объем увеличился в 5 раз, а внутренняя энергия уменьшилась на 4 кДж. Определить массу азота. 10. Двухатомный газ занимает объем 0,5 л при давлении 50 кПа. Газ сжимается адиабатически до некоторого объема и давления. Затем он охлаждается при постоянном объеме до первоначальной температуры, причем его давление становится равным 100 кПа. Построить график этого процесса. Найти объем и давление. 11. Температура нагревателя идеальной тепловой машины t1=1170 C, а холодильника –t2 =270C. Количество теплоты, получаемое машиной от нагревателя за 1 с, равно Q = 60 кДж. Вычислить кпд машины, количество теплоты, отдаваемое холодильнику за 1 с, и мощность машины.
Вариант 10 1. При какой температуре кислород, находясь под давлением 0,2 МПа, имеет плотность 1,2 кг/м3? Какова при этом концентрация молекул кислорода? 2. Каково давление смеси газов в колбе, если в каждом кубическом сантиметре находится 1020 молекул кислорода и 3∙1020 молекул азота. Температура смеси 1500 С. 3. В сосуде, объем которого 3 л, находится кислород массой 3 г при температуре 130 С. Определить внутреннюю энергию газа и давление газа на стенки сосуда. 4. Определить наиболее вероятную скорость молекул газа, плотность которого при давлении 40 кПа составляет 0,37 кг/м3. 5. Найти удельную теплоемкость при постоянном объеме для газовой смеси, масса киломоля которой равна 22 кг, а отношение удельных теплоемкостей равно 1,395. 6. Среднеквадратичная скорость молекул некоторого газа равна 851 м/с. Давление газа составляет 7,4∙105 Па. Найти плотность газа при этих условиях. 7. В баллоне объемом 10 л находится гелий под давлением 1 МПа и при температуре 300 К. После того как из баллона было взято 10 г гелия, температура понизилась на 290 К. Определить давление гелия, оставшегося в баллоне. 8. Кислород, занимавший объем 3 л при давлении 148 кПа, адиабатически расширяется до объема 89 л. Определить работу расширения. 9. Работа расширения некоторого двухатомного идеального газа составляет 2 кДж. Определить количество подведенной к газу теплоты, если процесс протекает изобарно. 10. Газ, совершающий цикл Карно, получает от нагревателя 42 кДж теплоты. Какую работу совершает газ, если абсолютная температура нагревателя в 3 раза выше, чем температура холодильника? 11. Один моль идеального двухатомного газа, находящийся под давлением в 1 атм при температуре 270 С, нагревается при постоянном объеме до давления в 2 атм. После этого газ изотермически расширяется до начального давления и затем изобарически сжимается до начального объема. Начертить график цикла. Определить температуры газа для характерных точек цикла.
Умение решать задачи приобретается длительными систематическими упражнениями. Для овладения необходимыми навыками, следует после изучения очередного раздела учебника внимательно рассмотреть типовые задачи, а также задачи, предлагаемые для самостоятельного решения.
Приложение 1. Некоторые математические формулы:
2. Десятичные приставки к названиям единиц: Т – тера (1012); д – деци (10-1); н – нано (10-9); Г – гига (109); с – санти (10-2); п – пико (10-12); М – мега (106); м – милли (10-3); ф – фемто (10-15); к – кило (103); мк – микро (10-6); а – атто (10-18).
3. Некоторые внесистемные величины:
4. Основные физические постоянные:
5. Плотность газов r (кг/м3) при нормальных условиях:
6. Эффективный диаметр молекул (нм):
7. Молярные массы (М 10-3 кг/моль) газов:
БИБЛИОГРАФИЧЕСКИЙ СПИСОК
1. Трофимова Т.И. Курс общей физики. М.: Высш.шк., 1990. 478 с. 2. Савельев И.В. Курс общей физики: В 3 т. Т. 1. М.: Наука, 1977. 416 с. 3. Детлаф А.А. Курс физики / А.А. Детлаф, В.М. Яворский. М.: Высш.шк., 1989. 608 с. 4. Волькенштейн В.С. Сборник задач по общему курсу физики. М.: Наука, 1992. 464 с. 5. Трофимова Т.И. Сборник задач по курсу физики. М.: Высш.шк., 1991. 589 с.
ОГЛАВЛЕНИЕ
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-04-08; просмотров: 6565; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.117.11.13 (0.01 с.) |

 RT
RT .
. 0,16·10-13 кг/м3.
0,16·10-13 кг/м3. =32×10-3 кг/моль,
=32×10-3 кг/моль, 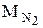 =28×10-3 кг/моль.
=28×10-3 кг/моль. RT. (1)
RT. (1) , (2)
, (2) , (3)
, (3) и
и  – парциальные давления каждого компонента.
– парциальные давления каждого компонента.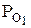 +
+  . (4)
. (4) +m
+m  , имеем:
, имеем: . (6)
. (6) =29×10-3 кг/моль.
=29×10-3 кг/моль. .
. Па.
Па. =20,8·103 Дж/моль×К;
=20,8·103 Дж/моль×К; ,
, =2Т1 = 600 К.
=2Т1 = 600 К.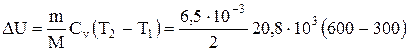 =20,3·103 Дж;
=20,3·103 Дж;
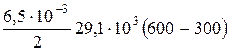 =28,4·103 Дж.
=28,4·103 Дж.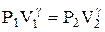 .
. .
.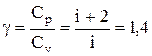 ,
, =105 ·101,4 =106,4 Па.
=105 ·101,4 =106,4 Па. gР2 = 6,4. На основании этого Р2=2,51·106 Па.
gР2 = 6,4. На основании этого Р2=2,51·106 Па. ,
, ,
, .
. ,
,  .
. Р
Р

 Р2 2 р2, V2, T2 3 р3, V3, T3
Р2 2 р2, V2, T2 3 р3, V3, T3

 Р1 1 р1, V1, T1 4 р4, V4, T4
Р1 1 р1, V1, T1 4 р4, V4, T4
 =
=  .
. .
. . Подставив найденные выражения в формулу (1), выполним преобразования:
. Подставив найденные выражения в формулу (1), выполним преобразования: .
. , ее молярная масса 0,018 кг/моль. Коэффициент объемного расширения воды равен 2·10-4 К-1. Атмосферное давление составляет 0,1 МПа.
, ее молярная масса 0,018 кг/моль. Коэффициент объемного расширения воды равен 2·10-4 К-1. Атмосферное давление составляет 0,1 МПа. ;
; ;
; ;
; ;
; ;
; .
.


