Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Классификация и номенклатура ферментовСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
Современные классификация и номенклатура ферментов разработаны Комиссией по ферментам Международного биохимического союза и утверждены на V Международном биохимическом конгрессе в 1961 г. в г. Москве. В основу классификации легли три принципа: 1. Химическая природа фермента. 2. Химическая природа субстрата, на который действует фермент. 3. Тип катализируемой реакции. Существует шесть классов ферментов.
Аэробные дегидрогеназы, или оксидазы, катализируют перенос протонов (электронов) непосредственно на кислород; Анаэробные дегидрогеназы ускоряют перенос протонов (электронов) на промежуточный субстрат, но не на кислород. Наиболее распространены оксидоредуктазы, содержащие в качестве кофактора никотинамидадениндинуклеотид ( НАД+), либо никотинамидадениндинуклеотидфосфат (НАДФ+). Их называют пиридинферментами. Коферментами оксидоредуктаз являются также флавопротеины (ФП) – флавинмононуклеотид ( ФМН) и флавинадениндинуклеотид (ФАД). Подобные ферменты получили название флавиновых дегидрогеназ. 2. Трансферазы - ферменты, катализирующие реакции межмолекулярного переноса различных атомов, групп атомов и радикалов. Фосфотрансферазы катализируютперенос остатка фосфорной кислоты. Донором фосфатных остатков в большинстве случаев является АТФ. Фосфорные эфиры органических соединений обладают повышенной химической активностью. Реакция фосфорилирования глюкозы катализируется гексокиназой или АТФ,D-глюкоза-6-фосфотрансеразой: Протеинкиназы переносят остаток фосфата с АТФ на белки,изменяя их биологическую активность. Аминотрансферазы ускоряют реакцию переноса аминогруппы с аминокислоты на a-кетокислоту: 
аспарагиновая α-кетоглутарат оксалоацетат глутаминовая кислота кислота Гликозилтрансферазы катализируют реакции переноса гликозильных остатков; ацилтрансферазы – реакции переноса ацилов (остатков карбоновых кислот). 3. Гидролазы катализируют расщепление внутримолекулярных связей органических веществ при участии молекулы воды.
Фосфатазы гидролизуют фосфорные эфиры: Г-1-Ф + Н2О Гликозидазы катализируют гидролиз гликозидов. Амилаза расщепляет гликозидные связи в молекулах крахмала. Пептидгидролазы ускоряют гидролиз пептидных связей в белках и пептидах. 4. Лиазы - ферменты, катализирующие разрыв связей С—О, С—С, Декарбоксилазы относятся к углерод-углерод-лиазам:
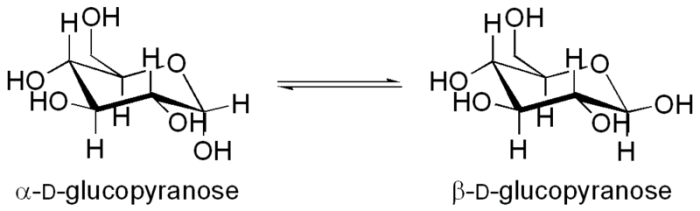
Некоторые лиазы ускоряют реакции не только отщепления, но и присоединения. 5. Изомеразы - ферменты, катализирующие взаимопревращения структурных, оптических и геометрических изомеров. Мутаротаза ускоряет реакцию превращения α-D-глюкопиранозы в
6. Лигазы (синтетазы) - ферменты, катализирующие синтез органических веществ из двух исходных молекул с использованием энергии АТФ либо других веществ: пируваткарбоксилаза СН3-СО-СООН + СО2 + АТФ ----------------------------àНООС-СН2-СО-СООН + АДФ + Рi. пировиноградная оксалоацетат кислота Международная комиссия подготовила Классификацию ферментов (КФ). Код каждого фермента содержит четыре цифры, разделенные точками. Первая цифра указывает номер класса, вторая означает подкласс и характеризует вид субстрата (у трансфераз указывает на природу переносимой группы, у гидролаз - на тип гидролизуемой связи). Третья цифра уточняет природу участвующих в реакции соединений или групп. Четвертая цифра – номер фермента в данном подподклассе. В подподклассе ферменты располагаются по алфавиту. Пример: каталаза – 1.11.1.6. ФЕРМЕНТЫ В МЕДИЦИНЕ Ферменты применяют как лечебные препараты (таблица 2):
- при их отсутствии или недостатке (наследственном или приобретенном); - для специфического разрушения некоторых продуктов обмена.
Таблица 2. Использование ферментов как лечебных препаратов
Ферменты используют в клинике в качестве аналитических реактивов (таблица 3). Для анализа часто применяются иммобилизованные ферменты, которые искусственно связаны с нерастворимым в воде носителем, что облегчает использование и повышает стабильность ферментов. Таблица 3. Использование ферментов как аналитических реагентов
Анализ кинетики появления и исчезновения ферментов в сыворотке крови используется в диагностике. Состав ферментов и их распределение в тканях у взрослого человека в норме в основном постоянны, и могут изменяться при болезнях. Почти все ферменты организма функционируют внутриклеточно. При повреждении тканей внутриклеточные ферменты появляются в сыворотке крови. При воспалительных процессах повышается проницаемость клеточных мембран и в сыворотку крови попадают цитоплазматические ферменты. Некроз ткани сопровождается разрушением всех клеточных структур, и в сыворотке могут быть обнаружены митохондриальные, ядерные и другие ферменты. Такие ферменты называют индикаторными. Появление в плазме или сыворотке крови ряда тканевых ферментов в повышенных количествах характеризует функциональное состояние различных органов и их поражение (таблица 4). Таблица 4. Использование ферментов в диагностике
Энзимопатии (синоним ферментопатии) - общее название болезней, развивающихся вследствие отсутствия или снижения активности тех или иных ферментов. Дефект одного фермента часто приводит к ряду нарушений в обмене веществ вследствие взаимозависимости метаболический процессов в организме. Выделяют наследственные и приобретенные энзимопатии. 1. Наследственные энзимопатии связаны с генетически обусловленной недостаточностью одного или нескольких ферментов. Известно более 150 наследственных ферментопатий, для которых установлена сущность генной мутации. Ферментативный дефект приводит к накоплению в организме продуктов обмена веществ, нарушающих функцию тех или иных органов, что обусловливает появление клинических признаков болезни. К энзимопатиям относятся фенилкетонурия, гликогенозы, хондродистрофия, гемофилия и т.д. Приобретенные энзимопатии. Токсические энзимопатии - следствие токсического воздействия ксенобиотиков и мутагенов внешней среды. Например, свинец, содержащийся в выхлопных газах транспорта, вызывает снижение активности фермента аминолевулинатдегидразы, участвующей в синтезе гема, что проявляется развитием анемии у детей крупных городов.
Алиментарные энзимопатии могут быть обусловлены длительным несбалансированным питанием, дефицитом белка в рационе, витаминной недостаточностью. Контрольные вопросы 1. Охарактеризуйте химическую природу и строение ферментов. 2. Каково строение активного центра фермента? 3. Что такое аллостерический центр? 4. Приведите примеры изоферментов; мультимолекулярных ферментных систем. 5. Опишите механизм действия ферментов. 6. В чем различие теорий Фишера и Кошленда? 7. Каким образом влияют изменение рН и температуры на скорость ферментативных реакций? 8. Что понимают под специфичностью действия ферментов? 9. Что такое константа Михаэлиса? Что она характеризует? 10. Как осуществляется регуляция активности ферментов? 11. В чем отличие обратимого и необратимого ингибирования? 12. Как изменяются Кm и umax при различных типах обратимого ингибирования? 13. Что общего и раздичного в механизмах неконкурентного и бесконкурентного ингибирования ферментов? 14. Приведите примеры использования ингибирования ферментов в медицине. 15. Чем обусловлено существование энзимопатий? 16. По какому признаку классифицируют ферменты? 17. Приведите примеры биохимических реакций, катализируемых ферментами всех шести классов. 18. Какой принцип лежит в использовании ферментов в медицине в диагностических целях? 19. Как на практике можно осуществить определение активности ферментов? 20. Приведите примеры использования ферментов как лекарственных препаратов. ВИТАМИНЫ Витамины (от лат. vita - жизнь) – пищевые незаменимые факторы, которые, присутствуя в небольших количествах в пище, обеспечивают нормальное развитие и жизнедеятельность организма человека и животных, адекватную скорость протекания биохимических и физиологических процессов. Витамины – группа разнообразных по химическим и физическим свойствам органических соединений. Физиологическое действие витаминов также весьма различно. Еще 100 лет назад считали, что для нормальной жизнедеятельности организма человека достаточно поступления белков, жиров, углеводов, минеральных веществ и воды. Оказалось, что существуют особые болезни, развитие которых связано с неполноценным питанием (цинга, бери-бери). Витамины были открыты в 1880 г. нашим соотечественником Н.И. Луниным. На связь витаминов с ферментами впервые в 1922 г. указал академик Н.Д. Зелинский. Во многих случаях витамины являются составными частями ферментов.
В количественном отношении потребность в витаминах ничтожна: человек в среднем должен потреблять ежедневно 0,1-0,2 г витаминов. Авитаминозы – болезни, возникающие при полном отсутствии в пище или полном нарушении усвоения какого-либо витамина. Гиповитаминозы – недостаточное поступление витаминов с пищей или неполное их усвоение. Гипервитаминозы – патологические состояния, связанные с поступлением чрезмерно больших количеств витаминов в организм. Причины гипо- и авитаминозов у человека и животных обычно делят на экзогенные и эндогенные. К экзогенным относится недостаточное поступле витаминов или полное отсутствие их в пище. Эндогенными причинами служат: а) повышенная потребность в витаминах при некоторых физиологических и патологических состояниях (беременность, тиреотоксикоз); б) нарушение процесса всасывания витаминов при заболеваниях пищеварительного тракта; в) усиленный распад витаминов в кишечнике вследствие развития в нем микрофлоры; г) болезни печени, поджелудочной железы, сопровождающиеся нарушением всасывания жиров и, соответственно, жирорастворимых витаминов. Витамины классифицировали по физиологическому действию, оказываемому на организм человека (например, антианемические, антигемморагические, антиинфекционные и т.д.). В настоящее время используется классификация, основанная на растворимости витаминов.
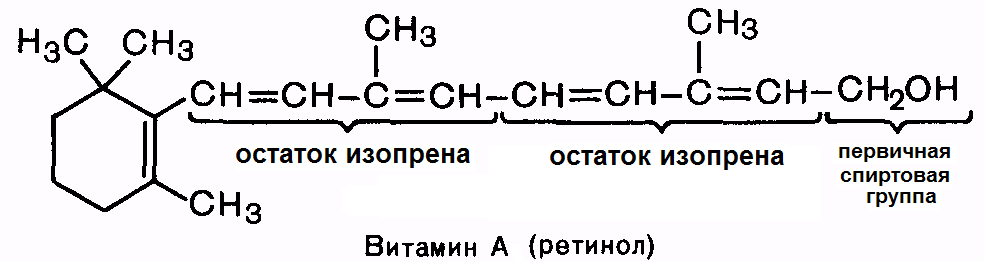
ЖИРОРАСТВОРИМЫЕ ВИТАМИНЫ Витамин А (ретинол).
Витамин А имеет несколько витамеров. Витамеры – вещества, сходные по химическому строению и обладающие физиологическим действием, характерным для того или иного витамина. Окисляясь в организме при участии биокатализатора, ретинол превращается в ретиналь, также обладающий активностью витамина А. Витамин А влияет на барьерную функцию кожи, слизистых, проницаемость клеточных мембран и биосинтез гликопротеинов, участвует в процессе светоощущения, входя в состав светочувствительного пигмента родопсина. Родопсин состоит из липопротеина опсина и простетической группы, представленной ретиналем. На свету родопсин расщепляется на белок опсин и ретиналь; последний превращается в транс-форму. С этими превращениями связана трансформация энергии световых лучей в зрительное возбуждение. Недостаточность витамина А ведет к торможению роста, снижению массы тела, поражению кожи, слизистых оболочек и глаз (ксерофтальмия, «куриная» (ночная) слепота). Витамин А содержится в печени, яичном желтке, молоке, масле; провитамин А (каротин) - в красномякотных овощах. Суточная потребность – 2,7 мг. У человека основным органом, в котором откладывается про запас витамин А, является печень. Описаны случаи гипервитаминоза А при употреблении в пищу печени белого медведя, тюленя, моржа, в которой содержится много свободного витамина А. Гипервитаминоз может развиться и в результате приема больших количеств рыбьего жира и препаратов витамина А. При гипервитаминозе наблюдаются воспаление глаз, выпадение волос, головные боли, диспепсические расстройства (тошнота, рвота).
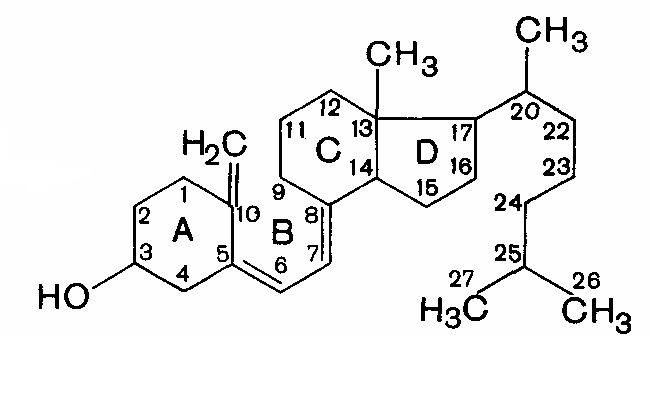
Витамин D (кальциферол) в организме человека существует в виде форм D2 и D3. Предшественник витамина D2 (эргокальциферола) – эргостерин. Предшественник витамина D3 (холекальциферола) – холестерол. Эргостерол и холестерол переходят в активную форму под действием солнечного облучения.
D2 (эргокальциферол) D3 (холекальциферол) Кальциферолы участвуют в регуляции процессов всасывания кальция и фосфора в кишечнике, в остеогенезе, в синтезе мРНК, Са-связывающих белков и гормонов. Недостаток витамина D в детском возрасте приводит к рахиту. Наблюдаются размягчение костей, их искривление; утолщения на костно-хрящевой границе ребер; большая голова, увеличенный живот (гипотония мышц). Авитаминоз D у взрослых ведет к остеопорозу (вымывание солей из костной ткани, в результате чего кости становятся хрупкими). Гипервитаминоз D наблюдается при приеме очень высоких доз витамина и может привести к смертельному исходу. Наблюдается усиление отложения фосфатов в костях и некоторых внутренних органах. Витамин D содержится в продуктах животного происхождения - сливочном масле, печени, желтке яиц и жире. Суточная потребность – 10 мкг, для детей – 20-25 мкг. Для профилактики рахита в детском возрасте рекомендуется УФ-облучение. Витамин Е (токоферол) (от греч. токос – потомство, феро – несу) получил свое название, т.к. было установлено, что он регулирует процесс размножения у крыс.
Витамин Е – один из самых сильных природных антиоксидантов. Он защищает полиненасыщенные жирные кислоты и липиды клеточных мембран от окисления. При отсутствии или недостатке витамина Е у человека и животных нарушается эмбриогенез и наблюдаются дегенеративные изменения репродуктивных органов. Развиваются дегенерация спинного мозга и паралич конечностей, жировая инфильтрация печени, мышечная дистрофия, биохимические изменения в мышцах. Источники витамина Е - растительные масла, салат, капуста и зерновые продукты. Витамин Е откладывается в мышцах, поджелудочной железе, жировой ткани, поэтому развитие авитаминоза почти не наблюдается. Суточная потребность – 5 мг. Витамин K (филлохинон).
Принимает участие в синтезе факторов свертывания крови. При недостатке его могут возникать самопроизвольные носовые кровотечения, кровавая рвота, внутренние кровоизлияния. Авитаминоз K встречается редко – смешанная пища достаточно богата им; кишечная микрофлора способна синтезировать витамин K. Препарат «Викасол» является производным витамина K3. ВОДОРАСТВОРИМЫЕ ВИТАМИНЫ Витамин С (аскорбиновая кислота) -бесцветные кристаллы, кислые на вкус.
Аскорбиновая кислота является участником окислительно-восстановительных процессов; необходима для синтеза коллагена, гормонов коры надпочечников, триптофана, распада гемоглобина в тканях. При недостаточном поступлении витамина С с пищей отмечается снижение массы тела, слабость, одышка, боли в сердце. В тяжелых случаях развивается цинга. Повышается проницаемость и хрупкость кровеносных сосудов, возникают спонтанные кровоизлияния, расшатываются и выпадают зубы. В основе этих явлений лежат нарушения синтеза коллагена. Источником витамина С для человека служат плоды шиповника, черная смородина, облепиха, рябина, красный перец, лимоны, капуста. Суточная потребность – 75 мг. Витамин B1 (тиамин) - первый кристаллический витамин, полученный в лаборатории. Содержит пиримидиновое и тиазоловое кольца, соединенные метиленовой связью:
Активная форма тиамина – тиаминпирофосфат (ТПФ) (тиаминдифосфат). Он является составной частью 5 ферментов, участвующих в промежуточном обмене веществ.
Симптомы авитаминоза В1: нарушение функций пищеварительного тракта, нарушения психики (галлюцинации), дегенеративные изменения нервных окончаний и проводящих пучков, атрофия и паралич конечностей, угнетение сердечно-сосудистой системы. При B1-авитаминозе развивается заболевание, получившее название полиневрита («бери-бери»), которое может привести к параличу и смерти. Источником витамина B1 являются дрожжи, хлеб из муки грубого помола, когда зерно в процессе обработки не теряет зародышей и оболочек. В животных продуктах содержится в печени, почках, мозге. Суточная потребность 1,2 мг. Витамин В2 (рибофлавин). Основу молекулы рибофлавина составляет изоаллоксазин, в котором сочетаются бензольный, пиразиновый и пиримидиновый циклы:
Способность рибофлавина легко окисляться и восстанавливаться лежит в основе его биологического действия. Рибофлавин является коферментом оксидоредуктаз (входит в состав ФАД и ФМН). При В2-авитаминозе наблюдаются остановка роста, выпадение волос, поражение слизистых оболочек (особенно в уголках рта), быстрая утомляемость зрения, понижение работоспособности, нарушение нормального синтеза гемоглобина; мышечная слабость. Источники витамина В2 - молоко и зеленые овощи; много его в печени и почках животных, в пивных и пекарских дрожжах. Суточная потребность – 1,7 мг. Витамин В6 (пиридоксин) является производным 3-оксипиридина. Представлен пиридоксолом, пиридоксалем и пиридоксамином, каждый из них в организме способен перейти в пиридоксальфосфат. Пиридоксальфосфат является простетической группой аминотрансфераз и карбоксилаз, участвует в образовании биогенных аминов, превращениях аминокислот, синтезе гема гемоглобина. Основные симптомы авитаминоза В6 - нарушение кроветворения, развитие различного рода дерматитов, которые не поддаются лечению никотиновой кислотой, атеросклероз. Источники пиридоксина – говядина, рыба, горох, яичный желток и зеленые части растений. Суточная потребность – 2 мг. Так как витамин В6 широко распространен в продуктах питании и может частично синтезироваться микрофлорой кишечника, то в обычных условиях В6-авитаминоз у человека не наблюдается. Витамин B12 (цианкобаламин). Содержит группировку из 4 восстановленных пиррольных колец с атомом Со+ в центре:
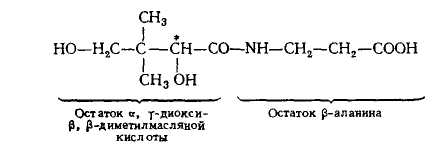
Производные В12 являются коферментами в составе ряда ферментов, ускоряющих важнейшие реакции азотистого, углеводного, нуклеинового и липидного обмена. В12 участвует в реакциях трансметилирования, во внутримолекулярном переносе атомов Н и различных химических групп (гидроксильные, аминогруппы и др.). Недостаток витамина B12 ведет к нарушению нормального кроветворения в костном мозгу, вызывает злокачественную мегабластическую анемию, нарушение деятельности нервной системы, снижение кислотности желудочного сока. Витамин В12 – единственный витамин, синтез которого осуществляется только микроорганизмами. Источники кобаламина: мясо, говяжья печень, рыба, молоко, яйца. Растения не содержат витамина B12. Депо витамина B12 у человека находится в печени, где он накапливается в количестве нескольких миллиграммов. Суточная потребность – 3 мкг. Витамин В5 (пантотеновая кислота) - содержится во всех животных, растительных и микробных объектах (греч. panthos - везде).
Пантотеновая кислота входит в состав коэнзима А. KоА принимает участие в реакциях переноса ацильных групп, с ним связан ряд биохимических реакций, лежащих в основе окисления и синтеза жирных кислот, биосинтеза жиров, окислительных превращений продуктов распада углеводов. При отсутствии витамина В5 возникают дерматиты, замедляется рост, наблюдается потеря веса, выпадение и депигментация волос, дегенеративные изменения в нервной системе. С этим связаны дискоординация движений, парличи, нарушение работы желудочно-кишечного тракта, органов размножения, надпочечников. У человека авитаминоз В5 редок, так как пантотеновая кислота вырабатывается кишечной микрофлорой. Источниками пантотеновой кислоты являются дрожжи, молоко, яйца, печень, почки, горох, цветная капуста, картофель, помидоры. Суточная потребность - 10 мг. Витамин РР (никотинамид и никотиновая кислота, ниацин, В3) - производное пиридина:
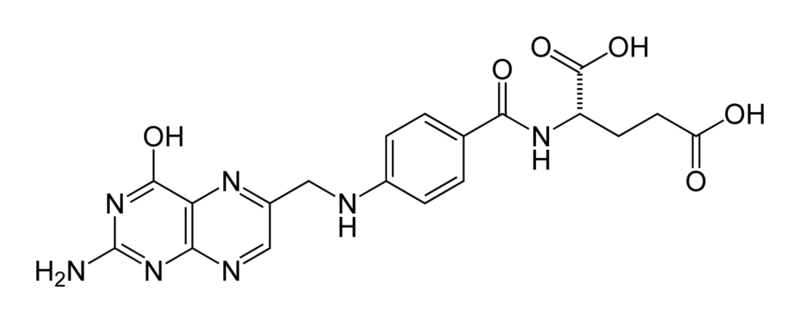
Витамин РР участвует во всех видах обмена веществ: углеводном, белковом и липидном. Никотинамид входит в состав важнейших коферментов дегидрогеназ – НАД+ (никотинамидадениндинуклеотид) и НАДФ+ (никотинамидадениндинуклеотидфосфат), участвующих в окислительно-восстановительных реакциях. Витамин РР имеет решающее значение для выработки энергии. При дефиците витамина РР возникает заболевание пеллагра. Авитаминоз РР выражается в воспалении слизистых оболочек желудочно-кишечного тракта, а затем - в воспалении кожи (дерматитах) на участках тела, подверженных освещению солнцем. Наблюдаются также поражения мозга. Источники витамина РР - гречка, хлеб, картофель, фасоль, печень и почки животных и др. Некоторое количество никотиновой кислоты синтезируется в организме человека из аминокислоты триптофана. Суточная потребность – 18 мг. Фолиевая кислота, витамин Вс (птероилглутаминовая кислота).
Человек редко страдает от Вс-авитаминоза, так как фолиевая кислота синтезируется микрофлорой желудочно-кишечного тракта и всегда поступает в организм в достаточном количестве. При авитамитозе Вс развивается анемия и нарушается деятельность органов пищеварения. Фолиевая кислота, являясь коферментом ряда ферментов, переносит одноуглеродные фрагменты при биосинтезе многих соединений: метильную группу, оксиметильную (-СН2ОН), формильную. Источниками фолиевых кислот являются шпинат, цветная капуста, печень животных, хлеб. Особенно высоко ее содержание в дрожжах. Витамин Р (рутин). В настоящее время известно много соединений, обладающих Р-витаминным действием. Их называют биофлавоноидами.
При отсутствии витамина Р повышается проницаемость капилляров, что сопровождается кровоизлияниями, болью в конечностях, общей слабостью и быстрой утомляемостью. Предполагают, что витамины группы Р участвуют в окислительно-восстановительных реакциях. Источником витамина Р являются те же продукты, в которых много витамина С, например черная смородина и лимоны. Витамин Н (биотин).
При недостатке этого витамина у человека наблюдается воспаление кожных покровов, выпадение волос, усиленное выделение жира сальными железами кожи (себоррея). В качестве кофермента биотин входит в состав ферментов, ускоряющих реакции карбоксилирования. Источником витамина Н являются печень и почки крупного рогатого скота, куриные яйца, молоко, томаты, соя, морковь, картофель, горох. Возможно также поступление биотина в организм за счет микробов-симбионтов. Витаминоподобные вещества. Помимо двух главных групп витаминов, выделяют группу разнообразных химических веществ, из которых часть синтезируется в организме и обладает витаминными свойствами. К ним относят холин, липоевую кислоту, витамин В15, парааминобензойную кислоту, карнитин, линолевую и линоленовую кислоты, витамин U и др. Антивитамины - это соединения, похожие по структуре на витамины, конкурирующие с витаминами в соответствующих биохимических процессах или выключающие витамины из процессов обмена веществ путем их разрушения или связывания. Примером конкурирующих антивитаминовмогут служить структурные аналоги витамина РР. Они способны образовывать псевдо-коферменты, имитирующие НАД+ и блокирующие деятельность НАД+-зависимых оксидоредуктаз. Примером выключающих антивитаминов является авидин - яичный белок, образующий с витамином Н нерастворимый биологически неактивный комплекс. Поскольку бактерии и вирусы, а также клетки опухолей обладают повышенной чувствительностью к отсутствию ряда витаминов, антивитамины используют как терапевтические средства. Методы определения витаминов Для выяснения обеспеченности организма человека каким-либо витамином определяют соответствующий витамин или продукт его обмена в сыворотке крови, моче, биопсийном материале. При взаимодействии витаминов с рядом химических соединений наблюдаются характерные цветные реакции, интенсивность окраски которых пропорциональна концентрации витаминов в исследуемом растворе. Поэтому витамины можно определить фотоколориметрически, например витамин В1. Некоторые витамины обладают способностью поглощать оптическое излучение только определенной части спектра. В частности, витамин А имеет специфичную полосу поглощения при 328-330 нм. Измеряя коэффициент поглощения спектрофотометрически, можно точно определить количественное содержание витаминов в исследуемом объекте. Для определения витамина В2 применяют флюорометрические методы. Используют титриметрические методы (определение аскорбиновой кислоты). Контрольные вопросы 1. Приведите известные Вам классификации витаминов. 2. Охарактеризуйте биологическую роль витаминов. 3. Дайте определение авитаминозам, гиповитаминозам, гипервитаминозам. 4. Каковы причины авитаминозных и гиповитаминозных состояний организма человека? 5. Перечислите жирорастворимые витамины. Какие из них обладают антиоксидантными свойствами? 6. Какие активные формы соответствуют витаминам В1, В2, В3, В5, В6? 7. Какие витамины входят в состав оксидоредуктаз? Какими свойствами обусловлена эта функция? 8. Какие витамины можно использовать в терапии дерматитов? 9. Дефицит каких витаминов приводит к развитию анемии? 10. Синтез какого витамина осуществляется только микроорганизмами? 11. Какой витамин участвует в регуляции фосфорно-кальциевого обмена? Каковы симптомы дефицита данного витамина? 12. Какие водорастворимые витамины обладают антиоксидантными свойствами? 13. Производные каких витаминов являются коферментами, переносящими одноуглеродные фрагменты? 14. Дефицит какого витамина приводит к появлению себорреи? Каковы биохимические функции этого витамина? 15. Биохимическими функциями каких витаминов является перенос аминогрупп? 16. Приведите примеры и симптомы гипервитаминозов. 17. Какие вещества относят к витаминоподобным? Приведите примеры, дайте краткую харатеристику биохимическим функциям. 18. Какие вещества называют антивитаминами? Каков механизм их действия? 19. Объясните, почему сульфаниламидные препараты вызывают гибель бактерий и могут использоваться в качестве лекарств. 20. Какие методы можно использовать для диагностики авитаминозов и гиповитаминозов?
|
||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-07-14; просмотров: 471; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.116.67.43 (0.02 с.) |

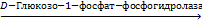 Г + Н3РО4
Г + Н3РО4