Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Физико-химические свойства белковСодержание книги
Поиск на нашем сайте
Белки относятся к высокомолекулярным соединениям. Относительная молекулярная масса белков - от 5000 до миллионов а.е.м. Для определения молекулярной массы белков применяют седиментационный анализ, гель-электрофорез, гель-хроматографию. Молекулярную массу вычисляют по скорости седиментации; последнюю выражают через константу седиментации S (сведберг). Характерные физико-химические свойства белков: - оптическая активность; - способность к поглощению УФ-лучей при 280 нм (имеет важное значение для количественного определения белков); - высокая вязкость растворов; - способность к набуханию; - низкое осмотическое и высокое онкотическое давление; - подвижность в электрическом поле; - незначительная диффузия; - белки не проникают через полупроницаемые мембраны (как биомембраны, так и мембраны искусственного происхождения). Белки – полиэлектролиты, т.к. имеют фунциональные группы, способные к электролитической диссоциации. Иизоэлектрическая точка (рI) – рН раствора, при котором суммарный заряд молекулы белка, обладающего амфотерными свойствами, равен нулю. Молекула белка неподвижна в электрическом поле. В изоэлектрической точке белки обладают наименьшей растворимостью и легко осаждаются. Для большинства белков тканей животных и человека рI = 5,5-7,0. Изоионный раствор белка - раствор, который не содержит никаких других ионов, кроме ионизированных остатков аминокислот белковой молекулы и ионов, образующихся при диссоциации воды. Значение рН изоионного раствора белка называют его изоионной точкой. Изоионная и изоэлектрическая точка белка совпадают только в том случае, когда обе равны 7.
КЛАССИФИКАЦИЯ БЕЛКОВ Согласно функциональному принципу различают 12 главных классов белков: 1) каталитически активные (ферменты); 2) гормоны; 3) регуляторы активности генома; 4) защитные (антитела, белки свертывающей и противосвертывающей систем крови); 5) ингибиторы ферментов; 6) транспортные; 7) мембранные; 8) сократительные; 9) рецепторные; 10) токсические; 11) белки вирусной оболочки; 12) белки с прочими функциями. Различают a-, β-, a+β- и a/β-белки: - a-белки содержат a-спирали (более 60%); - β-белки имеют β-структуру (не менее двух антипараллельных цепей); - a+β–белки включают те и другие структуры в одной полипептидной цепи; - a/β-белки состоят из a- и β-структур, которые чередуются вдоль домена или полипептидной цепи. По химическому составу белки делят на 2 группы. Простые белки состоят только из остатков аминокислот. При гидролизе образуют только свободные аминокислоты. Сложные белки двухкомпонентны: состоят из простого белка и небелковой части (простетической группы). ПРОСТЫЕ БЕЛКИ Альбумины и глобулины. Альбумины – белки, широко представленные в составе тканей животных и растений. Содержатся в сыворотке крови, белке яиц, молоке, в семенах растений. Хорошо растворимы в воде, солевых растворах, кислотах и щелочах. На альбумины приходится около 75-80% осмотического давления белков сыворотки крови. Функцией альбуминов крови является также транспорт жирных кислот. Глобулины - группа животных и растительных белков, широко распространённых в природе. Относятся к глобулярным белкам. Растворимы в слабых растворах нейтральных солей, разбавленных кислотах и щелочах. a-Фракция глобулинов содержится в крови в комплексе с билирубином и с липопротеинами высокой плотности. Представителем фракции β-глобулинов является протромбин -предшественник тромбина, участвующего в свертывании крови. Фракция g-глобулинов наиболее гетерогенная. Важнейшие g-глобулины - иммуноглобулины. Содержание альбуминов и глобулинов в плазме крови человека около 7%. Белковй коэффициент - отношение альбумин/глобулин - имеет диагностическое значение. В норме он близко к 2, а при ряде заболеваний может изменяться, например, уменьшается при воспалительных заболеваниях. Протамины и гистоны. Протамины – низкомолекулярные белки, содержащие 60-85% аргинина и обладающие основными свойствами. Хорошо растворяются в воде, кислой и нейтральной среде и осаждаются в щелочных средах. Обнаружены в ядрах сперматозоидов у рыб и птиц. В ядрах клеток находятся в комплексе с ДНК. Гистоны - белки основного характера с небольшой молекулярной масой. В их состав входят лизин и аргинин, содержание которых не превышает Проламины и глютелины. Проламины - белки растительного происхождения. Содержат 20-25% глутаминовой кислоты и 10-15% пролина. Растворимы в 60-80% водном растворе этанола (тогда как все прочие простые белки в этих условиях обычно осаждаются). Глютелины - простые белки, содержатся в зеленых частях растений, в семенах злаков. Характеризуются высоким содержанием глутаминовой кислоты и наличием лизина. Растворимы в разбавленных растворах щелочей. Глютелины являются запасными белками.
СЛОЖНЫЕ БЕЛКИ 1. Хромопротеины (от греч. chroma - краска) сложные белки, состоящие из простого белка и связанного с ним небелкового окрашенного компонента. Различают гемопротеины и флавопротеины. Хромопротеины участвуют в процессе дыхания, окислительно-восстановительных реакциях, транспорте кислорода и диоксида углерода, свето- и цветовосприятии и др. К группе гемопротеинов относятся гемоглобин, цитохромы, миоглобин, каталаза, пероксидаза. Все гемопротеины содержат железопорфирины, но различаютсяе по составу и структуре белковой части, и выполняют различные биологические функции. Так, различия гемоглобина различных биологических видов обусловлены различиами в структуре глобина. Рассмотрим строение гемоглобина – белка крови. Небелковым компонентом гемоглобина является гем - пигмент, придающий крови красный цвет. Основу его структуры составляет протопорфирин IX (рис. 6). В центре гема расположен ион железа в степени окисления +2, связанный с двумя атомами азота ковалентными связами и с двумя другими атомами азота - координационными связями. Вокруг гемма «обернута» полипептидная цепь. Железо в гемоглобине соединяется с атомом азота имидазольной группы гистидина молекулы белка пятой координационной связью. Шестая координационная связь железа используется для присоединения кислорода или других лигандов (рис. 7).
Гемоглобин взрослого человека НbА (от англ. аdult - взрослый) имеет четыре полипептидные цепи, составляющие глобин (рис. 8) - белковую часть молекулы. Две α-цепи содержат по 141 аминокислотному остатку, две β-цепи - по 146.
В крови взрослого человека присутствуют также гемоглобин НbА2 (2α-, 2δ-цепи, 2,5%) и НbA3 (менее 1%, отличается строением b-цепи). Фетальный гемоглобин (гемоглобин плода и новорожденных) HbF состоит из 2α- и 2γ-цепей. Гемоглобин F обладает повышенным сродством к кислороду и позволяет сравнительно малому объему крови плода выполнять функцию снабжения кислородом более эффективно. Кровь новорожденного содержит до 80% HbF, к концу 1-го года жизни фетальный гемоглобин почти полностью заменяется на НbА. Гемоглобинозы – болезни гемоглобинов. 1. Гемоглобинопатии. В их основе лежит наследственное изменение структуры какой-либо цепи нормального гемоглобина. В крови человека открыто около 150 различных типов аномальных гемоглобинов. Ониразличаются по физико-химическим свойствам (растворимость, электрофоретическая подвижность, изоэлектрическая точка, способность связывать кислород). Пример гемоглобинопатии - серповидно-клеточная анемия. Заболевание распространено в странах Южной Африки, Южной Америки и Юго-Восточной Азии. Химический дефект - замена глутаминовой кислоты в 6-м положении с N-конца на валин в β-цепях молекулы гемоглобина, что является результатом мутации в молекуле ДНК. У HbS снижены растворимость и сродство к кислороду. Эритроциты в условиях низкого парциального давления кислорода пимеют форму серпа. Отдавая кислорода в тканях, HbS превращается в плохо растворимую дезоксиформу и выпадает в осадок в виде тактоидов (веретенообразных кристаллов). Тактоиды деформируют клетку и приводят к гемолизу. Гетерозиготная форма заболевания протекает бессимптомно либо сопровождается легкой гемолитической анемией. У гомозиготных особей тяжелая форма серповидноклеточной анемии развивается с первых месяцев жизни. Болезнь протекает остро, и дети часто умирают в раннем возрасте. Примерами аномальных гемоглобинов являются также гемоглобин С (в b-цепи на 6 месте вместо глутаминовой кислоты находится лизин) и гемоглобин D (в b-цепи на 28 месте вместо глутаминовой кислоты находится лейцин). Данные мутации обнаружены в основном в Африке. 2. Талассемии - группа заболеваний с наследственным нарушением синтеза одной из цепей глобина. Различают α-талассемии, когда не происходит синтез α-цепи, и β-талассемии (не синтезируются β-цепи). Гемоглобинопатия Н (один из вариантов a-талассемии) характеризуется гемолитической анемией, выпадением в осадок гемоглобина Н, спленомегалией, тяжелыми изменениями костей. 3. Железодефицитные анемии – заболевания, возникающие при нарушение синтеза гемоглобина вследствие дефицита железа. Основными причинами железодефицитных анемий являются кровопотери, а также недостаток богатой железом пищи - мяса и рыбы. Производные гемоглобина Оксигемоглобин HbO2. Молекулярный кислород присоединяется к каждому гему Hb при помощи координационных связей железа. Присоединение каждой молекулы кислорода облегчает присоединение последующей. Эта аллостерическая зависимость получила название эффекта Бора. Оксигемоглобин, попадая в ткани, теряет кислород, превращаясь в дезоксигемоглобин. Карбгемоглобин HbCO2 - соединение гемоглобина с углекислым газом. Он нестоек и быстро диссоциирует в легочных капиллярах с отщеплением СО2. Карбоксигемоглобин HbCO - продукт присоединения оксида углерода CO (угарного газа) к гемоглобину. Гемоглобин имеет высокое сродство к СО и прочно с ним связывается, теряя способность к транспорту кислорода, что приводит к смерти от удушья. Метгемоглобин MtHb -форма гемоглобина, в которой железо гема находится в трехвалентном состоянии.Не способен переносить кислород. Образуется из свободного гемоглобина под действием различных окислителей, а в организме - при отравлениях нитробензолом, оксидами азота. Метгемоглобинемия - появление в крови метгемоглобина. Выделяют наследственные и приобретенные метгемоглобинемии. Наследственные развиваются в результате наличия нестабильных или аномальных гемоглобинов. Приобретенные метгемоглобинемии могут быть экзогенного токсического происхождения, возникающие при воздействии ряда химических веществ окружающей среды, и эндогенного происхождения, развивающиеся вследствие нарушения образования и всасывания нитратов при энтероколитах. При значительной метгемоглобинемии развивается кислородное голодание (гипоксия). Качественное определение производных гемоглобина проводится путем исследования их спектров поглощения. Миоглобин - глобулярный белок, функцией которого является запасание молекулярного кислорода в мышцах и передача его системам оксиления клеток. Состоит из одной полипептидной цепи. Активным центром, связывающим O2, как и в гемоглобине, является гем. Миоглобин определяет цвет мышц. К хромопротеинам относятся также ферменты каталаза и пероксидаза, входящие в антиоксидантную систему организма, и цитохромы, участвующие в окислительно-восстановительных реакциях и служащие переносчиками электронов. Флавопротеины – хромопротеины, простетические группы которых представлены производными витамина В2 - флавинмононуклеотидом (ФМН) и флавинадениндинуклеотидом (ФАД). Флавопротеины являются кофакторами оксидоредуктаз. 2. Липопротеины состоят из белка и простетической группы, представленной липидом (фосфолипиды, нейтральные жиры, производные холестерина, жирные кислоты). В образовании липопротеинов участвуют нековалентные связи различной природы, например, гидрофобные или ионные (если в состав входит фосфолипид). Липопротеины широко распространены и выполняют разнообразные биологические функции (белок ткани легких, липовителлин желтка куриного яйца и т.д.). Липопротеины существуют в свободном состоянии в плазме крови. Липопротеины сыворотки крови содержат гидрофобное липидное ядро, окруженное полярными липидами и оболочкой из белков, получивших название апобелки. Их функция - транспорт липидов, нерастворимых в воде. Липиды, ковалентно связанные с белком, выполняют функцию прикрепления белков к мембране клетки. Это структурированные липопротеины (липиды мембран клетки, миелиновой оболочки нервных волокон). 3. Фосфопротеины - сложные белки, в состав которых в качестве небелкового компонента входит фосфорная кислота, присоединенная к полипептидной цепи сложноэфирной связью через остатки серина или треонина. Возможен также ионный тип связи.
Представителями фосфопротеинов являются казеиноген молока, овальбумин белка куриного яйца, ряд ферментов (РНК-полимеразы). Фосфопротеины широко представлены в клетках ЦНС. Фосфопротеины являются ценным источником энергетического и пластического материала в процессе эмбриогенеза и постнатального роста и развития организма, участвуют в регуляции активности ядра клетки, в окислительных процессах в митохондриях, в транспорте ионов. 4. Гликопротеины -сложные белки, содержащие, помимо полипептидной цепи, линейные или разветвленные гетероолигосахаридные цепи из 2 - 15 остатков гексоз либо пентоз и конечный углевод
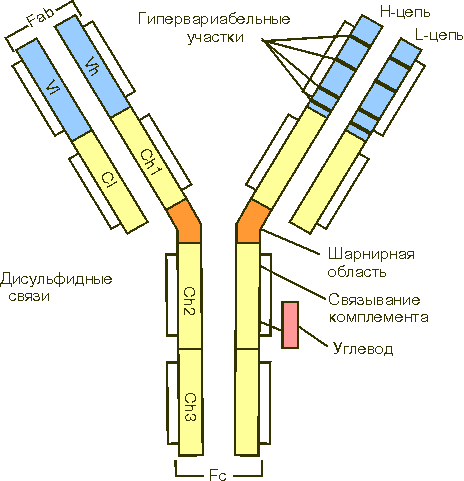
Представителями гликопротеинов являются белки плазмы крови (кроме альбуминов), муцин слюны, некоторые ферменты, белки хрящевой и костной тканей. Гликопротеины являются важным структурным компонентом клеточных мембран. Они обеспечивают клеточную адгезию, молекулярное и клеточное узнавание. Углеводные компоненты не только выполняют информативную функцию. Они повышают стабильность молекул гликопротеинов к различным химическим и физическим воздействиям, а также защищают их от действия протеиназ. Гликопротеины мембран эритроцитов определяют группу крови у человека. Типичными представителями гликопротеинов являются интерфероны, иммуноглобулины. Интерфероны – белки-ингибиторы размножения многих типов вирусов. Они образуются в клетке в ответ на внедрение вирусной нуклеиновой кислоты. Интерфероны являются также защитными белками при опухолевых поражениях. Иммуноглобулины, или антитела, выполняют защитную функцию, обезвреживая поступающие в организм чужеродные вещества – антигены - любой химической природы. Выделяют три основных класса иммуноглобулинов: IgG, IgA, IgM; минорные классы иммуноглобулинов плазмы человека обозначаются как IgD и IgE. Иммуноглобулины разных классов отличаются по молекулярной массе, по концентрации в крови, по биологическим свойствам. Структура иммуноглобулина G приведена на рис. 9. Он состоит из двух идентичных легких L-цепей (от англ. light) и двух идентичных тяжелых
Рис. 9. Структура иммуноглобулина Ряд заболеваний (например, ревматоидные артриты) сопровождается синтезом аномальных антител с аномально короткими суглеводными цепями, что вызывает стимуляцию иммунной системы против самого организма. Протеогликаны - комплексы белка и гликозаминогликанов. Углевод в этих соединениях составляет основную часть молекулы (до 95%). Типичными представителями гликозаминогликанов являются гиалуроновая кислота (ее основная функция - связывание воды в соединительной ткани) и гепарин, участвующий в регуляции свертывания крови. 5. Металлопротеины – белки, помимо полипептидной цепи содержащие ионы одного или нескольких металлов. Белки, содержащие негемовое железо: - ферритин (около 20% железа) сосредоточен главным образом в селезенке, печени, костном мозге. Выполняет роль депо железа в организме; - трансферрин сыворотки крови (около 0,13% железа) транспортирует ионы железа в ретикулоциты, в которых осуществляется биосинтез гемоглобина. Металлоферменты - белки, обладающие ферментативной активностью и содержащие катионы металлов. Алкогольдегидрогеназа содержит ионы Zn, АТФ-аза - ионы Na, K, Са, Мg, цитохромоксидаза – Cu, протеиназы - Mg, K. 6. Нуклеопротеины (НП) – сложные белки, небелковым компонентом которых являются нуклеиновые кислоты. Нуклеиновые кислоты (НК) - ДНК и РНК–полимеры нуклеотидов. ДНК находится в основном в ядре клетки, а также в митохондриях. РНК присутствует во всех частях клетки. Различают мРНК (определяет порядок аминокислот в молекуле белка), рРНК (входит в состав рибосом), тРНК (транспортирует аминокислоты к месту синтеза белка), мяРНК (выполняет каталитические функции). НК обеспечивают хранение и передачу наследственной информации путем программирования синтеза клеточных белков. В состав нуклеиновых кислот входят азотистые основания (ДНК - аденин, гуанин, цитозин, тимин, РНК - аденин, гуанин, цитозин, урацил), углеводы (дезоксирибоза и рибоза соответственно), остатки фосфорной кислоты. Нуклеотиды (рис. 10) состоят из пиримидинового или пуринового основания, пентозы (рибозы) и фосфорной кислоты. Нуклеотиды – нуклеозидфосфаты.
ДНК, выделенная из различных тканей одного и того же вида, имеет одинаковый состав азотистых оснований. Закономерности состава и количественного содержания азотистых оснований были впервые установлены Э. Чаргаффом Правила Чаргаффа: 1. Молярная доля пуриновых оснований равна молярной доле пиримидиновых оснований: А + Г = Ц + Т. 2. Количество аденина и цитозина равно количеству гуанина и тимина: А + Ц = Г + Т. 3. Количество аденина равно количеству тимина, количество гуанина равно количеству цитозина: А = Т, Г = Ц. 4. Коэффициент специфичности равен (Г + Ц)/(А + Т) (у животных
|
|||||||||||
|
Последнее изменение этой страницы: 2016-07-14; просмотров: 373; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.21.105.46 (0.012 с.) |



 Рис. 8. Гемоглобин
Рис. 8. Гемоглобин