Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Механизмы повреждения клеточных структурСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
Липидный механизм
Свободные радикалы – это атомы (или молекулы) с неспаренными электронами на внешних атомных или молекулярных орбитах, отличающиеся высокой реакционной способностью. Два электрона одной орбитали (спаренные) имеют противоположные спины (направление вращения электрона вокруг собственной оси, которое создает магнитное поле с параллельным, или антипараллельным вектором относительно магнитного поля Земли), а отсюда и нулевой общий магнитный момент. Неспаренный электрон придает атому (или содержащей его молекуле) магнитный момент, который предопределяет его химическую реакционную способность. Неспаренные электроны стремятся ликвидировать феномен неспаренности двумя путями. · Взаимодействием с другими свободнорадикальными атомами (или молекулами) с образованием химически инертного продукта; · «Выдергиванием» неспаренного электрона с противоположным спином из внешней оболочки свободных или связанных атомов. Объектом такого воздействия являются переходные металлы, богатые неспаренными электронами, в результате взаимодействия радикал становится химически инертным (тушится), а металл изменяет заряд. Но свободные радикалы способны «выдергивать» электроны и из биоорганических соединений, которые превращаются в свободнорадикальные (перикисные) соединения с патологическим нарушением биохимических процессов.
Свободные радикалы постоянно образуются в организме и попадают в него из окружающей среды (все виды излучения). Свободные радикалы не бывают «хорошими» или «плохими». Они необходимы организму для выполнения ряда функции, например в дыхательной цепочке, но оказывают повреждающее действие при увеличении их количества. В процессе биологического окисления образуются супероксидный радикал О2Ÿ и гидроксидный радикал ŸОН (свободные радикалы), о ксид азота NОŸ (преимущественно участвует в регуляции сосудистого тонуса) и перекись водорода Н2О2 (последняя не является свободным радикалом, но в результате менталлокатализа превращается в гидроксильный радикал). Н2О2 легко разрушается каталазой. супероксидный радикал О2Ÿ генерируется лейкоцитами при фагоцитозе, образуется в митохондриях в процессе окислительных реакций, в тканях при метаболической трансформации катехоламинов, синтезе простогландинов. Некоторые реакции сопровождаются образованием гидроксильного радикала ŸОН и пероксида водорода Н2О2 (необходимых киллерам и фагоцитам). Кислородные радикалы обеспечивают свободнорадикальное окисление субстратов, основными из которых являются полиненасыщенные жирные кислоты клеточных мембран. Это влияет на полярность гидрофобных углеводородных хвостов жирных кислот, которые образуют липидный бислой мембраны. В результате изменяется структура мембраны, ее проницаемость и ионный транспорт. В физиологических условиях это один из способов регуляции функции клетки. Оксид азота NO· легко проходит через мембранные структуры и в качестве посредника обуславливает расслабление гладких мышц стенки сосудов, ЖКТ, бронхов и других полых органов, выполняет роль нейротрансмиттера, а также антигрегантную и адгезивную функцию. Особое внимание заслуживает противомикробное и противопаразитарное действие NO·. Именно этим объясняется генерация больших количеств оксида азота клетками эпителия бронхов, а также иммунной системы (лейкоциты, макрофаги). Чужеродные липополисахариды в указанных клетках часто одновременно активируют и мембранную НАДФН-оксидазу, генерирующую супероксид O2·¾, который нейтрализует NO· с образованием пероксинитрита (ONOO-). При физиологическом рН превращается в слабую пероксинитрокислоту. Цитотоксическое действие пероксинитрита объясняется возможностью его распада на NO2- и OH·. Гидроксильный радикал способен запускать окисление липидов, белков и нуклеиновых кислот.
Физиологическое значение свободных радикалов заключается в регуляции генетической программы и апоптоза, образовании катехоламинов, стероидных гормонов и др., детоксикации ксенобиотиков, медиаторов и гормонов, разрушении фагоцитированных структур в фагоцитах. ПОЛ – физиологический процесс регуляции клеточной активности, однако при избытке свободных радикалов приводит к гибели клетки. Патологический эффект в организме возникает при избыточной продукции свободных радикалов, или при дефиците антиоксидантных факторов. При избытке образования свободных радикалов структуры клетки разрушаются, и она гибнет. Антиоксидантная система подразделяется на неэнзимную и энзимную. a) Неэнзимные антиоксиданты являются донорами электронов для радикальных молекул, превращают их в инертные молекулы, но являются «двуликими» и сами становятся свободнорадикальными. Выполняют лишь буферную роль в антиоксидантной защите организма. · водорастворимые соединения (аскорбиновая кислота, мочевая кислота, глютатион); · жирорастворимые соединения (a-токоферол, ретинол). · спирты и тиолы (цистеин, дитиотретиол, маннитол, тиомочевина, этанол и др.) b) Ферментные антиоксиданты способны выступать в качестве доноров или акцепторов свободных электронов, являются основной защитой организма от оксидативного стресса. · супероксиддисмутаза нейтрализует свободнорадикальный кислород с образованием перекиси водорода и атомарного кислорода; · каталаза разлагает перекись водорода; · глутатионпероксидаза в цитозоле клеток разлагает перекись водорода. c) Липидные антиоксидантные «ловушки» (перехват свободных радикалов) – это холестерол клеточных мембран, гидрофильные головки фосфолипидов клеточных мембран.
Кальциевые механизмы Существует 2 вида Ca++ насосов: Са++ АТФаза и Na+/Ca++ АТФаза. Если Са++ появляется в цитоплазме, то начинается активация ферментов. В зависимости от происхождения клетки, Са++ может активировать разные функции: в мышечных – сокращение, в нервных – возбуждение, в тучных клетках – выброс гистамина и т. д. Накопление Са++ в цитоплазме мышечной клетки приводит к активации ферментов: кальмодулина (сокращение мышечного волокна), протеинкиназ (синтез белка и, следовательно гипертрофия мышц). Но, если Са++ чуть больше, начинается активация фосфолипаз (расщепление фосфолипидов мембран, причем мембран как клеточной, происходит аутолиз клетки, так и мембран органелл, например, лизосом, лизосомальный аутолиз клетки, повреждение мембран митохондрий с последующим выходом из них Са++ (митохондрии – аккумулируют Са++). Активации лизосомальных ферментов способствует изменение pH в кислую сторону (аналогично перевариванию в ЖКТ). 5. – Апоптоз. Отличия апоптоза и некроза. Биологическое и патологическое значение апоптоза.
Апоптоз – запрограммированная, активная (энергозатратная) форма гибели клеток, проявляющаяся уменьшением ее размеров, конденсацией и фрагментацией хроматина, уплотнением мембраны без выхода содержимого в окружающую среду. Считается, что термин апоптоз предложил древнеримский врач Гален. В процессе наблюдения за природой он заметил, что если надломить ветку дерева, с которой уже начали опадать листья, то листопад прекращается, а листья, хотя и меняют цвет, остаются на ветке. То есть опадание листьев, в отличие от их омертвения на сломанной ветке, - физиологический процесс, преднамеренное самоубийство листьев. Сегодня термин апоптоз, буквально означающий «опадание листьев», применяется к физиологическому явлению - самоубийству клеток, т.е. генетически запрограммированной гибели клеток. Другими словами существует особая генетическая программа, реализация которой при определенных условиях приводит клетку к гибели. В современную науку использование термина апоптоз введено Керром (J.F.R. Kerr) в 1972 году. Апоптозом управляют особые гены: стимулирует апоптоз ген р53 (ему принадлежит важнейшая роль в противоопухолевой защите), ингибирует апоптоз – ген bcl2 (относится к протоонкогенам из-за его способности предотвращать апоптоз и сохранять клетки с мутациями). Апоптоз противопоставляется другой распространенной форме гибели клеток – некрозу.
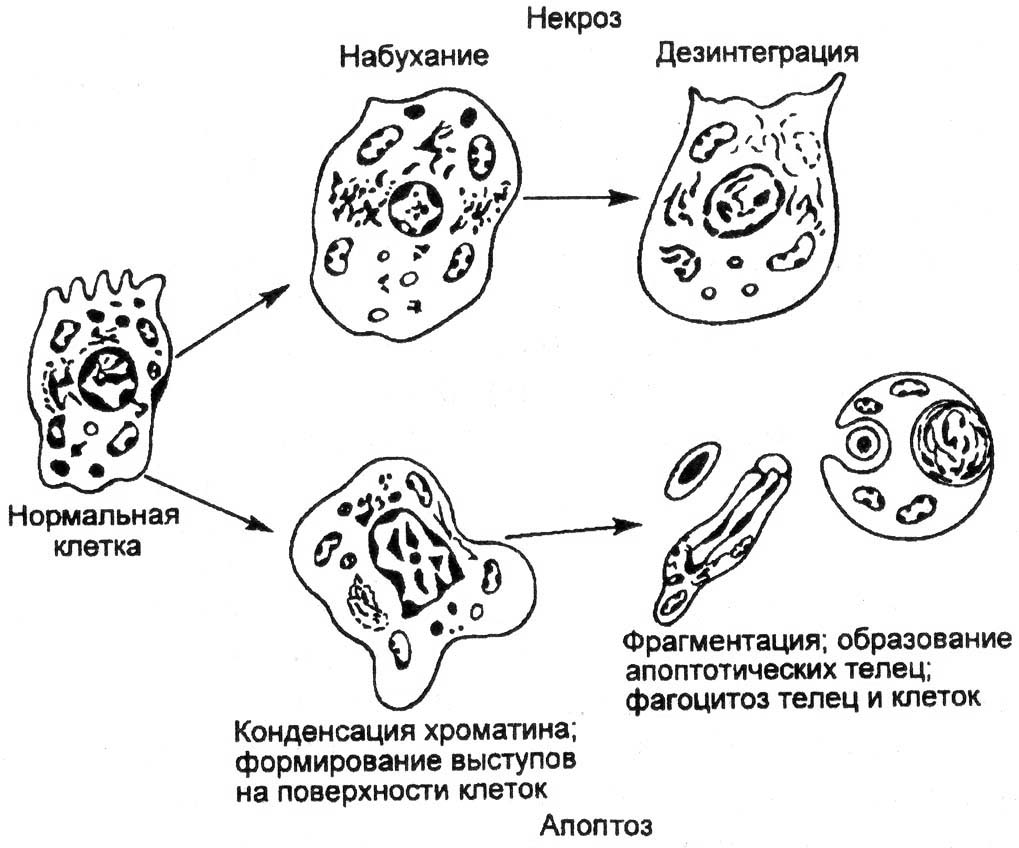
Рис. 2.2. Сравнительное изображение развития некроза и апоптоза клеток.
Апоптоз проявляется уменьшением объема клетки в противоположность ее набуханию при некрозе; конденсацией и фрагментацией хроматина; снижением трансмембранного потенциала митохондрий; уплотнением цитоплазматической мембраны без выхода содержимого в окружающую среду. В результате фагоцитоза, которому клетки подвергаются уже в процессе апоптоза, их содержимое не выделяется в окружающую среду, как это бывает при некрозе, когда вокруг гибнущих клеток скапливаются активные внутриклеточные компоненты, включая энзимы, закисляется среда, что способствует гибели других клеток и развитию очага воспаления. Апоптоз поражает индивидуальные клетки и практически не отражается на их окружении. Стадии апоптоза: I. Индукторная. Сигналами к развитию апоптоза (индукторами апоптоза) являются внеклеточные (антигены, гормоны (например, кортикостероиды), цитокины, УФ- и g-излучение, нагревание) и внутриклеточные (повреждение хромосом и дефицит сигналов) факторы. К универсальным индукторам относятся также нарушение осмотического равновесия, высокое содержание Ca++ и NO. Индукторы апоптоза в свою очередь запускают ферменты (каспазы), которые регулируют весь процесс апоптоза. Эта стадия подразумевает прохождение неких контрольных точек, в которых клетке предоставляется выбор между индукцией и блокадой апоптоза, т. е. данная стадия еще является обратимой. После их прохождения клетка вступает в следующую необратимую фазу апоптоза. II. Эффекторная – в клетке происходит снижение трансмембранного потенциала митохондрий, развивается массовый протеолиз и расщепление ядерной ДНК с формированием крупных фрагментов (олигонуклеосом и нуклеосом. Такая фрагментация считается биохимическим маркером апоптоза, а на ее выявлении основаны современные методы диагностики апоптоза. III. Деградация клетки. Роль апоптоза: · Поддержание постоянства численности клеток (своего рода контроль перенаселения. · Определение формы организма и его частей (например, наблюдается интенсивный апоптоз нервных клеток в процессе формирования коры у зародыша на 12-23-й неделях беременности). · Обеспечение правильного соотношения численности клеток различных типов (быстрая атрофия гормон-зависимых тканей при снижении концентрации соответствующих гормонов, например, в женских половых органах в течение менструального цикла, или в простате при снижении концентрации андрогенов). · Удаление генетически дефектных клеток. · Селекция лимфоцитов и регуляция иммунных процессов.
Рис. 2.3. Схема клеточного цикла.
Ингибиторы апоптоза:
Воздействие радиации вызывает (через свободно-радикальное повреждение) мутации и изменение в структуре ДНК. В результате – клетка остается в G1-фазе митоза (если она входит в S - фазу, то происходит апоптоз). Мутационная форма белка Р53 не обладает способностью останавливать клеточный цикл, это явление наблюдается у опухолевых клеток Теломераза – фермент, обеспечивающий восстановление длины теломерного (концевого) участка хромосомной ДНК. Каждое деление делает хромосому короче на 10-20 теломерных фрагментов. Что дает возможность произвести только 50 делении (лимит Хайфлика). У человека теломераза функционирует только в эмбриональных клетках и семенниках, вырабатывающих сперматозоиды в течение всей жизни. В опухолевых клетках теломераза активна. Патология, обусловленная нарушением апоптоза: a) Ослабление апоптоза · аутоиммунные процессы (семейный аутоиммунный лимфопролиферативный синдром, системная красная волчанка, ревматоидный артрит); · злокачественные опухоли (лимфома Беркитта, лейкозы, солидные опухоли). b) Ускорение апоптоза · врожденные уродства (волчья пасть, заячья губа и др.); · болезни крови (миелодисплазии, анемии (железо- фолио- В12 – дефицитные), тромбоцитопения, нейтропения). · инфекционные заболевания (СПИД, бактериальный сепсис и др.); · дистрофические заболевания нервной системы (боковой амиотрофический склероз, болезнь Альцгеймера, спинальная мышечная атрофия); · другие заболевания (инфаркт миокарда, токсические гепатиты). 6. – Реактивность и резистентность. Виды. Взаимосвязь резистентности и реактивности. Методы измерения реактивности и резистентности.
Реактивность - свойство организма как целого отвечать изменениями жизнедеятельности на воздействие окружающей среды. Реактивность - один из важнейших факторов патогенеза болезней.
Течение болезни может быть: · Гиперэргическое (гиперэргия) - быстрое, яркое, выраженное. · Гипоэргическое (гипоэргия) - затяжное, вялое со стертыми симптомами, низким уровнем фагоцитоза и образования антител.
Виды реактивности: 1. Биологическая (видовая, первичная) – изменения жизнедеятельности, возникающие под влиянием обычных для каждого животного воздействий окружающей среды. Например, невосприимчивость человека к чумке собак, к гонорее и сифилису крупного рогатого скота и т. д. Зимняя спячка - видовой вариант изменения реактивности (суслики не болеют в период спячки чумой и туберкулезом). 2. Групповая – формируется у групп индивидуумов, находящихся под влиянием общего фактора чаще всего внутренней среды. Например, чувствительность к психо-эмоциональному стрессу у гипер- и астеников. Реактивность мужчин и женщин. Возрастные изменения реактивности. Группы крови. 3. Индивидуальная – формируется в зависимости от совокупности конкретных факторов, в которых обитает и формируется организм (наследственность, возраст, пол, питание, температура, содержание кислорода).
· специфическая – характерна для одного конкретного фактора (иммунная, реакция зрачка на свет). · неспецифическая - характерна для различных факторов (стресс-реакция, парабиоз, фагоцитоз, биологические барьеры).
Резистентность (устойчивость) – это свойство организма противостоять различным воздействиям или невосприимчивость к воздействиям повреждающих факторов внешней среды.
Формы резистентности
Резистентность организма фармакологически в большинстве случаев стремятся повысить. Например, стимуляторы иммунной системы повышают устойчивость, сопротивляемость организма к микроорганизмам и опухолям.
Реактивность и резистентность организма не всегда изменяются однонаправлено. В некоторых случаях, повышенная иммунная реактивность организма может спровоцировать так называемые аллергические заболевания, вызывающие или повреждение структур организма (аутоиммунные заболевания), или иногда - даже летальный исход (анафилактический шок). В подобных случаях, требуется фармакологическая коррекция данного вида реактивности препаратами, угнетающими иммунный ответ.
|
|||||||||
|
Последнее изменение этой страницы: 2016-06-19; просмотров: 416; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.223.108.134 (0.012 с.) |