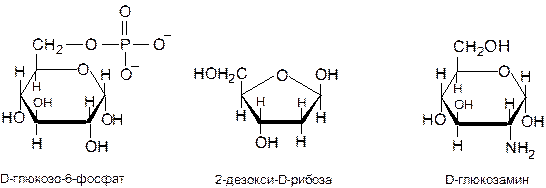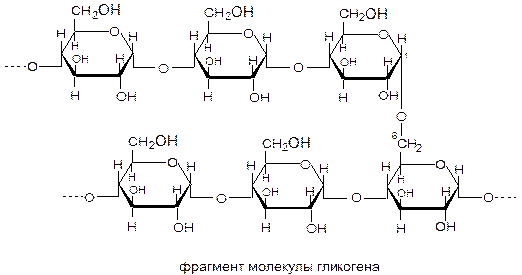Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Структура и свойства моносахаридовСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
Глава 6. УГЛЕВОДЫ
Производные моносахаридов Несмотря на то, что в растворе моносахарида равновесие существенно сдвинуто в сторону циклических форм, некоторое количество ациклической формы присутствует в растворе, что позволяет моносахаридам вступать в реакции, характерные для альдегидов и кетонов. Восстановление карбонильной группы моносахарида ведет к образованию сахарного спирта, например сорбита, образующегося при восстановлении альдегидной группы глюкозы. К сахарному спирту относится глицерин. Альдегидные группы альдоз могут окисляться множеством реагентов, образуя альдоновые кислоты, относящиеся кклассу сахарных кислот. Например, при окислении альдегидной группы D-глюкозы образуется D-глюконовая кислота, фосфорилированная форма которой является важным промежуточным продуктом углеводного обмена. Окислению может подвергаться и первичная –ОН-группа альдоз. При этом образуются уроновые кислоты. Так, при окислении первичной –ОН-группы D-глюкозы образуется D-глюкуроновая кислота. Уроновые кислоты являются компонентами многих полисахаридов. Характерным свойством уроновых кислот считается способность образовывать лактоны.
Одной из наиболее важных сахарных кислот является аскорбиновая кислота (витамин С), представляющая собой лактон. К производным моносахаридов относятся моносахариды, этерифицированные фосфорной кислотой, – фосфорнокислые эфиры. Они являются важными промежуточными продуктами углеводного обмена, например a-D-глюкозо-6-фосфат. Дезоксисахара представляют собой моносахариды, в которых одна или несколько ОН-групп замещены на атомы водорода. Важнейшим представителем является b-D-2-дезоксирибоза, которая входит в состав нуклеотидов ДНК. Аминосахара – моносахариды, в которых одна или несколько ОН-групп замещены на аминогруппы. Например, N-ацетилглюкозамин вместе с N-ацетилмурамовой кислотой входит в состав клеточной стенки прокариот.
Полисахариды В природе углеводы встречаются в основном в форме полисахаридов. Полисахариды представляют собой длинные полимерные цепочки, которые построены из остатков моносахаридов, соединенных между собой гликозидными связями. Полисахариды присутствуют во всех клетках и выполняют в них структурную, рецепторную, защитную функции, а также играют роль запасных веществ. В состав полисахаридов могут входить различные моносахариды. Полисахариды, построенные из остатков одного и того же моносахарида, называются гомополисахаридами, а полисахариды, содержащие остатки различных моносахаридов, − гетерополисахаридами. Чаще всего в составе полисахаридов встречается D-глюкоза. Нередко полисахариды имеют заместители неуглеводной природы – остатки серной, фосфорной или органических кислот. Полисахариды различаются также по типу гликозидной связи, молекулярной массе и степени разветвленности макромолекул. Молекулярная масса полисахаридов колеблется в широких пределах –от нескольких тысяч до нескольких миллионов дальтон. Большинство полисахаридов имеют тривиальные названия, связанные с источником, из которого они были выделены, например целлюлоза, крахмал, хитин. Основой более строгой номенклатуры служит моносахаридный состав полисахарида: D-глюканом называется полисахарид, построенный из остатков D-глюкозы. Резервные полисахариды. Большинство резервных полисахаридов – это гомополисахариды, в которых преобладают a(1®4)-гликозидные связи. Эти вещества выполняют роль источников углерода и энергии для клеток в периоды голодания, поэтому их структура отвечает основному требованию – доступности для гидролитических ферментов, их расщепляющих. К ним относятся крахмал и гликоген, которые представляют собой рыхлые, разветвленные структуры, доступные для ферментативного расщепления в большом количестве участков. Они откладываются в цитоплазме клеток в виде крупных гранул. Поддержание уровня глюкозы в крови является важной физиологической функцией, которая реализуется через биосинтез гликогена при избытке глюкозы и его гидролиз при недостатке глюкозы в клетке. Крахмал преобладает в клетках растений, микроводорослей, некоторых бактерий. Крахмал состоит из двух компонентов – a-амилозы и амилопектина. a-Амилоза представляет собой линейный полимер a-D-глюкозы (1000−4000 звеньев), остатки которой соединены с помощью a(1®4)-гликозидных связей. При этом в молекуле появляется большая свобода вращения вокруг связей С1−О и О−С4, и цепочка образует стабильную спираль с шестью остатками глюкозы на один виток. Молекулы йода по своим размерам точно подходят к центральной полости этой спирали и образуют комплекс, обусловливающий приобретение темно-синей окраски растворами a-амилозы при йодно-крахмальном тесте. Амилопектин состоит из цепей поли-a-D-глюкозы с a(1®4)-гликозидными связями, образующих остов молекулы. От этих цепей отходят боковые ветви, присоединенные к основной цепи a(1®6)-гликозидными связями. Ветви являются более короткими цепочками a(1®4)-глюкозида, содержащего 12 остатков D-глюкозы, и мешают основной цепи образовывать спираль. Амилопектин в отличие от a-амилозы имеет разветвленную структуру и вместе с a-амилозой образует сложную сеть. Молекулы амилопектина содержат сотни тысяч остатков a-D-глюкозы, являясь одними из самых крупных природных молекул. Гликоген преобладает в клетках животных, грибов и некоторых бактерий. Гликоген состоит из остатков a-D-глюкозы, соединенных a(1®4)-гликозидными связями. Его структура сильно напоминает структуру амилопектина, но у гликогена боковые ветви, присоединенные к основной цепи a(1®6)-гликозидными связями, расположены значительно чаще, чем у амилопектина, т. е. гликоген отличается от амилопектина большей разветвленностью и более плотной упаковкой молекулы. У гликогена отсутствует спиральная структура, и его молекулы еще более «открыты» действию ферментов.
Структурные полисахариды. К ним относятся полисахариды, являющиеся основными компонентами клеточных стенок растений и микроорганизмов. Клеточные стенки растений обладают необычайной прочностью и в процессе роста растения меняют свою структуру и состав. Основными компонентами клеточных стенок растений являются полисахариды, среди которых преобладает целлюлоза, в значительной степени определяющая архитектуру клеточной стенки. Этот гомополисахарид является самым распространенным углеводом на Земле (древесина содержит ~50% целлюлозы). Мономерами целлюлозы служат остатки b-D-глюкозы, соединенные в длинные цепочки (до 10 000 остатков глюкозы в каждой) с помощью b(1®4)-гликозидных связей. В такой молекуле отсутствует полная свобода вращения вокруг С1−О и О−С4-связей, и полимер приобретает конформацию, благоприятную для образования межцепочечных поперечных водородных связей в случае, когда цепочки располагаются антипараллельно. В результате молекулы целлюлозы объединяются в микрофибриллы толщиной 10−25 нм. Они перевиваются и образуют тонкие нити, которые, в свою очередь, могут обматываться одна вокруг другой, как пряди в канате, формируя макрофибриллы. Каждая макрофибрилла имеет толщину ~ 0,5 мкм и длину 6−8 мкм. Прочность макрофибрилл сопоставима с прочностью стальной проволоки. Кроме того, отдельные участки микрофибрилл имеют упорядоченное строение и придают клеточной стенке кристаллические свойства. Таким образом, целлюлоза за счет сложности своей структуры и высокой упорядоченности выполняет защитную и опорную функции в растении. В таком виде полисахариды недоступны действию собственных ферментов, и целлюлоза не может использоваться растением как резервное вещество. Только некоторые бактерии, грибы, простейшие обладают ферментными системами, способными расщеплять целлюлозу. Микро- и макрофибриллы целлюлозы в клеточной стенке погружены в матрикс, который также состоит в основном из полисахаридов и меняет свою структуру в процессе роста растения. На начальных этапах развития матрикс состоит из пектиновых веществ, а в дальнейшем в нем появляются гемицеллюлозы.Пектиновые вещества – это полимеры a-D-галактуроновой кислоты, в которых некоторые водородные атомы замещены метильными группами. Гемицеллюлозы делятся на ксиланы (полимеры ксилозы), глюкоманнаны и галактаны. На более поздних этапах развития растения, когда происходит одревеснение клеточной стенки, в клетках откладывается лигнин – химически устойчивый полимер, содержащий большое число ароматических спиртов. Кроме этого, в составе клеточных стенок растений обнаружены небольшие количества гликопротеинов, нерастворимых липидных полимеров и восков. Лабораторная работа Выполнение работы Вопросы для самоконтроля 1. Что собой представляют моно-, олиго- и полисахариды? 2. Какие моносахариды относятся к альдозам, а какие – к кетозам? Приведите примеры. 3. Назовите, какие стереоизомерные формы характерны для моносахаридов. Как определить принадлежность моносахаридов, содержащих два и более асимметрических атома углерода, к D- или L-ряду? 4. Что такое эпимеры? Приведите примеры. 5. Напишите реакции образования циклического полуацеталя и циклического полукеталя из D-глюкозы и D-фруктозы соответственно. 6. Чем обусловлено существование a- и b-изомеров моносахаридов? Какой углеродный атом циклических альдоз называется аномерным? 7. Приведите различные способы изображения циклических форм моносахаридов. Какая из этих конформаций термодинамически более устойчива и почему? 8. В чем состоит суть явления мутаротации? 9. Напишите структурные формулы производных моносахаридов. Укажите их биохимические функции. 10. Какие функциональные группы моносахаридов принимают участие в формировании гликозидной связи и как ее обозначают? Напишите уравнение реакции. 11. Чем отличаются восстанавливающие олигосахариды от невосстанавливающих? Приведите примеры. 12. Какова роль в клетках резервных и структурных полисахаридов? Приведите примеры. 13. В чем состоят особенности выделения и анализа полисахаридов? 14. Объясните принцип качественной реакции Молиша на a-D-глюкозу. 15. На чем основан метод количественного определения a-D-глюкозы по Миллеру?
Глава 6. УГЛЕВОДЫ
Структура и свойства моносахаридов Моносахариды, их олигомеры (олигосахариды) и полимеры (полисахариды) составляют класс углеводов. Моносахариды представляют собой альдегиды или кетоны, содержащие две или более ОН-групп, общей формулой (СН2О) n. Кроме гидроксильных и карбонильных групп они могут содержать тиольные, карбоксильные группы, аминогруппы и др. Полисахариды являются продуктами поликонденсации моносахаридов. Это типичные полимеры, построенные из множества моносахаридных остатков. Олигосахариды составляют промежуточную группу между моно- и полисахаридами и содержат от двух до десяти моносахаридных остатков. Простейшие из моносахаридов (n = 3) называются триозами. К ним относятся глицеральдегид и дигидроксиацетон. Глицеральдегид назван альдозой, так как он содержит альдегидную группу, а дигидроксиацетон – кетозой, поскольку он содержит кетогруппу.
Моносахариды с четырьмя, пятью и шестью атомами углерода называются соответственно тетрозами, пентозами и гексозами. Так, из гексозных сахаров D-глюкоза является альдозой, а D-фруктоза – кетозой.
Природные моносахариды обладают оптической активностью, причем величина удельного вращения является характерным параметром моносахарида. Все моносахариды, за исключением дигидроксиацетона, содержат один или более асимметрических атома углерода. Простейшей альдозой, имеющей один асимметрический атом углерода, является глицеральдегид, существующий в двух стереоизомерных формах – D- и L-изомеров.
Моносахариды, содержащие два и более асимметрических атома углерода, относятся к D- или L-ряду в зависимости от конфигурации асимметрического атома углерода, наиболее удаленного от альдегидной или кетогруппы. Моносахарид (изображенный в проекциях Фишера) относят к D-ряду, если ОН-группа асимметрического атома углерода, наиболее удаленного от альдегидной или кетогруппы, находится справа, а атом водорода слева как в D-глицеральдегиде. Если ОН-группа асимметрического атома углерода, наиболее удаленного от альдегидной или кетогруппы, находится слева, а атом водорода справа как в L-глицеральдегиде, моносахарид относят к L-ряду.
Простейшей кетозой, имеющей один асимметрический атом углерода, является тетроза – тетрулоза. Два моносахарида, отличающиеся только по конфигурации одного определенного атома углерода, называются эпимерами. Например, D-глюкоза и D-манноза являются эпимерами по второму углеродному атому, а D-глюкоза и D-галактоза – эпимерами по четвертому углеродному атому.
Приведенные выше структуры моносахаридов являются ациклическими. Однако моносахариды могут образовывать циклические структуры в результате взаимодействия карбонильной группы моносахарида с одной из его гидроксильных групп. Альдегидная группа обладает высокой реакционной способностью и может реагировать с –ОН-группой с образованием циклического полуацеталя. Так, альдегидная группа при С1 атоме в молекуле глюкозы с открытой цепью реагирует с –ОН-группой при С5 атоме этой же молекулы, образуя внутримолекулярный полуацеталь. Образованный таким образом 6-членный циклический сахар называется пиранозой из-за его сходства с пираном.
D-глюкоза a-D-глюкопираноза Подобно этому кетогруппа может реагировать с –ОН-группой с образованием циклического полукеталя. Так, кетогруппа при С2 атоме фруктозы с открытой цепью взаимодействует с –ОН-группой при С5 атоме с образованием внутримолекулярного полукеталя. Этот 5-членный циклический сахар называется фуранозой из-за его сходства с фураном. У альдоз фуранозный цикл образуется с участием –ОН-группы при С4 атоме.
D-фруктоза a-D-фруктофураноза При циклизации альдоз и кетоз возникает новый хиральный центр при С1 и С2 атомах, ранее входивших в состав альдегидной и кетогруппы соответственно. Это влечет за собой появление еще одной пары стереоизомеров (аномеров) для каждого моносахарида, которые отличаются друг от друга по конфигурации С1 (С2 у кетоз) карбонильного атома и называются a-иb- изомерами (аномерами). Символ a означает, что –ОН-группа при С1 (С2 у кетоз) атоме расположена под плоскостью кольца, а символ b означает, что эта –ОН-группа находится над плоскостью кольца. С1 (С2 у кетоз) атом, находящийся в центре полуацетальной группы и непосредственно связанный с двумя атомами кислорода, называется аномерным углеродным атомом, а гидроксил, образующийся при С1 (С2 у кетоз) атоме в результате циклизации моносахарида, называется полуацетальным. Он резко отличается по свойствам от других –ОН-групп молекулы и легко может замещаться на другие нуклеофильные группы с образованием различных производных моносахаридов.
a-D-глюкоза b-D-глюкоза Циклические формы моносахаридов принято изображать в формулах Хеуорса, так как проекционные формулы Фишера дают весьма смутное представление о трехмерной структуре моносахаридов. Нижнюю часть кольца (жирные линии) представляют выступающей к наблюдателю, а противоположный край – лежащим за плоскостью рисунка. Примерная плоскость кольца перпендикулярна плоскости бумаги. Эти формулы однозначно указывают конфигурацию молекулы, но не отображают взаимного пространственного расположения групп, присоединенных к кольцу. Поэтому для изображения пространственной структуры моносахаридов применяются конформационные формулы. Благодаря свободному вращению групп вокруг С−С-связей молекулы моносахаридов могут принимать различные конформации. 6-членное пиранозное и 5-членное фуранозное кольца в действительности не плоские. Большинство пираноз и их производных имеет термодинамически более устойчивую конформацию кресла, в которой большая часть замещающих групп (–СН2ОН, –ОН-групп) располагается в экваториальной плоскости. Для b-D-глюкопиранозы конформация кресла является предпочтительной, так как –СН2ОН и все –ОН-группы расположены экваториально, когда связь заместителя с кольцом образует с осью молекулы тетраэдрический угол. Все атомы водорода b-D-глюкопиранозы расположены аксиально, т. е. параллельно оси молекулы.
b-D-глюкоза В растворах одновременно присутствуют все возможные изомеры одного и того же моносахарида, находящиеся в динамическом равновесии друг с другом приблизительно в эквимолярных соотношениях. В обычных условиях равновесие существенно сдвинуто в сторону циклических a- и b-пираноз (фураноз), что в значительной степени определяется термодинамикой конформации пиранозного (фуранозного) кольца. Так, при растворении a- или b-изомеров D-глюкозы в воде при 25оС образуется равновесная смесь, состоящая примерно на 1/3 из a-D-глюкозы, для которой [a]D20 = +112,2° и на 2/3 из b-D-глюкозы, для которой [a]D20 = +18,7°. Со временем оптическое вращение раствора постепенно изменяется и в конце концов достигает равновесного значения [a]D20 = +52,7°. Это явление называется мутаротацией. Образовывать устойчивые кольца и существовать в виде аномерных форм способны только моносахариды с пятью и более атомами углерода. Тетрозы и триозы в водном растворе могут существовать только в ациклической форме. Производные моносахаридов Несмотря на то, что в растворе моносахарида равновесие существенно сдвинуто в сторону циклических форм, некоторое количество ациклической формы присутствует в растворе, что позволяет моносахаридам вступать в реакции, характерные для альдегидов и кетонов. Восстановление карбонильной группы моносахарида ведет к образованию сахарного спирта, например сорбита, образующегося при восстановлении альдегидной группы глюкозы. К сахарному спирту относится глицерин. Альдегидные группы альдоз могут окисляться множеством реагентов, образуя альдоновые кислоты, относящиеся кклассу сахарных кислот. Например, при окислении альдегидной группы D-глюкозы образуется D-глюконовая кислота, фосфорилированная форма которой является важным промежуточным продуктом углеводного обмена. Окислению может подвергаться и первичная –ОН-группа альдоз. При этом образуются уроновые кислоты. Так, при окислении первичной –ОН-группы D-глюкозы образуется D-глюкуроновая кислота. Уроновые кислоты являются компонентами многих полисахаридов. Характерным свойством уроновых кислот считается способность образовывать лактоны.
Одной из наиболее важных сахарных кислот является аскорбиновая кислота (витамин С), представляющая собой лактон. К производным моносахаридов относятся моносахариды, этерифицированные фосфорной кислотой, – фосфорнокислые эфиры. Они являются важными промежуточными продуктами углеводного обмена, например a-D-глюкозо-6-фосфат. Дезоксисахара представляют собой моносахариды, в которых одна или несколько ОН-групп замещены на атомы водорода. Важнейшим представителем является b-D-2-дезоксирибоза, которая входит в состав нуклеотидов ДНК. Аминосахара – моносахариды, в которых одна или несколько ОН-групп замещены на аминогруппы. Например, N-ацетилглюкозамин вместе с N-ацетилмурамовой кислотой входит в состав клеточной стенки прокариот.
|
||||
|
Последнее изменение этой страницы: 2016-12-27; просмотров: 885; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.220 (0.011 с.) |