Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Закон отношения проводимостей.Содержание книги
Поиск на нашем сайте
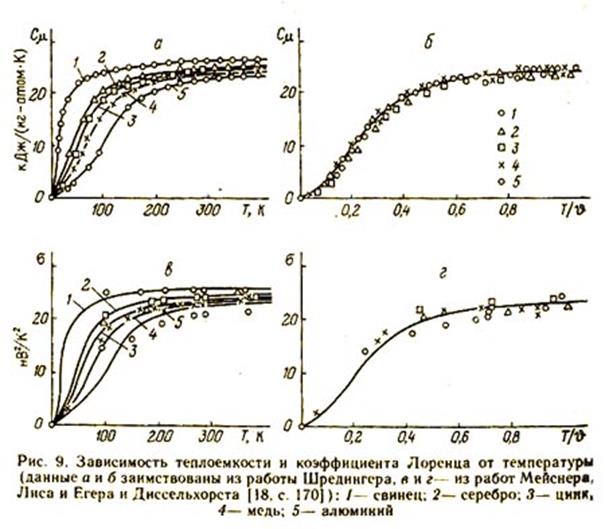
Воспользуемся теперь началами, определяющими явления переноса, и выведем еще два новых закона, из которых вытекают многие известные законы физики и химии; для простоты рассмотрим две степени свободы. Первый закон - отношения проводимостей - получается из соотношений (106), (112), (113), (117), (118), (122), (123), (127), (128). При n = 2имеем [16, с.24; 17, с.65; 18, с.167; 21, с.185] a11/a22 = b11/b22 = L11/L22 = M11/M22 = s = KP11/KP22 = AP22/AP11; (298) a12/a11 = b12/b11 = L12/L11 = M12/M11 = s1211 = KP12/KP11 = AP11/AP12. (297) Закон отношения проводимостей формулируется следующим образом: отношение проводимостей s или s1211 для любой пары степеней свободы системы равно отношению сопряженных с ними емкостей. Из законов отношения проводимостей и тождественности в качестве частного случая вытекает известный опытный закон Видемана-Франца (1853 г.) с поправкой Лоренца (1872 г.). Применительно к термоэлектрической системе, если в формуле (296) вермопроводность LQ и вермоемкость КQ выразить через теплопроводность LQ и теплоемкость С, а электроемкость КY - через аналог газовой постоянной RY из соответствующего уравнения состояния для идеальной термоэлектрической системы, то получится выражение [18, с.168; 21, с.186] LQ/ LY = sТ = RYиСmТ (298) где s = RYиСm (299) Индексом μ отмечены мольные значения величин. Это и есть искомое теоретическое уравнение. Совместно с приближенным законом тождественности, утверждающим одинаковость мольных емкостей, оно говорит о том, что отношение теплопроводности к электропроводности пропорционально абсолютной температуре Т и приблизительно не зависит от рода металла, коэффициент пропорциональности s именуется коэффициентом Лоренца. Закон Видемана-Франца получается, если правую часть уравнения (298) считать величиной постоянной. Поправку Т ввел Лоренц; он установил, что постоянным является коэффициент s. Однако в действительности, согласно ОТ, коэффициент Лоренца s есть величина переменная, определяемая формулой (299); он пропорционален теплоемкости. Для металлов в первом приближении можно принять RYm = 10-12 кг×атом/(Ф×К) (300) Выводы ОТ хорошо подтверждаются экспериментами, в которых коэффициент Лоренца и теплоемкость определяются независимыми методами. Например, на рис. 9, а приведена опытная зависимость мольной теплоемкости при.постоянном давлении от температуры для различных металлов. Теплоемкости использованы для определения по формулам (299) и (300) коэффициента Лоренца; эти его значения изображены на рис. 9, е в виде кривых; здесь же точками нанесены опытные коэффициенты Лоренца, найденные как отношение теплопроводности к электропроводности. Совпадение результатов получается удовлетворительным.
Для большей наглядности на рис 9, 6 мольная теплоемкость изображена в функции от относительной температуры Т/J, где J - характеристическая температура, фигурирующая в теории теплоемкости Дебая; при этом, как показал Шредингер, опытные значения теплоемкости для различных металлов группируются вблизи одной кривой. Эта кривая, пересчитанная на коэффициент Лоренца, приведена на рис. 9, г;здесь же в виде точек представлены опытные значения коэффициента Лоренца. Эти точки тоже хорошо группируются вблизи универсальной теоретической кривой [17, с.133; 18, с.170]. Предлагаемый способ выражения коэффициента Лоренца через температуру Дебая очень удобен на практике. При определении по формулам (298) и (300) одних величин (неизвестных) с помощью других (известных) можно пользоваться обобщенной кривой, приведенной на рис. 9, г,которая дает универсальную зависимость коэффициента s от температуры для различных металлов. Однако, согласно закону состояния, коэффициент RYm, входящий в формулы (298) и (299), постоянен только для идеального ансамбля. У реальных ансамблей он должен быть функцией вермиора и электриора (электрического заряда), а следовательно, температуры и электрического потенциала. В работе [20, с.247] установлена существенная зависимость коэффициента RYm от температуры, причем линейная аппроксимация этой зависимости дает хорошие по точности результаты. Это позволяет уточнить расчет свойств различных металлов с помощью коэффициента Лоренца. Коэффициент RYm является величиной, обратной электроемкости КYm [20, с.251]. Но всякая емкость обладает свойством аддитивности. Следовательно, на основе аддитивности величины 1/RYm можно рассчитывать свойства сплава по известным свойствам отдельных компонентов, входящих в его состав. Соответствующий метод, сопровождаемый многочисленными экспериментальными данными, приводится в монографии [20, с.243]. Опыт показывает, что уравнение (298) может быть использовано также для определения свойств металлов и сплавов в жидком состоянии. При этом характеристическая температура Дебая уже не играет столь важной роли, как для твердых металлов [20, с.249]. Некоторые из описанных методов пригодны для полупроводников. В этом случае наблюдается заметная зависимость коэффициента RYm не только от температуры, но и от электрического потенциала, что хорошо согласуется с выводами ОТ. Из сказанного ясно, что ОТ вносит в закон Видемана-Франца и Лоренца серьезные поправки. Во-первых, металлы следует сравнивать при одинаковых не абсолютных (Т), аотносительных (Т/J) температурах. Во-вторых, надо пользоваться не постоянным, а переменным значением коэффициента Лоренца. В-третьих, закон Видемана-Франца и Лоренца является в принципе приближенным законом, ибо, согласно ОТ, коэффициент Лоренца пропорционален отношению емкостей, а одинаковость емкостей для различных металлов есть следствие приближенного закона тождественности. Из закона отношения проводимостей вытекают также некоторые другие известные законы, в частности закон Грюнейзена (1908 г.), согласно которому отношение объемного коэффициента теплового расширения к теплоемкости не зависит от температуры [18, с.175]. Кроме того, из закона отношения проводимостей могут быть выведены многие новые закономерности для твердых, жидких и газообразных тел и различных степеней свободы системы, охватывающих, например, такие свойства, как диэлектрическая постоянная, магнитная проницаемость, вязкость, изотермическая сжимаемость и т.д. [17, 18]. Эти закономерности могут быть с успехом применены на практике для определения неизвестных свойств веществ по известным [ТРП, стр.303-306].
Закон отношения потоков.
Вторым упомянутым выше частным законом является закон отношения потоков. Он с количественной стороны характеризует эффект увлечения одних потоков другими. Выводится этот закон в предположении, что все термодинамические силы, кроме данной, равны нулю [18, с.283]. В этих условиях для двух степеней свободы (n = 2), например, из уравнений (116) при Х2 = 0 получаем s1121 = (I1/I2)Х2 =0 = (dE1/dE2)Х2 =0 = b11/b21 = KP11/KP21 (301) При Х1 = 0 имеем s1222 = (I1/I2)Х1 =0 = (dE1/dE2)Х1 =0 = b12/b22 = KP12/KP22 (302) Проводимости b в этих равенствах могут быть заменены другими частными проводимостями на основе соотношений (296) и (297) закона отношения проводимостей. Закон отношения потоков формулируется следующим образом: при наличии нескольких степеней свободы и действии только одной термодинамической силы отношение любых двух потоков или экстенсоров равно отношению сопряженных с ними проводимостей или емкостей. Закон отношения потоков совместно с приближенным законом тождественности позволяет установить группу ансамблей, в пределах которых соблюдается постоянство (одинаковость) отношения соответствующих потоков. Из этих двух законов вытекают, например, известные эмпирические правило (закон) Трутона [17, с.311; 18, с.337], первый и второй законы Фарадея [18, с.345] и т.д. Чтобы вывести эти и многие другие законы, надо написать уравнения переноса типа (116) для химической, фазовой, вермической, механической, электрической, диффузионной и некоторых других степеней свободы. Например, фазовые превращения происходят под действием разности фазовых интенсиалов (фазиалов) δμф. При конечной разности δμф и нулевых значениях разностей всех остальных интенсиалов, включая температуру, из уравнения (302) получается, что отношение удельной мольной теплоты фазового превращения к абсолютной температуре равно отношению соответствующих мольных емкостей. При этом тепловой эффект превращения по существу представляет собой эффект увлечения вермического вещества массой. Отсюда видно, что закон Трутона, утверждающий, что для одной килограмм-молекулы всех веществ отношение теплоты к температуре испарения или конденсации есть величина постоянная, соблюдается только в меру постоянства мольных емкостей, входящих в правую часть выражения (302). О неточности закона Трутона можно судить по данным, приведенным в работе [18, с.338]. Для процессов плавления и затвердевания закон Трутона выполняется еще хуже, чем для испарения и конденсации, так как у жидких и твердых тел емкости сильнее зависят от состава ансамбля, в том числе от его массы, об этом уже говорилось выше. Таким образом, ОТ позволяет внести в закон Трутона определенные разъяснения, уточнения и ограничения. Во-первых, приходится констатировать, что этот закон в целом правильно отражает общую тенденцию развития процессов испарения и конденсации. Вместе с тем он является в принципе приблизительным законом, ибо фактически опирается на приближенный закон тождественности. Неточность закона тождественности, а следовательно, и закона Трутона объясняется, как мы уже убедились, наличием всеобщей связи между различными степенями свободы системы. Прежние теории не учитывали этих связей, поэтому не могли пролить свет на загадочную неточность закона Трутона. Происхождение этой неточности всегда было неясно и вызывало много недоуменных вопросов. Теперь, наконец, становятся понятными как физический смысл, так и причина приближенности закона Трутона. Во-вторых, ОТ позволяет внести в закон Трутона весьма существенное ограничение, связанное с действием закона экранирования седьмого начала. Это ограничение имеет общий смысл, относится ко всем степеням свободы системы и касается всех случаев определения теплового эффекта различных фазовых и химических превращений, реакций, процессов и т.д., поэтому на нем целесообразно остановиться более подробно; суть его заключается в следующем. Любой реальный процесс протекает под действием определенной разности интенсиалов. Согласно закону экранирования (222), это связано с выделением или поглощением некоторого количества тепла диссипации (экранирования). Экранированная теплота в принципе неотличима от основной работы переносимого или увлеченного вермиора. Следовательно, при определении тепловых эффектов фазовых и химических превращений надо обязательно учитывать степень необратимости реального процесса, то есть количество экранированного в этом процессе тепла. Например, в случае фазового превращения к увлеченному массой равновесному теплу превращения rm добавляется (при конденсации и затвердевании) или вычитается (при испарении и плавлении) экранированное тепло в количестве RЭm = ТQЭm = - δμфmm (303) где ΘЭμ - экранированный вермиор, определяемый по формуле (223), mm - масса одной килограмм-молекулы вещества. Неучет экранированного тепла rэm,может привести к существенным ошибкам. Поэтому опыты по определению величины rm, надо проводить в условиях, близких к равновесным, когда δμф ® 0. В противном случае на величине rm скажется эффект неравновесности, который обнаружит себя в том, что rm при конденсации и затвердевании будет выше, чем при испарении и плавлении. Равновесное значение rm, представляющее собой физический коэффициент, заключено между двумя этими значениями. Кстати сказать, отсюда следует, что о степени неравновесности реального процесса можно судить по отклонению полученной в опыте величины rm от ее равновесного значения. При этом надо иметь в виду, что на величине rm может сказаться также неравенство нулю других интенсиалов. Выведем теперь уравнения первого и второго законов Фарадея, регламентирующих явления электролиза. Для этого в уравнении переноса типа (116) положим равными нулю все разности интенсиалов, кроме электрического. В результате получается следующее новое теоретическое соотношение [18, с.345; 21, с.190]: smYYY = Im/IY = m/Y = bmY/bYY = KPmY/KPYY (304) которое определяет первый закон Фарадея, установленный им экспериментально в 1833-1834 гг.: при электролизе за время t на электродах выделяются количества вещества m, пропорциональные количеству электрического заряда Ψ,прошедшего через то же время через электролит. Уравнение (304) закона отношения потоков ОТ дает точное значение коэффициента пропорциональности. При последовательном соединении нескольких электролитов количества выделившихся веществ пропорциональны килограмм-эквивалентам этих веществ - таково содержание второго закона Фарадея. Под килограмм-эквивалентом понимается отношение m/z, где μ - атомная или молекулярная масса иона, z - его валентность. Иными словами, величина m/z представляет собой массу ансамбля, переносимого (увлеченного) единичной порцией (квантом) электрического заряда. Для этого случая из выражения (304) получаем smYYY = m/(zYF) где YF – электрический заряд, Ф, переносящий один килограмм-эквивалент вещества. Из двух последних равенств имеем m = mY/(zYF) (305) Первый (304) и второй (305) эмпирические законы Фарадея составляют основу современной электрохимии. Согласно закону отношения потоков, они характеризуют эффект увлечения массы электрическим зарядом. Применить к ним закон тождественности не представляется возможным, так как ионы одинаковой валентности обычно сильно разнятся по массе. Согласно общей теории, равенства (304) и (305) справедливы только в том случае, когда напоры всех интенсиалов, кроме электриала δφ, равны нулю. В противном случае масса может переноситься также под действием разностей и других интенсиалов. С помощью уравнений переноса и закона отношения потоков можно написать большое множество конкретных соотношений типа (301), (302) и (304), выражающих определенные закономерности развития различных реальных процессов. Большинство этих закономерностей еще нигде не используется и не имеет названий. Но несомненно, что многие из них со временем найдут практическое применение. Характерным примером тому служат известные законы Фарадея и Трутона. Добавление к найденным соотношениям приближенного закона тождественности дает возможность объединить однотипные явления в определенные группы, как это сделано Трутоном и Фарадеем. В настоящей главе и ранее неоднократно упоминаются так называемые физические коэффициенты. Согласно ОТ, физическими коэффициентами служат коэффициенты при экстенсорах и интенсиалах в уравнениях состояния и переноса, а также в уравнениях более высоких порядков. Например, к ним относятся коэффициенты состояния, емкости и проводимости и т.п., а также комбинации из указанных характеристик типа s, R, r, YF и т.д. Важно подчеркнуть, что все они суть функции экстенсоров и, следовательно, в принципе являются величинами переменными. В определенных условиях их можно условно, с большим или меньшим приближением к действительности, рассматривать как величины постоянные; часто это приводит к существенному упрощению задачи, например, в случае идеального тела (см. параграф 7 гл. X). Хорошие результаты при этом дают осредненные значения коэффициентов в соответствующем диапазоне изменения параметров. Физическими коэффициентами не являются главные количественные характеристики ансамбля - экстенсоры, а также энергия, служащая производным свойством первого порядка, интенсиалы, служащие производными свойствами второго порядка, работа и некоторые другие величины. Вместе с тем экстенсоры содержат в себе характеристики, которые по справедливости могут быть названы фундаментальными, или абсолютными,или мировыми физическими постоянными (константами). Таковыми служат минимальные порции (кванты) различных простых веществ, например электрического (заряд электрона, или электриант е),вермического (вермиант t), вибрационного (постоянная Планка h) и т.д. Не исключено, что и эти константы способны претерпевать какие-то изменения со временем [18, с.196; 21, с.242]. Все остальные коэффициенты не являются константами в истинном смысле этого слова [ТРП, стр.306-310].
Теорема интенсиалов.
Для завершения краткой иллюстрации различных способов применения начал рассмотрим одну весьма любопытную теорему, которая характеризует определенные тенденции развития самопроизвольных природных процессов. Теорема гласит, что в изолированной неравновесной системе среднее значение любого данного интенсиала способно и вынуждено самопроизвольно изменяться за счет других интенсиалов; количественная сторона и направление этого изменения определяются конкретными свойствами системы. Докажем эту теорему с помощью семи начал ОТ [20, с.240; 21, с.176]. Дана реальная изолированная неравновесная система, обладающая n степенями свободы и удовлетворяющая условию (298). В объеме такой системы происходит непрерывное самопроизвольное перераспределение всех n веществ и постепенное выравнивание всех n интенсиалов. Этот процесс сопровождается следующими эффектами. Согласно уравнению (31) первого начала ОТ, суммарная энергия системы остается неизменной, то есть dU = 0; U = const. Согласно уравнению (50) второго начала ОТ, общее количество любого i -того вещества системы сохраняется постоянным, то есть dEi = 0; Εi = const. Перераспределение веществ в системе подчиняется пятому и шестому началам, а изменение состояния - третьему и четвертому. Система является реальной; это значит, что в общем случае в ней все коэффициенты состояния суть величины переменные. Отсюда прямо следует, что выравнивание интенсиалов неизбежно сопровождается изменением их средних значений. Средние значения могли бы оставаться постоянными только в том случае, если бы система была идеальной, то есть обладала бы постоянными значениями коэффициентов состояния (емкостей). Весьма существенно, что изменениям подвергаются средние значения всех интенсиалов. Это объясняется всеобщей связью явлений и находит свое выражение в неравенстве нулю перекрестных коэффициентов состояния. В результате каждый данный интенсиал испытывает влияние со стороны всех n перераспределяющихся веществ одновременно. Не менее существенно и то обстоятельство, что изменение средних значений любого данного интенсиала может происходить только за счет других, ибо подчиняется законам сохранения энергии и экстенсора. Благодаря этому возрастание каждого данного интенсиала по необходимости влечет за собой уменьшение остальных и наоборот. Теорема доказана. Эффект самопроизвольного изменения интенсиалов изолированной неравновесной системы усиливается благодаря действию седьмого начала ОТ, особенно его закона экранирования. Выделяющееся экранированное вермическое вещество поступает в общий фонд свободных аргументов уравнения состояния и через последнее изменяет все остальные интенсиалы. На средние значения интенсиалов могут повлиять также другие содержащиеся в системе и высвобождающиеся экранированные вещества. Как видим, даже простые процессы перераспределения веществ способны вызвать изменение средних значений интенсиалов. Возможности изменений заметно расширяются при наличии в системе более сложных естественных или искусственно воспроизводимых процессов, например круговых. Весьма важно, что теорема интенсиалов справедлива для любых степеней свободы системы - хрональной, метрической, кинетической, ротационной, вибрационной, вермической, электрической и т.д. Особый интерес представляет кинетическая степень, у которой интенсиалом служит скорость в квадрате. Это значит, что теорема утверждает способность и необходимость изменения скорости изолированной системы за счет изменения других ее интенсиалов, то есть утверждает принципиальную осуществимость безопорных движителей (БМ) [20, с.242; 21, с.178]. Соответствующий пример изменения скорости естественного тела, каковым является планета Земля, обсуждается в работе [21, с.179]. Теория и практика осуществления искусственных БМ рассматриваются в гл. XXI и XXII. На этом можно закончить краткое изложение различных характерных способов применения начал. Приведенные примеры хорошо иллюстрируют возможности теории. Теперь можно приступить к более подробному изучению свойств всевозможных явлений, находящихся на различных количественных и качественных уровнях мироздания, а также к более детальному анализу различных известных законов, теорий и научных дисциплин. Начнем с повторного рассмотрения наипростейшего макроявления, или парена, но уже с привлечением всего аппарата ОТ [ТРП, стр.310-312].
|
|||||||
|
Последнее изменение этой страницы: 2016-06-19; просмотров: 396; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.145.88.111 (0.012 с.) |