Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Ряд факторов влияет на аффинность гемоглобинаСодержание книги
Поиск на нашем сайте к О2, т.е. на насыщение гемоглобина кислородом при данном РО2. При этом, в первую очередь, изменяется положение кривой и гораздо меньше форма кривой. Отсюда можно описать уменьшение аффинности как сдвиг кривой связывания гемоглобином кислорода вправо (повышенный Р0.5), а увеличение аффинности, как сдвиг кривой связывания гемоглобином кислорода влево (пониженный Р0,5). Повышение температуры приводит к понижению аффинности, т.е. приводит к сдвигу кривой связывания вправо (рис. 7-32). Наоборот, охлаждение вызывает сдвиг кривой влево. У гомойотермных организмов значение этого влияния небольшое, хотя температура крови на периферии тела отчетливо может отклоняться от температуры всего организма. Более важным является влияние концентрации ионов Н+ и РСО2. Повышение концентрации ионов Н+ (понижение рН) вызывает снижение аффинности гемоглобина к кислороду (сдвиг кривой вправо), понижение концентрации ионов Н+ вызывает повышение аффинности гемоглобина к кислороду. Эта зависимость, известная как эффект Бора, осуществляется путем аллостерического обменного влияния (термин «аллостерический» означает «связанный с другим центром») между местом связывания Н+ и местом связывания О2. Эффект Бора может быть связан также с изменением РСО2: повышение РСО2сдвигает кривую связывания О2 вправо, понижение - влево. Это влияние основывается, в первую очередь, на том, что повышение РСО2 ведет к понижению рН и наоборот. Влияние самих молекул СО2 на аффинность гемоглобина к О2 является, напротив, незначительным. Эффект Бора помогает как насыщению гемоглобина кислородом, так и отдаче О2 в тканях. В легких РСО2 в крови понижается именно в связи с отдачей СО2 и при этом рН повышается. Из-за этого повышается способность гемоглобина связывать О2. В тканях в связи с поступлением СО2, РСО2 в крови повышается и рН понижается. Это способствует отдаче гемоглобином кислорода и поступлению О2 в клетки. Вообще сдвиг кривой связывания гемоглобином О2 влево благоприятствует процессам насыщения гемоглобина кислородом в легких, так как при одинаковом РО2 достигается более высокое насыщение гемоглобина кислородом. С другой стороны, сдвиг кривой вправо облегчает освобождение О2 в тканях, так как при одинаковом насыщении О2 РО2, вызывающее диффузию, повышается. К2 роме того, на аффинность гемоглобина к О2 влияет внутриэритроцитная концентрация катионов. Но особенно выраженным является снижающий аффинность гемоглобина к О2 эффект 2,3-дифосфоглицерата (2,3-BPG), чья концентрация в эритроцитах сходна с концентрацией тетрамерного гемоглобина (приблизительно 2,5 ммоль). В отсутствии 2,3-BPG аффинность гемоглобина к О2 является очень высокой (Р0,5 = 2 кПа). Главная функция 2,3-BPG состоит, следовательно, в правом перемещении кривой связывания О2, т.е. в область, которая соответствует физиологическим условиям. Рис. 7-32. Факторы влияющие на аффинность гемоглобина к О2. Уменьшение аффинности означает, что при одинаковом РО2 Hb способен связывать О2 в меньшей степени; кривая при этом сдвигается вправо. Причиной этого является повышение ряда факторов в эритроците (t°, рН, CO2 и т.п.). Уменьшение этих факторов влияет, наоборот, на повышение аффинности, т.е. сдвиг кривой влево
Карбоксигемоглобин Способность к транспорту кислорода кровью нарушается, если гемоглобин не способен присоединять О2. При этом, практически важными являются две формы гемоглобина. Угарный газ (окись углерода, монооксид углерода: CO) может вместо О2 обратимо связать двухвалентное железо гемма, и тогда возникает карбоксигемоглобин (HbCO). Аффинность гемоглобина к СО приблизительно в 300 раз больше, чем к О2, т.е. гемоглобин связывает СО более активно. В этом случае гемоглобин не может быть использован для транспорта О2. Соединение СО с железом гема ведет к увеличению аффинности остальных молекул гема тетрамерного Hb к О2. То есть при связывании Hb с СО повышается аффинность Hb к О2, что препятствует отдаче О2 в тканях (см. выше), и кривая связывания О2, следовательно, сдвигается влево (рис. 7-33). Из-за высокой аффинности гемоглобина к СО даже очень низкие парциальные давления СО приводят к связыванию значительного количества гемоглобина с СО с образованием HbCO. То, что у людей, находящихся в условиях интенсивного уличного движения транспорта, или при курении отравления СО наступают редко, объясняется только медленным переходом СО из альвеолярного газа в кровь. Метгемоглобин Двухвалентное железо гема (Fe2+) может окисляться в трехвалентное (Fe3+). Гемоглобин с трехвалентным железом называется метгемоглобин (MetHb, также хемиглобин). Он не может обратимо присоединять О2 и поэтому является для транспорта О2неактивным. Совершенно похоже, как и при соединении с СО, окисление железа гема ведет к увеличению аффинности остальных (неоксидированных) молекул гема к О2. То есть кривая связывания О2 частично метгемоглобинизированным Hb сдвинута влево. При помощи средств восстановления (например, дитионит) MetHb может опять восстановиться в гемоглобин (Fe3+ становится Fe2+). В организме восстановление MetHb, который возникает спонтанно или под действием ряда токсических соединений (например, нитраты, нитриты, анилинсодержащие вещества), обеспечивает метгемоглобинредуктаза. Особенно подвержены действию токсических соединений, образующих MetHb (например, питьевая вода с высокой концентрацией нитрата), грудные дети, так как у них MetHb-редуктаза еще недостаточно активна. Рис. 7-33. Влияние угарного газа на связывание гемоглобином О2 крови. Если построить кривую, отражающую половину кислородной емкости крови (что соответствует 50% анемии, голубая кривая) и затем ее значения умножить на 2, то кривая связывания в своей верхней части совпала бы с кривой, отражающей кислородную емкость крови, причем ее форма была бы нормальной. Напротив, связывание 50% гемоглобина с СО (50% HbCO, фиолетовая кривая) ведет также к делению пополам кислородной емкости крови. Но при этом форма кривой связывания сильно изменена (сдвиг влево), что затрудняет отдачу О2 в ткани
Факторы, влияющие на связывание кислорода гемоглобином Напомним, что существует ряд факторов, которые влияют на аффинность гемоглобина к О2, т.е. на насыщение гемоглобина кислородом при данном РО2. Характерно, что эти факторы смещают в ту или иную сторону (вправо или влево) саму кривую, но мало влияют на ее форму. Уменьшение аффинности приводит к сдвигу кривой связывания гемоглобином кислорода вправо, а увеличение аффинности приводит к сдвигу кривой связывания гемоглобином кислорода влево. Способность гемоглобина связывать и отдавать кислород изменяется в зависимости от температуры. Оксигемоглобин при одном и том же парциальном давлении кислорода в окружающей среде отдает больше кислорода при более высокой температуре тела, чем при более низкой (рис. 7-34 А). То есть повышение температуры приводит к понижению аффинности, что приводит к сдвигу кривой связывания вправо. На рис. 7-34 Б показаны смещения кривой в право и влево при различных респираторных нарушениях, которые вызывают изменения РСО2 и рН. Необходимо напомнить, что эффект Бора, может быть связан также с изменением РСО2 - повышение РСО2 сдвигает кривую связывания О2 вправо, понижение - влево, поскольку повышение РСО2 ведет к понижению рН и наоборот. Ниже будет показано, что уменьшение рН сдвигает кривую влево. Влияние самих молекул СО2 на аффинность гемоглобина к О2 является, напротив, незначительным. Далее мы можем рассмотреть изменение кривой в каждом отдельном случае. При неизменном РСО2 (40 мм рт.ст.) повышение концентрации ионов Н+2 (понижение рН) вызывает снижение аффинности гемоглобина к кислороду (сдвиг кривой вправо), понижение концентрации ионов Н+ вызывает повышение аффинности гемоглобина к кислороду (рис. 7-34 В). При неизменной рН (7,4) при повышении напряжения углекислого газа (при одном и том же парциальном давлении кислорода) происходит снижение аффинности гемоглобина к кислороду (сдвиг кривой вправо), т.е. при повышении напряжения углекислого газа образуется меньше оксигемоглобина (рис. 7-34 Г). Заметим, что резкое снижение способности гемоглобина связывать кислород в присутствии углекислого газа отмечается при парциальном давлении кислорода, равном 46 мм рт.ст., (при том его напряжении) которое имеется в венозной крови. Это свойство гемоглобина имеет важное значение для организма. В капиллярах тканей напряжение углекислого газа в крови увеличивается и потому уменьшается способность гемоглобина связывать кислород, что облегчает отдачу кислорода тканям. В альвеолах легких, где часть углекислого газа переходит в альвеолярный воздух, способность гемоглобина связывать кислород возрастает, т.е. увеличивается образование оксигемоглобина. Особенно резкое снижение способности гемоглобина связывать кислород отмечается в крови мышечных капилляров во время интенсивной мышечной работы, когда в кровь поступают кислые продукты обмена веществ, в частности молочная кислота. Это способствует отдаче большого количества кислорода мышцам. Рис. 7-34. Сдвиги сатурационной кривой О2 при ряде воздействий. А - эффекты респираторных нарушений, связанные с изменением рСО2 и рН. Б - сдвиги сатурационной кривой при изменения рН, но при неизменном рСО2. В - сдвиги сатурационной кривой при изменения рCO2, но при неизменном рН
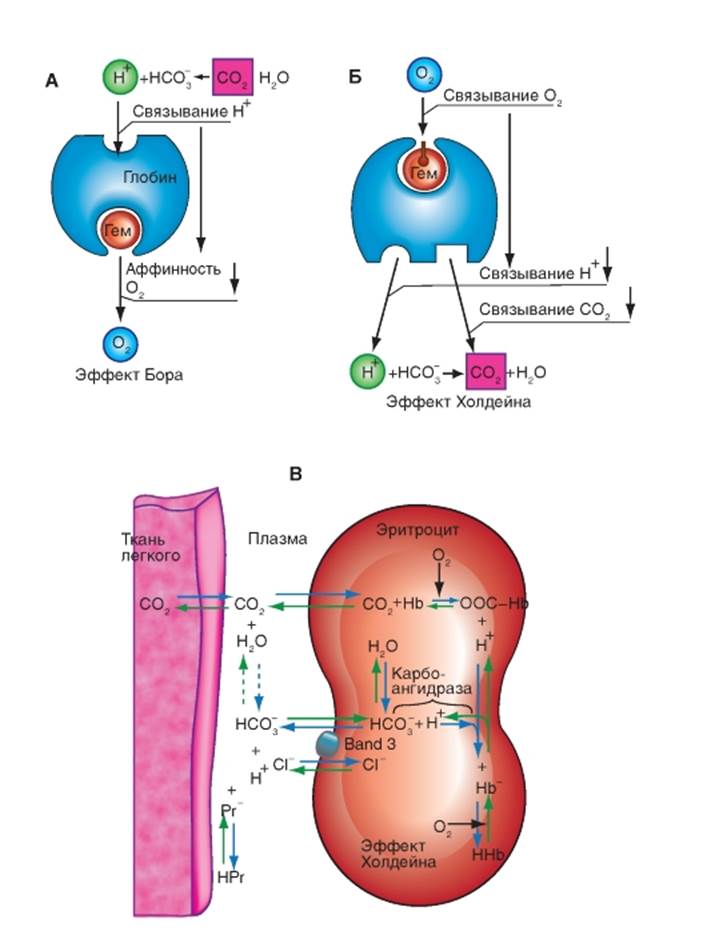
Связывание углекислого газа По аналогии с кривой связывания О2, кривая связывания СО2 описывает связь между концентрацией СО2 (все три формы: физически растворенный, в составе бикарбонатов и в соединении с белками) и парциальным давлением СО2 крови (рис. 7-35 А). При этом концентрация химически связанного СО2 (особенно НСО3-) несколько превышает его физически растворенную часть. В противоположность к кривой связывания О2, химически связанная часть СО2 не достигает, однако, «значения насыщения», т.е. не имеется «емкости СО2» крови. На кривую связывания СО2 оказывает влияние ряд факторов. Понижение рН или повышение температуры сдвигают кривую связывания вправо. При равном же РСО2 дезоксигенированная кровь связывает значительно больше СО2, чем оксигенированная (рис. 7-35 А). Этот феномен, известный как эффект Холдейна, основывается на одинаковом механизме с эффектом Бора, а именно на аллостерическом обмене на гемоглобине. При освобождении гемом места связывания кислорода происходит присоединение иона Н+ к его месту связывания на глобине (рис. 7-35 Б). Кроме того, часть карбамино-СО2 является зависимой от насыщения О2 (оксилабильное карбомат-связывание). Присоединение О2 уменьшает способность связывания СО2 в качестве карбомата. Как и эффект Бора, эффект Холдейна имеет большое физиологическое значение. Повышение парциального давления О2 в легком облегчает освобождение СО2 из химического связанного состояния и его переход в физически растворенное состояние. Концентрации НСО3- и карбомата понижаются, РСО2 повышается так, что СО2 может лучше диффундировать в альвеолярный воздух. Напротив, поступление О2 в ткани способствует увеличению связывания СО2 в крови. В условиях артериальной крови (рН = 7,4, РСО2 = 5,3 кПа) с помощью эффекта Холдейна при связывании 1 моля О2 освобождается 0,28 моль СО2. При RQ (отношение выделенного СО2 и поступившего О2), равном 0,85, на 1 моль О2 образуется 0,85 моль СО2. Как упоминалось выше, 0,28 моль есть 1/3 газа, освобождающегося через эффект Холдейна, не требующего изменения РСО2 в крови. Ну а2/3 освобожденного CO2 образуются в результате реакции с образованием угольной кислоты из диссоциированных ионов Н+ и НСО3-, которая превращается в СО2 и воду. Рис. 7-35. Связывание СО2. А - кривая связывания СО2 в крови человека. Общая концентрация СО2 составляется из физически растворенной и химически связанной части (HCO3-, карбамат). На основе эффекта Холдейна дезоксигенированная кровь связывает (насыщение О2, SO2 = 0%) больше СО2, чем оксигенированная кровь (SO2 = 100%). Физиологическая кривая связывания СО2, которая учитывает изменение SO2 в легких и тканях, проходит поэтому отвеснее, чем кривые связывания при постоянном SO2. Б - при эффекте Холдейна связывание гемма с О2 способствует отдаче глобином Н+ (буфер), что, в свою очередь, влияет на равновесие НСО3-и СО2. Дополнительно, влияет часть насыщения О2 (оксилабильное связывание карбомата) на связывание карбомата СО2. Дополнительно часть карбоматного соединения СО2 испытывает влияние от насыщения гемоглобина О2 (оксилабильное связывание карбомата)
Обмен СО2 Рисунок 7-36 демонстрирует процессы, которые происходят в крови, когда в тканях образуется СО2, который выделяется легкими. Из ткани СО2 диффундирует в плазму и, далее, в эритроциты. Из-за высокой диффузионной способности СО2 быстро происходит полное уравнивание парциального давления между эритроцитами и плазмой. Повышение РСО2 ведет к образованию НСО3-, а именно, в размере, в котором небикарбонатные буферы могут связывать ионы Н+, возникающие в результате реакции СО2 + Н2О ↔ НСО3- + Н+. Так как буферная емкость небикарбонатного буфера в эритроцитах (гемоглобин, около 60 ммоль • рН) много больше, чем буферная емкость белков плазмы (белки плазмы, около 8 ммоль • рН), в эритроцитах образуется больше НСО3-, чем в плазме. К этому надо добавить, что установление равновесия СО2 + Н2О ↔ НСО3- + Н+ в плазме протекает медленно. В эритроцитах, однако, имеется фермент карбоангидраза, которая значительно ускоряет эту реакцию, так что равновесие в эритроцитах достигается намного быстрее, чем в плазме. Поэтому концентрация НСО3- в эритроцитах повышается быстрее, чем в плазме, и возникает химический градиент НСО3-, вследствие чего НСО3- попадает из эритроцитов в плазму. Для сохранения электронейтральности из плаз- мы в эритроциты входят ионы Cl- с помощью электронейтрального обменника. Однако равновесие может быть достигнуто окончательно только тогда, когда и концентрация Н+ плазмы соответствует измененным значениям НСО3- и СО2. В этом установлении равновесия Н+ в меньшей степени участвует обмен Н+ или ОН- на мембране эритроцита, но в гораздо большей степени медленная реакция СО2 с Н2О в плазме с образование Н+ и НСО3- (рис. 7-36). По новым данным, эта реакция ускоряется посредством карбоангидразы, которая закреплена в эндотелии капилляров, но является доступной плазме (см. также внутриклеточная и мембраносвязанная карбоангидраза почек). Таким образом, в плазме одна часть СО2 реагирует с водой и это ведет к повышению концентрации Н+, т.е. способствует установлению его равновесия. Образовавшийся при этом НСО3- попадает опять в эритроциты и является источником там образования СО2. Этот круг событий (цикл Якоба-Стюарта) протекает в обратном направлении по сравнению с первичной последовательностью. На рис. 7-36 далее представлены реакция СО2 с карбоматом и связывание возникающих ионов Н+ с помощью буферных систем, а именно белков плазмы и гемоглобина, а также влияние эффекта Бора-Холдейна. В легком все эти этапы протекают в обратном направлении. Рис. 7-36. Процессы обмена СО2 в большом круге кровообращения
Эффекты Бора и Холдейна Эффект Холдейна, основывается на одинаковом механизме с эффектом Бора, а именно на аллостерическом обмене на гемоглобине. При освобождении гемом места связывания кислорода происходит присоединение иона Н+ к его месту связывания на глобине (рис. 7-37 А, Б). Кроме того, часть карбамино-СО2 является зависимой от насыщения О2 (оксилабильное карбомат-связывание). Присоединение О2 уменьшает способность связывания СО2 в качестве карбомата. Как и эффект Бора, также и эффект Холдейна имеет большое физиологическое значение. Повышение парциального давления О2 в легком облегчает освобождение СО2 из химического связанного состояния и его переход в физически растворенное состояние. Концентрации НСО3- и карбомата понижаются, РСО2 повышается так, что СО2 может лучше диффундировать в альвеолярный воздух. Напротив, поступление О2 в ткани способствует увеличению связывания СО2 в крови. В условиях артериальной крови (рН = 7,4, РСО2 = 5,3 кПа) с помощью эффекта Холдейна при связывании 1 моля О2 освобождается 0,28 моль СО2. При RQ (отношение выделенного СО2 и поступившего О2), равном 0.85, на 1 моль О2 образуются 0,85 моль СО2. Как упоминалось выше, 0,28 моль есть 1/3 газа, освобождающегося через эффект Холдейна, не требующего изменения РСО2 в крови. Ну а2/3 освобожденного CO2 образуются в результате реакции с образованием угольной кислоты из диссоциированных ионов Н+ и НСО3-, которая превращается в СО2 и воду. Рис. 7-37 В демонстрирует процессы, которые происходят в крови, когда в тканях образуется СО2, выделяемый затем легкими. Из ткани СО2 диффундирует в плазму и, далее, в эритроциты. Из-за высокой диффузионной способности СО2 быстро происходит полное уравнивание парциального давления между эритроцитами и плазмой. Повышение РСО2 ведет к образованию НСО3-, а именно в размере, в котором небикарбонатные буферы могут связывать ионы Н+, возникающие в результате реакции СО2 + Н2О ↔ НСО3- + Н+. Так как буферная емкость небикарбонатного буфера в эритроцитах (гемоглобин, около 60 ммоль • 1-1 • рН -1) много больше, чем буферная емкость белков плазмы (белки плазмы, около 8 ммоль • 1-1 • рН-1 в эритроцитах образуется больше НСО3-, чем в плазме. К этому надо добавить, что установление равновесия СО2 + Н2О ↔ НСО3- + Н+ в плазме протекает медленно. В эритроцитах, однако, имеется фермент карбоангидраза, которая значительно ускоряет эту реакцию, так что равновесие в эритроцитах достигается намного быстрее, чем в плазме (шаг 1-2). В целом, поэтому концентрация НСО3- в эритроцитах повышается быстрее, чем в плазме, и возникает химический градиент НСО3-, вследствие чего НСО3- попадает из эритроцитов в плазму. Для сохранения электронейтральности из плазмы в эритроциты входят ионы C1- с помощью электронейтрального обменника. Однако равновесие может быть достигнуто окончательно только тогда, если и концентрация Н+ плазмы соответствует измененным значениям НСО3- и СО2. В этом установлении равновесия Н+ в меньшей степени участвует обмен Н+ или ОН- на мембране эритроцита, но в гораздо большей степени медленная реакция СО2 с Н2О в плазме с образованием Н+ и НСО3-. По новым данным, эта реакция ускоряется посредством карбоангидразы, которая закреплена в эндотелии капилляров, но является доступной плазме. Таким образом, в плазме одна часть СО2 реагирует с водой и это ведет к повышению концентрации Н+, т.е. способствует установлению его равновесия. Образовавшийся при этом НСО3- попадает опять в эритроциты и является источником там образования СО2. Этот круг событий (цикл Якоба-Стюарта) протекает в обратном направлении по сравнению с первичной последовательностью. На рис. 7-37 В представлены реакция СО2 с карбоматом и связывание возникающих ионов Н+ с помощью буферных систем, а именно белков плазмы и гемоглобина, а также влияние эффекта Бора-Холдейна. В легком все эти этапы протекают в обратном направлении. Рис. 7-37. Принципы эффекта Бора (А) и эффекта Холдейна (Б). A - эффект Бора описывает влияние изменения концентрации ионов Н+, и тем самым, связывание Н+ с гемоглобином, на связывание гемом О2. Изменение концентрации СО2 влияет на изменение концентрации ионов Н+, которые, в свою очередь, при связывании с белком в виде карбомата влияют на аффинность гемма к О2. Б - при эффекте Холдейна связывание гема с О2 способствует отдаче глобином Н+ (буфер), что, в свою очередь, влияет на равновесие НСО3- и СО2. Дополнительно, влияет часть насыщения О2 (оксилабильное связывание карбомата) на связывание карбомата СО2. Дополнительно часть карбоматного соединения СО2 испытывает влияние от насыщения гемоглобина О2 (оксилабильное связывание карбамата). В - реакции при поступлении СО2 в кровь (ткани, голубые стрелки) и при выделении СО2 из крови (легкое, зеленые стрелки). Пунктирные стрелки в плазме означают, что установка в положение равновесия происходит медленно. Hb-СОО- = карбамат, ННb/Hb- указывает на буферные свойства гемоглобина. Транспортер Band-3 обеспечивает равный обмен НСО3- -С1-
Газообмен в большом круге кровообращения На рисунке представлен эритроцит, пришедший в большой круг кровообращения, плазма, в которой он находится, и ткань. Эритроцит принес в большой круг кровообращения О2 для обмена на СО2. В эритроците СО2 находится в виде КНbO2, т.е. в связанном с гемоглобином. Переход О2 из эритроцита в плазму и далее в ткань осуществляется по градиенту рО2, а переход СО2 в обратном направлении - по градиенту рСО2. При достижении артериальной кровью периферических тканей рО2 в ней находится на уровне 95 мм рт.ст. На рис. 7-38 видно, что в окружающей тканевые клетки интерстициальной жидкости рО2 достигает только 40 мм рт.ст. Таким образом, имеется большой градиент давления, под влиянием которого кислород начинает быструю диффузию из капиллярной крови в ткани - настолько быструю, что рО2 в капиллярах почти сравняется с рО2 (40 мм рт.ст.) в интерстиции, поэтому рО2 в крови, покидающей капилляры и поступающей в системные вены, составляет около 40 мм рт.ст. Величина рО2 ткани определяется равновесием между: (1) скоростью транспорта О2 кровью к ткани; (2) скоростью потребления О2 тканями. Клетки непрерывно потребляют О2. Следовательно, рО2 в клетках периферических тканей постоянно ниже, чем рО2 в периферических капиллярах, поэтому нормальное рО2 внутри клеток может оказаться как низким (5 мм рт.ст.), так и довольно высоким (40 мм рт.ст.) и в среднем (при прямом измерении у низших животных) составляет 23 мм рт.ст. Обычно для полного обеспечения кислородом клеточных процессов вполне достаточно рО2, равного 1-3 мм рт.ст. Кислород в клетках практически полностью превращается в двуокись углерода, в результате в клетке повышается рСО2. Из-за повышения рСО2 двуокись углерода диффундирует из клеток в тканевые капилляры и переносится кровью в легкие. В качестве примера рассмотрим градиент парциального давления СО2 в на уровне системы клетка - интерстициальная жидкость. В этом случае рСО2 внутри клетки равно 46 мм рт.ст., а рСО2 В интерстициальной ткани - 45 мм рт.ст. Таким образом, градиент составляет только 1 мм рт.ст. Как же далее СО2 попадает в эритроцит. В артериальной крови, пришедшей в большой круг кровообращения, рСО2 равно 40 мм рт.ст. Заметим также, что в плазме работает бикарбонатная буферная система. Рис. 7-38. Обмен газов в большом круге кровообращения
Газообмен в малом круге кровообращения На рис. 7-39 представлен эритроцит, пришедший в малый круг кровообращения, плазма, в которой он находится, и альвеола. Эритроцит принес в малый круг кровообращения СО2 для обмена на О2. В эритроците СО2 находится в двух состояниях. Первое - в виде HHbCO2, т.е. связанное с гемоглобином, и второе - KHCO3. Переход СО2 из эритроцита в плазму и далее в альвеолу осуществляется по градиенту рСО2, а переход О2 в обратном направлении - по градиенту рО2. На рис. 7-39 показана диффузия молекул О2 из альвеолярного воздуха в кровь. рО2 в альвеолярной газовой смеси составляет 104 мм рт.ст., а рО2в венозной крови, входящей в легочный капилляр через его артериальный конец, составляет только 40 мм рт.ст. (большое количество О2 было поглощено из крови во время прохождения ее через периферические ткани). Таким образом, разница рО2, являющаяся причиной диффузии кислорода в легочные капилляры, составляет 104 - 40 = 64 мм рт.ст. Очень быстро рО2 в крови составит около 104 мм рт.ст., т.е. почти достигает рО2 в альвеолярном воздухе. В целом, около 98% объема крови, входящей в левое предсердие после прохождения легких, прошло через легочные капилляры и было оксигенировано до рО2, равного приблизительно 104 мм рт.ст. После диффузии кислорода из альвеол в капиллярную кровь его дальнейший транспорт в капилляры периферических тканей совершается почти полностью в связанной с гемоглобином форме. Наличие в эритроцитах гемоглобина позволяет крови транспортировать в 30-100 раз больше кислорода, чем могло бы транспортироваться в виде газа, растворенного в водной со ставляющей крови. Ранее обсуждалось, что при достижении артериальной кровью периферических тканей рО2 в ней находится на уровне 95 мм рт.ст., т.е. кровь в аорте имеет рО2 примерно равное 95 мм рт.ст. Откуда же берется эта разница? Выше отмечалось, что около 98% объема крови, входящей в левое предсердие после прохождения легких, прошло через легочные капилляры и было оксигенировано до рО2, равного приблизительно 104 мм рт.ст. Но 2% объема крови ушли из аорты в бронхиальное кровообращение, которое снабжает в основном глубокие ткани легких, и не вошли в контакт с альвеолярным воздухом. Эту часть кровотока в легких называется «шунтирующей», поскольку она направляется мимо газообменных участков легких. На выходе из легких рО2 шунтированной крови находится примерно на уровне нормальной системной венозной крови - около 40 мм рт.ст. При смешивании этой крови (рО2 = 40 мм рт.ст.) в легочных венах с оксигенированной кровью (рО2 равно 104 мм рт.ст.) из альвеолярных капилляров, эта так называемая «венозная примесь» крови приведет к снижению рО2, входящей в левую половину сердца и выбрасываемой оттуда в аорту крови, примерно до 95 мм рт.ст. Кроме того, как показано на рис. 7-39, в плазме работает бикарбонатная буферная система. Рис. 7-39. Обмен газов в малом круге кровообращения
Диффузионная способность легких Между газовой средой в альвеолярном пространстве и кровью, протекающей в легочных капиллярах, находится альвеолярно-капиллярный барьер, включающий структуры альвеолярной и капиллярной стенок. Именно эту, хотя и очень тонкую стенку между газом в альвеолярном пространстве и кровью легочных капилляров, газы должны преодолеть путем диффузии. Эта стенка состоит из нескольких слоев: альвеолярного эпителия, интерстициума и капиллярного эндотелия. Необходимо отметить, что кроме диффузии через альвеолярно-капиллярный барьер, например, кислород на своем пути к гемоглобину, дополнительно должен проникнуть в плазму, пройти через мембрану эритроцитов и попасть во внутреннюю часть красных кровяных клеток. Так как реакция О2 с гемоглобином (а также реакция перехода от СО2 к НСО3-) протекает очень быстро, она незначительно ограничивает транспорт газа. Отсюда обоснованно рассматривать переход О2 и СО2 между альвеолами и эритроцитами в легочных капиллярах как диффузию, осуществляемую через объединяющий общий барьер в виде тканевого слоя и плазмы крови. Диффузионный поток (V) через альвеолярнокапиллярную мембрану пропорционален разности парциальных давлений (∆Р) между альвеолярным газом и капиллярной кровью легких:
Коэффициент пропорциональности DL называется диффузионной способностью легких. Он зависит, по закону диффузии Фика, от поверхности проникновения - площади (А) и толщины (х) мембраны, а также от растворимости (α) и от коэффициента диффузии (D) диффундирующего газа:
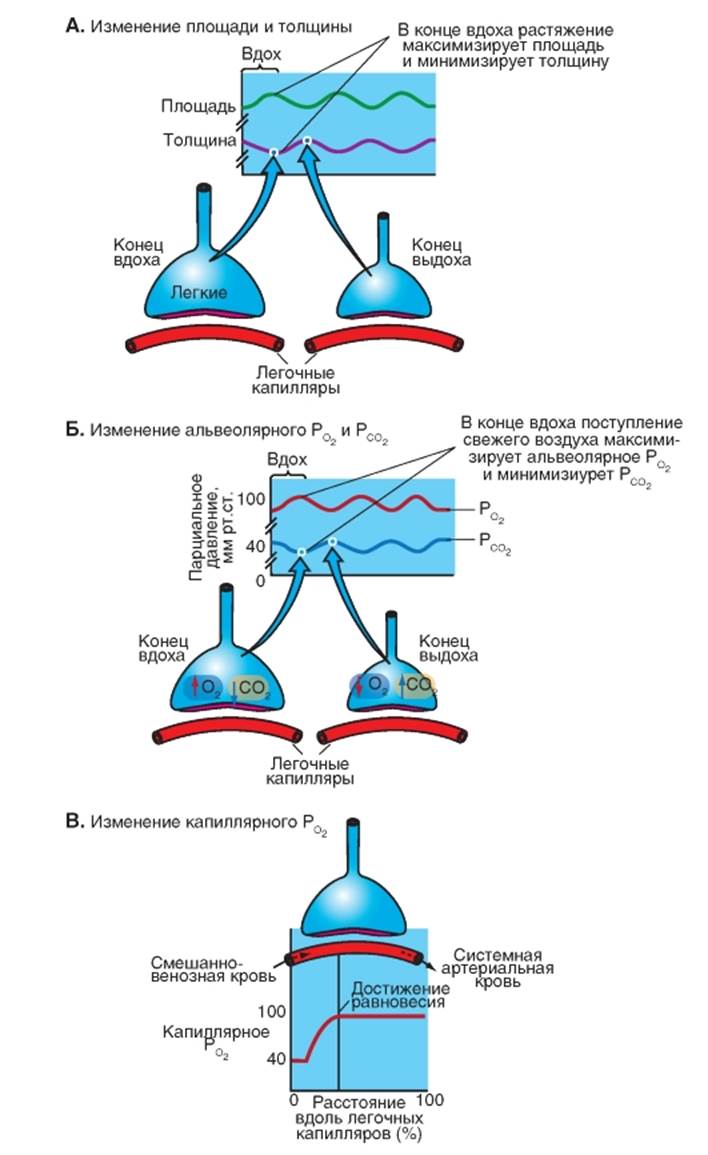
Произведение D • α обозначается как константа диффузии Крога (К). Геометрические факторы А и х in vivo можно оценить с крайне низкой степенью точности. Кроме того, толщина х в различных частях альвеолы весьма различна. Наконец, в процессе респираторного цикла толщина и площадь претерпевают изменения, как это показано на графиках (рис. 7-40 А). Так, в конце вдоха растяжение максимизирует площадь и минимизирует толщину; в конце выдоха - наоборот. Далее, нельзя легко измерить К и α, так как их значения в отдельных слоях альвеолярной мембраны могут быть совершенно различными. Во время респираторного цикла помимо площади и толщины меняются и два других параметра - РО2 и РСО2, как это показано на графиках (рис. 7-40 Б) - и эти изменения связаны с пространственными и временными свойствами. В конце вдоха поступление свежего воздуха максимизирует альвеолярное РО2 и минимизирует альвеолярное РСО2; в конце выдоха - наоборот. Наконец, обратим внимание на РО2 вдоль капилляра (рис. 7-40 В), которое претерпевает существенное изменение, показанное на графике в увеличенном размере. В начале капилляра «поддерживаемая» разность давления является высокой, и большое количество О2 диффундирует через альвеолярно-капиллярную мембрану. Благодаря поступлению О2 в кровь увеличивается РО2 вдоль капилляра, вследствие чего «поддерживаемая» разность давления и диффузионный поток снижаются. Конечно-капиллярная артериальная кровь, которая покидает капилляр, имеет практически то же самое РО2 (и РСО2), как альвеолярный воздух. Кривая капиллярного уравнения РО2проходит в нормальных условиях более отвесно, чем на представленном для пояснения рисунке. Усредненная альвеолярно-капиллярная разность РО2 в норме равна примерно 1 кПа. Это является причиной того, почему все эти факторы обобщают в глобальную, но измеримую величину диффузионной способности легких DL. Но кислород должен диффундировать не только через альвеолярную мембрану, а также еще через слой в крови, пока он не достигнет гемоглобина. Как правило, значение DL включает также диффузию в крови и определяется, таким образом, еще и диффузионными свойствами крови. Рис. 7-40. Закон Фика и сложность его использования. А - изменение площади и толщины. Б - изменение альвеолярного РО2 и РСО2. В - изменение капиллярного ро2
Диффузия кислорода в легких На рис. 7-41 А продемонстрировано поступление О2 из альвеолярного воздуха в кровь легочных капилляров. В верхней части рис. 7-41 А изображена альвеола, расположенная рядом с легочным капилляром, и показана диффузия молекул кислорода из альвеолярного воздуха в кровь. РО2 в альвеолярной газовой смеси составляет 104 мм рт.ст., а РО2 в венозной крови, входящей в легочный капилляр через его артериальный конец, составляет только 40 мм рт.ст., так как большое количество кислорода было поглощено из крови во время прохождения ее через периферические ткани. Таким образом, начальная разница в парциальном давлении, являющаяся причиной диффузии кислорода в легочные капилляры, составляет 104-40, или 64 мм рт.ст. На графике рис. 7-41 Б виден резкий подъем РО2 крови во время прохождения ее через капилляр; к моменту прохождения 1/3 длины капилляра РО2 в крови составляет около 104 мм рт.ст., т.е. почти достигает РО2 в альвеолярном воздухе. При контакте с альвеолярной мембраной кровь в капиллярах легких непрерывно получает О2, вследствие чего парциальное давление О2 вдоль капиллярной контактной поверхности от смешено-венозного исходного значения (РО2) в начале капилляра (альвеолярно-начально-капиллярное РО2) повышается до более высокого значению в конце капилляра. Это РО2 крови в конце капилляра (альвеолярно-конечно-капиллярное РО2 или Рс'О2) в нормальном легком при дыхании воздухом является практически одинаковым с альвеолярным РО2 (Рао2), так как диффузионная способность нормального легкого так высока, что альвеолярная мембрана в покое не представляет собой диффузионного препятствия для О2 (так же, как и для СО2). Поэтому в норме, уже в первой трети капилляра РО2становится равным РАО2. (рис. 7-41 Б). Только при сильно повышенном поступлении О2 (например, при тяжелой физической работе: рис. 7-41 В) или в условиях гипоксии (рис. 7-41 Г) можно констатировать незначительный диффузионный лимит для О2. При глубокой гипоксии диффузионный лимит может стать значительным, так как кривая связывания О2 в гипоксической области РО2 имеет вертикальный характер при поступлении О2 РО2вдоль легочных капилляров мало меняется, так что остается большая разность между РАо2 и Рс'О2. Как показывает рисунок разность давления ∆РО2 меняется вдоль капилляра. Среднее значение при расчете DL для О2 по уравнению является, отсюда, сложно измеряемым. Особыми методами определили DL для О2 у здорового легкого, и ее величина приблизительно равна 275 мл/мин • кПа. При поступлении О2 в покое = 310 мл/мин. С учетом этой величины и уравнения 10,46 средняя разность альвеолярнокапиллярного РО2приблизительно равна 1,1 кПа (8 мм рт.ст.). Хотя в отдельной альвеоле альвеолярный газ и кровь в конце капилляра (альвеолярно-конечнокапиллярная кровь) имеют практически одинаковые значения РО2 и значения РСО2, из-за вентиляционно-перфузионной неравномерности легкого имеются отчетливо измеряемые различия РО2 между смешанно-альвеолярным газом и артериальной кровью, которая смешивается из альвеолярноконечно-капиллярной крови, то есть крови, оттекающей от всех альвеол легкого. Уравнение
показывает, однако, как DL ведет себя по отношению к различным газам. Т
|
|||||||||||||||||
|
Последнее изменение этой страницы: 2016-04-20; просмотров: 983; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.214 (0.012 с.) |