

Мы поможем в написании ваших работ!
ЗНАЕТЕ ЛИ ВЫ?
|
Механизм спонтанного дыхания
Содержание книги
- Рецепторная и рефлекторная функция ганглиев.
- Метасимпатическая нервная система
- Механизм саморегуляции выделения медиатора в синапсах вегетативной нервной системы
- Рефлекторная функция спинного мозга
- Проводниковая функция спинного мозга
- Спинальные механизмы регуляции мышечного тонуса и фазных движений.
- Клинически важные спинальные рефлексы
- Рефлекторная функция продолговатого мозга.
- Рефлекторная функция продолговатого мозга. Бульбарные механизмы поддержания позы человека.
- Структурно-функциональная организация и физиологические функции среднего мозга и моста (сенсорные, проводниковые, моторные, вегетативные, интегративные, рефлекторные).
- Современные представления о влиянии РФ.
- Структурно-функциональная организация лимбической системы. Ее роль в формировании мотиваций, эмоций, организации памяти. Участие лимбических структур в интегративной деятельности цнс.
- Проводниковый отдел и принципы его построения.
- Основные функции анализаторов
- Основные формы нарушения цветового восприятия.
- Механизм работы вестибулярного анализатора
- Внимание, его нейрофизиологические механизмы. Роль внимания в процессах запоминания и обучения.
- Нейроструктурные предпосылки мышления
- Механизмы долговременной памяти
- Функциональная асимметрия полушарий головного мозга и ее роль в реализации психических функций
- Механизмы возрастания минутного объёма дыхания при физической нагрузке. Причины развития дыхательного алкалоза при тяжёлой мышечной работе.
- Чем представлен дыхательный аппарат у человека? Респираторные и нереспираторные функции воздухопроводящих путей и легких.
- Перечислите этапы биомеханики вдоха. Назовите виды давления в грудной полости и их роль в биомеханике вдоха и выдоха?
- Специфические регуляторы дыхания: опишите зависимость минутного объёма дыхания от рН ликвора, рО2 в крови. Опыт Фредерика.
- Работа дыхательных мышц и её зависимость от сопротивления дыханию. Виды сопротивления. Что такое предел дыхания?
- Механизм спонтанного дыхания
- Периоды рефрактерности сердца
- Резус-фактор, физиологическая роль. Физиологические основы переливания крови. Основные правила переливания крови. Гемотрансфузионный шок.
- ФУС, обеспечивающая поддержание постоянства уровня питательных веществ в крови.
- Пищеварение в полости рта. Состав и пищеварительные свойства слюны. Регуляция секреторной функции слюнных желез.
- Пищеварение в желудке. Состав и пищеварительные свойства желудочного сока. Фазы желудочной секреции. Механизмы регуляции желудочной секреции.
- Состав и пищеварительное действие поджелудочного сока. Регуляция панкреатической секреции.
- Моторная функция желудка, тонкого и толстого кишечника. Физиологические особенности и значение .
- Механизмы всасывания. Виды всасывания. Виды транспорта веществ через мембрану. Особенности всасывания углеводов, белков, жиров.
- Участие почек в поддержании кислотно-основного равновесия крови.
- Строение нефрона. Кровообращение в почке, его особенности.
- Реабсорбция в почечных канальцах. Виды реабсорбции. Механизмы реабсорбции. Пороговые вещества. Регуляция реабсорбции.
- Температурное «ядро» и «оболочка». Методы измерения температуры тела. Количество тепловой энергии, вырабатываемой в сутки в организме теплокровного животного, механизмы её распределения в организме.
- Способы отдачи тепла (теплопроведение, конвекция, излучение, испарение). Внутренний и наружный потоки энергии. Регуляция теплоотдачи.
- Терморегуляция. Понятие о гипотермии и гипертермии.
- Механизмы адаптации к теплу и холоду.
- Учёт расхода энергии в организме. Прямая и непрямая калориметрия.
- Методы прямой и непрямой калориметрии.
- Основной обмен, величина и факторы, его определяющие. Правило поверхности тела.
- Рабочий обмен. Группы людей по энергозатратам. Специфически-динамическое действие питательных веществ.
- Основные системы питания, теории рационального питания. Значение белков, жиров, углеводов.
- Физиологические нормы питания. Понятие о белковом минимуме и белковом оптимуме. Нормы углеводов и жиров для человека. Соотношение питательных веществ в пищевом рационе.
- Методы изучения желез внутренней секреции
- Нейросекреты гипоталамуса. Либерины и статины.
- Тиреоидные гормоны и их эффекты.
Неврологический механизм, лежащий в основе рефлекса Геринга Брейера, сложен и является ярким примером тормозной обратной связи. У взрослых людей рефлекс начинается с продолжительного вдоха, значительно превышающего эупнейский приливный объем. Это грудное расширение впоследствии и постепенно активируется, медленно адаптируя легочные рецепторы растяжения. Эти рецепторы передают сигнал через блуждающий нерв (дыхание за дыханием) к "насосным " клеткам, расположенным в вентролатеральном ядре солитарного тракта. Эти насосные клетки получают эти вагусные входы и проецируют информацию на медуллярные постинспираторные нейроны. Эти нейроны впоследствии проецируют тормозные сигналы обратно к инспираторным нейронам вдоль боковой части дыхательного столба, тем самым прекращая вдох и начиная длительный выдох.
19.Физико-химические механизмы транспорта кислорода кровью. Значение эритроцитов в этом процессе. Кислородная ёмкость крови и процент насыщения артериальной и венозной крови кислородом. Коэффициент утилизации кислорода, его значение при различных функциональных состояниях организма, зависимость от уровня метаболизма в тканях. Оксигемометрия и оксигемография.
Газы транспортируются кровью в физически растворенном и химически связанном
Общее содержание газов в крови (об.%)
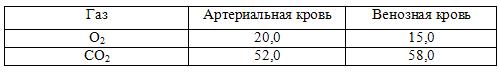
Содержание физически растворённого газа в жидкости описывается законом Генри-Дальтона.
[газ] = Рr × α / 760,
где Рr - напряжение газа в жидкости,
α- коэффициент растворимости Бунзена.
В знаменателе стоит 760, т.к. при определении α в качестве единиц давления используют атмосферы, а Рr выражают в мм рт.ст.
В артериальной крови содержание физически растворенного О2 составляет 0,3 об.%, а СО2 – 2,6 об.%, в венозной – 0,11 и 2,9 об.% соответственно. Несмотря на то, что напряжение О2 в артериальной крови 96 мм рт. ст., а напряжение СО2 43 мм рт. ст., содержание физически растворённого СО2 выше. Это объясняется большей растворимостью этого газа.
Следовательно, лишь небольшая часть О2 и СО2 находится в крови в физически растворённом виде. Но это состояние играет огромную физиологическую роль, так как во-первых, именно эта форма является функционально активной, т.е. способной диффундировать к тем или иным веществам для последующего связывания, а во-вторых, от содержания в крови физически растворенного газа зависит скорость реакций его химического связывания, которые подчиняются закону действующих масс.
Связывание О2
97% О2, транспортирующегося от легких к тканям, химически связано с гемоглобином.
Молекула гемоглобина состоит из 4 субъединиц, поэтому реакция оксигенации протекает следующим образом: Hb + 4О2 = Hb(О2)4. Молекула О2 обратимо связывается с гемом гемоглобина. Каждый грамм гемоглобина может связать 1,34 мл О2 (число Хюфнера) (1,39 мл, если гемоглобин химически чистый). Следовательно, при содержании гемоглобина в 1 л крови 140 г в этом объеме будет находиться (без учета физически растворённого О2) 1,34×140 = 190 мл О2, т.е. 19 об.%. Количество О2, которое вообще способна связать кровь, называется кислородной ёмкостью крови (в среднем 20 об.%). Реализуется полностью, если кровь контактирует с газовой смесью с высоким содержанием О2 (РО2 > 300 мм рт. ст.). В естественных условиях гемоглобин оксигенирован только на 97%.
Насыщением (saturation) гемоглобина кислородом называется процентное отношение HbО2 к общему содержанию гемоглобина.
SО2 = [HbО2] / [Hb]+[HbО2]
Реакция оксигенации гемоглобина, как указывалось, подчиняется закону действующих масс. Это означает, что отношение между гемоглобином и HbО2зависит от содержания физически растворенного О2 в крови, которое, в свою очередь, в соответствии с законом Генри-Дальтона, пропорционально напряжению О2. Графически эту зависимость отражает кривая диссоциации оксигемоглобина (КДО).
Еще в 1904 г. С.Bohr установил, что характер реакции гемоглобина с О2 описывается S-образной кривой.
На кривой выделяют 3 участка: от 0 до 10 мм рт. ст. – прямо пропорциональная зависимость, от 10 до 60 – насыщение очень быстрое, от 60 до 90 – насыщение почти не изменяется. В артериальной крови (напряжение О2 96 мм рт. ст.) гемоглобин насыщен кислородом на 97%, в венозной крови (напряжение О2 40 мм рт. ст.) – на 75%.
В настоящее время принято оценивать положение КДО не по наклону кривой, а по расположению на ней двух точек. Первая соответствует 50%-ому насыщению гемоглобина кислородом. Это Р50 – напряжение полунасыщения (точка разрядки по Крогу). В норме при рН = 7,4 и t = 37оС Р50 артериальной крови 26 мм рт. ст. (3,46 кПа). Оно выше у женщин, чем у мужчин. Напряжение разрядки достаточно высоко, что обеспечивает эффективный градиент напряжения О2 между капиллярами и тканями, где напряжение О2 не более 10-15 мм рт.ст. Вторая точка – Р95 – точка зарядки – соответствует 95%-ому насыщению гемоглобина кислородом. В норме Р95 артериальной крови 70 мм рт. ст.
Количество потребленного О2 в процентах от его содержания в артериальной крови называют коэффициентом утилизации кислорода (КУК). В норме он равен 25%, после физической нагрузки может достигать 75-85%. В локальных участках тканей, где ток крови чрезвычайно медленный или очень высока скорость метаболизма, КУК может возрастать до 100%, т.е. из крови будет поглощаться весь кислород.
Факторы, влияющие на величину КУК:
1. Количество функционирующих капилляров, их геометрия, скорость кровотока.
2. рН, температура и другие факторы, влияющие на диссоциацию HbO2.
Оксигемометрия — фотометрический метод измерения степени насыщения артериальной крови кислородом, основанный на спектральных свойствах оксигемоглобина и восстановленного гемоглобина. Для оксигемометрии пользуются специальными приборами — оксигемометрами, построенными на принципах фотоэлемента.
20. Классификация типов вентиляции легких в зависимости от парциального давления газов в альвеолярной газовой смеси.
1.Нормовентиляция – вентиляция, при которой парциальное давление углекислого газа в альвеолярной смеси газов близко к 40 мм рт. ст.
2. Гипервентиляция – усиленная по сравнению с метаболическими потребностями организма вентиляция, приводящая к «вымыванию» углекислого газа из альвеолярной газовой смеси, в результате чего его парциальное давление становится ниже 40 мм рт. ст.
3. Гиповентиляция – сниженная по отношению к метаболическим потребностям организма вентиляция, при которой парциальное давление углекислого газа в альвеолах увеличивается свыше 40 мм рт. ст.
4. Повышенная вентиляция – любое возрастание вентиляции, независимо от парциального давления углекислого газа в альвеолярной смеси газов.
5. Эупноэ (eu, греч. – хорошо, правильно, pnoe, греч. – дыхание) – нормальная вентиляция в покое, сопровождающаяся субъективным ощущением комфорта.
6. Гиперпноэ (hyper, греч. – чрезмерное повышение) – увеличение глубины дыхания, независимо от его частоты.
7. Тахипноэ (tachys, греч. – скорый, быстрый) – возрастание частоты дыхания.
8. Брадипноэ (bradys, греч. – медленный) – урежение дыхания.
9. Апноэ (а, греч. – отсутствие чего-либо) – остановка дыхания в результате отсутствия физиологической стимуляции дыхательного центра при снижении напряжения углекислого газа в артериальной крови.
10. Диспноэ (dys,греч. – расстройство) – неприятное субъективное ощущение недостаточности или затрудненности дыхания (одышка).
11. Ортопноэ (orthos, греч. – прямой) – выраженная одышка, обусловленная застоем крови в капиллярах легких в результате недостаточности левого сердца. Усугубляется в горизонтальном положении.
12. Асфиксия (asphyxia, греч. – удушье) – остановка дыхания, обусловленная, главным образом, параличом дыхательного центра и приводящая к гипоксии (недостаточному снабжению тканей кислородом) и гиперкапнии (повышению напряжения углекислого газа в крови).
21.Газообмен в тканях. Градиент напряжений О2 и СО2 между различными тканями и кровью капилляров и его значение в тканевом газообмене. Факторы, влияющие на коэффициент утилизации кислорода.
Обмен газов в тканях
Этот процесс происходит путём диффузии и подчиняется её законам.
Обмен О2.
Молекулы О2 диффундируют в сторону более низких величин напряжения этого газа: из капилляров (рО2 = 96 мм рт. ст.) в межклеточную жидкость (рО2 = 20-40 мм рт. ст.), затем в клетки.
Наименьшее напряжение О2 в клетках наблюдается в местах его потребления – митохондриях, где он используется для биологического окисления.
В результате отдачи О2 тканям его количество в крови постепенно уменьшается. Поэтому скорость этого процесса больше в артериальном конце капилляра, чем в венозном. Зная число Хюфнера (1,34) и степень насыщения гемоглобина кислородом (SО2) в артериальном и венозном концах капилляра, можно рассчитать объемное содержание О2 в крови:
О2 = 1,34 × [Hb] × SO2 × 10-5
где SO2 выражается в %,
[Hb ] в г/л.
Количество потребленного О2 в процентах от его содержания в артериальной крови называют коэффициентом утилизации кислорода (КУК). В норме он равен 25%, после физической нагрузки может достигать 75-85%.
Факторы, влияющие на величину КУК:
1. Количество функционирующих капилляров, их геометрия, скорость кровотока.
2. рН, температура и другие факторы, влияющие на диссоциацию HbO2.
Обмен СО2.
Наибольшее напряжение СО2 (до 60 мм рт. ст.) отмечается в клетках в результате образования этого газа в митохондриях. В тканевой жидкости напряжение СО2 изменчиво, около 46 мм рт. ст. В артериальной крови напряжение этого газа составляет 40 мм рт. ст. По градиенту напряжений СО2 диффундирует из клеток в кровеносные капилляры и транспортируется кровью к легким.
Таким образом, адекватное поступление О2 в ткани и удаление из них СО2 происходит в результате взаимодействия крови, дыхательной и сердечно-сосудистой систем.
22.Транспорт кровью углекислого газа. Физико-химические механизмы его связывания. Ёмкость артериальной и венозной крови для углекислого газа. Роль эритроцитов и карбоангидразы в его транспорте. Эффект Вериго-Холдена.
Механизмы, отвечающие за транспорт СО2, должны одновременно обеспечивать поддержание кислотно-щелочного равновесия крови и, тем самым, внутренней cреды организма.
I. Прежде всего происходит гидратация молекул СО2 с образованием Н2СО3
СО2 + Н2О → Н2СО3
В плазме эта реакция протекает очень медленно. В эритроцитах она ускоряется в 20 тысяч раз, что связано с действием карбоангидразы – фермента, расположенного только внутри клеток. Его существование предполагал еще И.М.Сеченов, но открыт он был в 1932 г. Мелдрумом и Рэфтоном.
Следующая реакция в цепи химических превращений СО2 заключается в диссоциации слабой кислоты Н2СО3 на бикарбонат-ионы и протоны
Н2СО3 → НСО3- + Н+
Накопление НСО3- в эритроцитах приводит к тому, что между их внутренней средой и плазмой крови создается градиент концентрации этого иона. НСО3-могут передвигаться по этому градиенту лишь в том случае, если при этом не будет нарушаться равновесное распределение электрических зарядов. Взамен НСО3- в эритроциты поступает Cl-. Этот обменный процесс называется хлоридным сдвигом Хамбургера. Накопление анионов внутри эритроцитов приводит к повышению осмотического давления, что вызывает поступление в них воды. В результате этого объем эритроцитов в венозной крови больше, чем в артериальной. Поэтому эритроциты занимают 40% объема артериальной крови и 40,4% - венозной. Образующиеся при реакции диссоциации Н2СО3 протоны рН не изменяют, поскольку гемоглобин, будучи амфолитом, обладает значительной буферной емкостью. Кроме того, восстановленный гемоглобин является более слабой кислотой, чем оксигемоглобин, поэтому может присоединять дополнительное количество Н+.
HbO2-→ O2↑ + Hb-→ HНb ← H+
II. Второй способ связывания СО2 – непосредственное его присоединение к аминогруппам белкового компонента гемоглобина за счет образования карбаминовой связи.
HbNH2 + CO2 → HbNHCOO- + H+ (реакция Рэфтона)
Соединение гемоглобина с СО2 называют карбаминогемоглобином.
В 1892 г. Вериго было установлено, что емкость для СО2 крови, содержащей восстановленный гемоглобин, значительно выше, чем в условиях полной оксигенации гемоглобина. Это явление, затем подробно изученное Холденом (1914), обусловлено тем, что, во-первых, оксигемоглобин является более сильной кислотой, чем восстановленный гемоглобин, и, следовательно, когда реакция происходит между КНbO2 и Н2СО3, равновесие наступает при образовании меньшего объема КНСО3, чем в случае, когда реакция течет между КНb и Н2СО3. Во-вторых, оксигенация гемоглобина ведет к снижению образования карбаминогемоглобина, поскольку уменьшает количество свободных NH2 групп глобина, способных связывать СО2. Следовательно, степень оксигенации гемоглобина влияет на способность крови связывать СО2. Это явление получило название эффекта Вериго-Холдена.
Соотношение между фракциями СО2 в крови. Каждый миллилитр крови, протекая через ткани, захватывает примерно 2 мМоль СО2. 10% этого количества остается в физически растворенном виде, 10% образует карбаминовую связь с гемоглобином, 35% транспортируется в виде бикарбонатов калия в эритроцитах, а остальные 45% – в виде бикарбонатов натрия в плазме. При прохождении крови через легкие СО2 выделяется из этих фракций точно в таком же соотношении.
Карбоангидраза содержится в эритроцитах, в плазме крови ее нет. соответственно — процесс соединение углекислого газа с водой происходит практически только в эритроцитах. Но это процесс обратимый, который может изменять свое направление. В зависимости от концентрации углекислого газа карбоангидраза катализирует как образование угольной кислоты, так и расщепление ее на углекислый газ и воду.
23.Функциональная система, поддерживающая оптимальное содержание газов в крови и тканях. Перечислить звенья ФУС, описать уровни нервного центра и их роль в регуляции дыхания. Дыхательный центр по Миславскому (расположение, классификация нейронов, особенности автоматии).
Первое звено – полезный приспособительный результат. Им является поддержание оптимального уровня показателей газового гомеостаза в тканях – напряжения кислорода и углекислого газа.
Второе звено – рецепторы. Изменения показателей газового гомеостаза воспринимаются хеморецепторами. Их подразделяют на центральные и периферические.
Периферические хеморецепторы расположены в стенках сосудов и в тканях.
Центральные (медуллярные) хеморецепторы. На их существование указывает классический опыт французского исследователя Л. Фредерика (1882) с перекрестным кровообращением. Рецепторы находятся на вентральной поверхности продолговатого мозга латеральнее пирамид (около корешков блуждающего и подъязычного нервов) на глубине не более 0,2 мм вблизи дыхательного центра, нейроны которого лежат глубже. Поэтому центральные хеморецепторы образно называют «контролер под боком у центра». Они образуют два рецептивных поля - M и L, между которыми расположено небольшое поле S. Рецепторы полей M и L возбуждаются при уменьшении рН межклеточной жидкости мозга. Рецепторы поля S не чувствуют изменения рН. Однако они необходимы для реализации эффектов возбуждения полей M и L, которые исчезают при разрушении поля S.
Центральные хеморецепторы не реагируют на гипоксию. Это доказывается тем, что после денервации периферических хеморецепторов этот фактор не оказывает стимулирующего влияния на дыхание.
Третье звено – дыхательный центр. Это совокупность нейронов, расположенных на разных уровнях центральной нервной системы, обеспечивающих соответствие дыхания изменяющимся метаболическим запросам организма. Дыхательный центр находится в ретикулярной формации в области дна IV желудочка и является парным, при этом каждая его половина иннервирует дыхательные мышцы ипсилатеральной (той же) стороны тела. Н.А.Миславский также показал, что дыхательный центр состоит из центра вдоха и центра выдоха. Однако, в 1956 г. Баумгартен доказал, что четкой границы между этими центрами не существует, но имеются участки, где расположены преимущественно инспираторные и экспираторные нейроны. В 1923 г. Лумсден, а затем и другие исследователи установили, что дыхательный центр имеет более сложную организацию – в его состав также входят структуры, расположенные в верхней части варолиевого моста.
Согласно современным представлениям (на основании результатов перерезки центральной нервной системы на различных уровнях, разрушения и раздражения локальных участков мозга, регистрации потенциалов действия отдельных нейронов с помощью микроэлектродов), различают следующие уровни дыхательного центра:
1. Спинальный – мотонейроны, аксоны которых иннервируют диафрагму (расположены в передних рогах серого вещества спинного мозга на уровне С III-V), межреберные мышцы и мышцы живота (на уровне Th I-XII). Этот отдел дыхательного центра получает нисходящие влияния по ретикулоспинальному тракту. Самостоятельного значения не имеет. Роль его заключается в изменениии силы сокращения мышц-респираторов в зависимости от сопротивления дыханию.
2. Бульбопонтинный (центральный дыхательный механизм) – структуры продолговатого мозга и варолиевого моста. После перерезки мозга между этими отделами дыхание, хотя и измененное, сохраняется. Это указывает на то, что важнейшие структуры дыхательного центра находятся в продолговатом мозге и обладают автоматией – непрерывной спонтанной ритмической импульсной активностью (это свойственно только инспираторным нейронам). Автоматия дыхательного центра отличается от автоматии проводящей системы сердца тем, что: 1) существенно зависит от взаимодействия многих нейронов, важное значение среди которых имеют тормозные; 2) поддерживается тонической специфической импульсацией (от хеморецепторов) и неспецифической (от множества других рецепторов, поступающей по коллатералям проводниковых путей в ретикулярную формацию, а от нее – к дыхательному центру). Тонус ретикулярной формации, определяющий «фон» работы мозга, заставляет «бодрствовать» и дыхательный центр. Поэтому после обширной деафферентации (прерывания потока импульсов от внутренних органов и сосудов) у новорожденного животного происходит постепенное, в течение 30 минут, угасание автоматии (Сергиевский, Широкий, 1961). Этот уровень дыхательного центра обеспечивает регуляцию дыхания в покое.
3. Гипоталамо-лимбико-ретикулярные структуры и кора больших полушарий. Значение этих структур в обеспечении соответствия дыхания метаболическим запросам организма доказывается тем, что после перерезки мозгового ствола между средним мозгом и мостом у животных существенно нарушается дыхание при нагрузке. Указанный уровень обеспечивает регуляцию дыхания в состоянии физического или эмоционального напряжения. При этом он осуществляет интеграцию дыхания с соматическими компонентами поведенческих актов (гипоталамус) и произвольную регуляцию дыхания (кора).
Центры гипоталамуса стимулируют инспираторные нейроны бульбарного отдела дыхательного центра, что приводит к усилению дыхания в условиях общей защитной реакции организма (при болевых воздействиях, физической работе, эмоциональном возбуждении), а также к увеличению его частоты при повышении температуры тела (тепловая одышка).
Электрическая стимуляция лимбической системы переднего мозга угнетает дыхание.
Кора больших полушарий влияет на деятельность бульбарного отдела дыхательного центра либо прямо (через кортико-бульбарные пути), либо опосредованно (через подкорковые структуры – стриопаллидарную и лимбическую системы, гипоталамус, ретикулярную формацию). В коре нет участков, специфически регулирующих дыхание, поскольку его изменения возникают при раздражении множества областей коры. Однако, они наиболее выражены при раздражении соматосенсорной и орбитальной зон.
Кора обеспечивает наиболее тонкое приспособление дыхания к изменяющимся условиям существования. Это достигается за счет образования условных рефлексов. Впервые условные дыхательные рефлексы были выработаны В.М.Бехтеревым и В.П.Протопоповым. Примером их может служить увеличение вентиляции легких на стук метронома после нескольких его сочетаний с вдыханием воздуха с повышенным содержанием углекислого газа (Г.П.Конради). В естественных условиях выработка таких рефлексов происходит в процессе тренировок. Значение условнорефлекторной регуляции заключается в том, что вызванные ею изменения дыхания опережают возможные сдвиги показателей газового гомеостаза, т.е. имеют упреждающий характер. В результате газовые параметры заранее соответствуют будущим метаболическим потребностям организма. Это регуляция дыхания не по отклонению регулируемого параметра от нормального уровня, а по возмущению. Под последним понимают выведение организма из состояния физиологического покоя. Регуляция по возмущению более точна и оперативна, чем по отклонению.
С участием коры связаны следующие особенности регуляции дыхания у человека.
1. Возможность произвольного управления дыханием. Это необходимо во время речи, пения, игры на духовых инструментах и др.
2. Относительная независимость дыхательного центра от сигналов, поступающих от хеморецепторов сосудов и механорецепторов легких. Поэтому после гипервентиляции у человека не наступает апноэ, а блокада проведения импульсов по блуждающему нерву, имеющему важную роль в регуляции дыхания, не приводит к брадипноэ.
3. Возможности субъективной оценки газового состава крови и состояния дыхательных путей.
4. «Самообучение» системы регуляции дыхания – по мере тренировок условные дыхательные рефлексы становятся более точными, т.е. совершенствуется регуляция дыхания по возмущению. У нетренированных людей любая нагрузка вызывает, как правило, гипервентиляцию. С возрастанием степени тренированности последняя исчезает.
5. Зависимость дыхания от активности коры. С одной стороны, ослабление тонических кортикальных влияний (во время сна, при закрытии глаз) приводит к снижению вентиляции легких. С другой стороны, интеллектуальная деятельность сопровождается учащением дыхания. Стресс вызывает и учащение, и углубление дыхания.
6. Значительная индивидуальная вариабельность. По отношению чувствительности разных людей к углекислому газу выделяют гипо- и гипервентиляторов.
Четвертое звено – исполнительные органы. Различают три контура:
1) внешний;
2) внутренний;
3) поведенческий.
Внешний – регулирует потребление кислорода из окружающей среды и выделение в нее углекислого газа за счет изменения глубины и частоты вентиляции легких. Имеет основное значение. Его полезный приспособительный результат – постоянство состава альвеолярной смеси газов.
Внутренний – включается при длительной произвольной задержке дыхания или при дыхании воздухом со сниженным содержанием кислорода. Поддерживает газовый гомеостаз весьма ограниченное время за счет внутренних, генетически детерминированных, вегетативных. Значение этого контура возрастает при нарушении работы внешнего, например, при удалении одного легкого.
Поведенческий – функционирует только в экстремальных ситуациях, когда организм не может длительно поддерживать газовый гомеостаз за счет вышеописанных механизмов. По мере того, как газовые показатели все больше отклоняются от нормы, возникает мотивация по устранению такой ситуации или ее избегания. Это формирует определенное поведение, результаты которого решают данную задачу.
Пятое звено – обратная афферентация. Это мульти-параметрическая импульсация в дыхательный центр от рецепторов о результатах совершенных системой действий, т.е. о степени достижения полезного приспособительного результата. Она адресована находящемуся в дыхательном центре контролирующему аппарату – акцептору результата действия. Как только инспираторные нейроны посылают команды к эффекторам, по коллатералям аксонов этих нейронов копии команд распространяются к специальной группе интернейронов, связанных между собой циклическими соотношениями. Возбуждение в «ловушках» продолжает циркулировать до поступления обратной афферентации от хеморецепторов и рецепторов растяжения легких (см. ниже). Затем происходит ее оценка. Если характер поступающей импульсации соответствует дыхательной потребности, вдох прекращается и после выдоха формируется следующий дыхательный цикл. Если нет – инспираторные нейроны изменяют команду и посылают её вентиляторному аппарату при следующем вдохе.
Следовательно, в функциональной системе дыхания на основе обратных связей все время оценивается дыхательная потребность. С помощью акцептора результата действия она постоянно сопоставляется с количеством и качеством поступившего в легкие воздуха.
Нейроны ДЦ по Миславскому:
Ретикулярные нейроны осуществляют связь дыхательных с вышележащими уровнями дыхательного центра и с различными рецепторами.
Респираторно-связанные нейроны иннервируют мышцы верхних дыхательных путей.
Среди дыхательных нейронов различают инспираторные (разряжаются во время вдоха) и экспираторные (активны во время выдоха). В зависимости от соотношения биоэлектрической активности дыхательных нейронов с фазами вдоха и выдоха выделяют:
1) «ранние» инспираторные нейроны – разряжаются с максимальной частотой в начале вдоха;
2) «поздние» инспираторные нейроны – частота их разрядов максимальна в конце вдоха;
3) «полные» инспираторные нейроны – их импульсная активность постоянна или постепенно нарастает в течение вдоха;
4) постинспираторные нейроны – максимально активны в начале выдоха;
5) экспираторные нейроны – их активность постоянна или постепенно увеличивается в течение выдоха;
6) преинспираторные нейроны – разряжаются с максимальной частотой в самом конце выдоха непосредственно перед вдохом.
24.Опишите центральные и периферические хеморецепторы и их значение в регуляции дыхания. Через какие рецепторы и как влияют на дыхание гипоксия, гиперкапния, ацидоз? Механизм первого вдоха новорожденного.
Хеморецепторный контроль дыхания осуществляется при участии центральных и периферических хеморецепторов. Центральные (медуллярные) хеморецепторы расположены непосредственно в в ростральных отделах вентральной дыхательной группы, в структурах голубого пятна (locus coeruleus), в ретикулярных ядрах шва ствола мозга и реагируют на водородные ионы в окружающей их межклеточной жидкости мозга (рис. 10.23). Центральные хеморецепторы представляют собой нейроны, которые в определенной степени являются рецепторами углекислого газа, поскольку величина рН обусловлена парциальным давлением С02, согласно уравнению Гендерсона—Гасельбаха, а также тем, что концентрация ионов водорода в межклеточной жидкости мозга зависит от парциального давления углекислого газа в артериальной крови. Рис. 10.23. Зависимость вентиляции легких от степени стимуляции центральных хеморецепторов изменениями [Н+]/РС02 в артериальной крови. Увеличение парциального давления С02 в артериальной крови выше порога (РС02 = 40 мм рт. ст.) линейно увеличивает объем вентиляции легких. Увеличение вентиляции легких при стимуляции центральных хеморецепторов ионами водорода называется центральным хеморефлексом, который оказывает выраженное влияние на дыхание.
Так, в ответ на уменьшение рН внеклеточной жидкости мозга в области локализации рецепторов на 0,01 легочная вентиляция возрастает в среднем на 4,0 л/мин. Однако центральные хеморецепторы медленно реагируют на изменения С02 в артериальной крови, что обусловлено их локализацией в ткани мозга. У человека центральные хеморецепторы стимулируют линейное увеличение вентиляции легких при увеличении С02 в артериальной крови выше порог, равного 40 мм рт. ст. Периферические (артериальные) хеморецепторы расположены в каротидных тельцах в области бифуркации общих сонных артерий и в аортальных тельцах в области дуги аорты. Периферические хеморецепторы реагируют как на изменение концентрации водородных ионов, так и парциального давления кислорода в артериальной крови. Рецепторы чувствительны к анаэробным метаболитам, которые образуются в ткани каротидных телец при недостатке кислорода. Недостаток кислорода в тканях каротидных телец может возникнуть, например, при гиповентиляции, ведущей к гипоксии, а также при гипо-тензии, вызывающей снижение кровотока в сосудах каротидных телец.
При гипоксии (низкое парциальное давление кислорода) периферические хеморецепторы активируются под влиянием увеличения концентрации в артериальной крови, прежде всего, ионов водорода и РС02. Рис. 10.24. Зависимость вентиляции легких от степени стимуляции периферических хеморецепторов гипоксическим стимулом. При стимуляции периферических хеморецепторов гипоксией имеет место мультипликативное взаимодействие парциального давления С02 в артериальной крови и гипоксии, в результате которого происходит максимальное увеличение вентиляции легких. Напротив, при высоком Парциальном давлении кислорода в артериальной крови периферические хеморецепторы слабо реагируют на увеличение РС02. Если в артериальной крови парциальное давление С02 становится ниже порога (40 мм рт.ст.), то периферические хеморецепторы также слабо реагируют на гипоксию. Действие на периферические хеморецепторы этих раздражителей усиливается по мере снижения в крови Р02 (мультипликативное взаимодействие). Гипоксия увеличивает чувствительность периферических хеморецепторов к [Н+] и С02. Это состояние называется асфиксией и возникает при прекращении вентиляции легких. Поэтому периферические хеморецепторы называются часто рецепторами асфиксии. Импульсы от периферических хеморецепторов по волокнам синокаротидного нерва (нерв Геринга — часть языкоглоточного нерва) и аортальной ветви блуждающего нерва достигают чувствительных нейронов ядра одиночного тракта продолговатого мозга, а затем переключаются на нейроны дыхательного центра. Возбуждение последнего вызывают прирост вентиляции легких. Вентиляция легких увеличивается линейно в соответствии с величиной [Н+] и РС02 выше порога (40 мм рт. ст.) в артериальной крови, протекающей 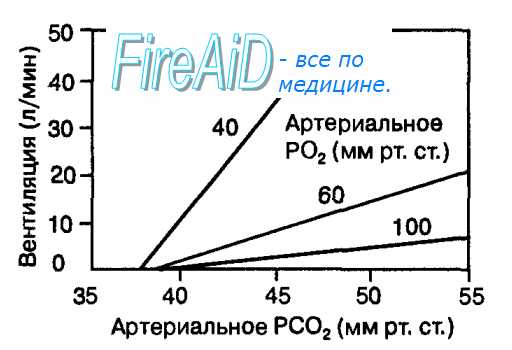 через каротидные и аортальные тельца (рис. 10.24). Наклон кривой на рисунке, который отражает чувствительность периферических хеморецепторов к [Н+] и РС02, варьирует в зависимости от степени гипоксии. через каротидные и аортальные тельца (рис. 10.24). Наклон кривой на рисунке, который отражает чувствительность периферических хеморецепторов к [Н+] и РС02, варьирует в зависимости от степени гипоксии.
Механизм первого вдоха. Внутриутробно плод по-настоящему не дышит, так как он получает О2 из организма матери и туда же выделяет СО2 через пуповину и плаценту. С 11-й недели беременности у плода появляются периодические сокращения диафрагмы и межреберных мышц, которые усиливаются к концу внутриутробного периода. Эти движения необходимы для нормального развития легких, они подготавливают аппарат внешнего дыхания к самостоятельному дыханию после рождения. После рождения ребенка пуповина пережимается и перерезается, что приводит к повышению в артериальной крови напряжения СО2 и понижению напряжения О2. Углекислота возбуждает центральные хеморецепторы, что стимулирует инспираторный отдел дыхательного центра. Активность инспираторных нейронов также стимулирует поток импульсов с экстерорецепторов: тактильных, температурных, болевых, зрительных, слуховых, вестибулярных. Первому вдоху способствуют устранение рефлекса ныряльщика и резкое расширение сжатой во время родов грудной клетки.
При отсутствии самостоятельного дыхания можно пробудить ритмику дыхания с помощью прямого искусственного дыхания «рот в рот» или используя резиновую грушу, запуская регуляторные рефлексы с воздухоносных путей. В результате новорожденный делает первый вдох, обычно глубокий, так как возбуждение иррадиирует на вышележащие центры. Первый вдох, растягивая легкие по рефлексу Геринга–Брейера и с участием пневмотаксического центра, стимулирует первый выдох, который тоже всегда глубокий и активный, так как включаются подвижные ассоциации дыхательного центра. Он обычно сопровождается первым криком ребенка. Имеются особенности первого выдоха новорожденного. Он может быть затруднен из-за функционально суженной голосовой щели и напряжения голосовых связок. Выдыхается воздуха в 2–3 раза меньше, чем вдыхается, так как происходит формирование функциональной остаточной емкости. В процессе дыхания у новорожденного жидкость из альвеол удаляется в течение нескольких часов. Часть жидкости уходит с выдыхаемым воздухом, частично она всасывается в кровяное русло согласно градиенту онкотического давления (онкотическое давление крови выше, нежели легочной жидкости), частично удаляется всасыванием в лимфу. Во время родов небольшое количество жидкости заглатывается ребенком и выходит наружу через рот. Минутный объем воздуха новорожденного составляет 1300 мл, жизненная емкость легкого равна 120–140 мл, она определяется при крике ребенка – так называемая ЖЕЛ крика; частота дыхания – около 40 в 1 мин.
Дыхание, обеспечивающее достаточную вентиляцию легких и газообмен в них, возможно даже у недоношенных детей. Формирование всех механизмов, обеспечивающих эти процессы, начинается с 6–7 месяца внутриутробного развития. Давление в плевральной щели новорожденного является отрицательным только при вдохе. Гортань у детей относительно уже, чем у взрослых.
25.Функциональная система, поддерживающая оптимальное содержание газов в крови и тканях. Перечислить звенья ФУС, описать исполнительные органы и их роль в поддержании газового состава крови и тканей.
См. 23+
Полезный результат ФСКС - нормальная концентрация кислорода в тканях- является иерархически самым главным результатом гомеостатической деятельности организма, так как результаты деятельности других гомеостатических функциональных систем (ФС поддержания АД, ФС поддержания состава крови, ФС рН и др.) являются подрезультатами ФСКС, так как вместе обеспечивают условия для кислородного снабжения организма.
Набор исполнительных механизмов ФСКС определяется теми исполнительными механизмами, которые входят в указанные выше функциональные системы подчиненного ранга. Их пять групп:
1) параметры внешнего дыхания (глубина и частота дыхания, легочные объемы и емкости, эффективность легочной вентиляции);
2) параметры гемодинамики и сердечной деятельности (частота сердцебиений и ударный объем сердца, АД и скорость кровотока);
3) параметры выделительной функции и механизмы поддержания рН, ведь кислотность влияет на кривую диссоциации гемоглобина (выделительная функция ЖКТ и почек, потоотделение, буферные состава крови);
4) параметры насыщения крови кислородом (кислородная емкость крови, количество Нв и эритроцитов, сродство Нв к кислороду);
|




 через каротидные и аортальные тельца (рис. 10.24). Наклон кривой на рисунке, который отражает чувствительность периферических хеморецепторов к [Н+] и РС02, варьирует в зависимости от степени гипоксии.
через каротидные и аортальные тельца (рис. 10.24). Наклон кривой на рисунке, который отражает чувствительность периферических хеморецепторов к [Н+] и РС02, варьирует в зависимости от степени гипоксии.


