Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Последовательность выполненияСодержание книги
Поиск на нашем сайте
Работы
1. Заполнить таблицу
*Навеска исследуемого металла, масса которой определяется с точностью до 0,0001 г, выдается студентам лаборантом. ** Данные, соответствующие строкам 5-7, предоставляются преподавателем.
2. Перед началом проведения эксперимента, необходимо отсоединить двухколенную пробиркуот основной бюретки, вылить содержимое пробирки (если оно имеется) в раковину и тщательно промыть двухколенную пробирку водопроводной водой. 3. Расположить рабочую и вспомогательную бюретки путем маневрирования их положения по высоте таким образом, чтобы уровень воды в основной бюретке был около нулевого значения. 4.Навеску металла поместить в одно из «колен» двухколенной пробирки. 5. В другое «колено» пробирки прилить (аккуратно, чтобы исключить попадание кислоты в «колено» с навеской металла) ~ 2 мл раствора соляной кислоты, т.е. до метки, нанесенной красным химическим карандашом. 6. Двухколенную пробирку вращательным движением плотно надеть на пробку (мениск воды в основной бюретке при этом немного сместится от нулевого значения). 7. Проверить герметичность прибора. С этой целью вспомогательную бюретку, предварительно освободив от крепления, резко опустить вниз на 15–20 см. Если прибор герметичен, то мениск воды в ней останется практически на том же уровне. Если герметичность отсутствует, мениски воды в бюретках будут постепенно сравниваться. В этом случае с помощью лаборанта следует проверить надежность соединений в приборе. 8. Перед началом эксперимента необходимо установить давление в герметичном приборе равным атмосферному давлению. Для этого, перемещая бюретки относительно друг друга, следует добиться, чтобы мениски воды в бюретках находились строго на одной высоте, т.е. на одной горизонтальной прямой. 9. Записать в таблицу значение начального уровня воды в рабочей бюретке. 10. Бережно прилить кислоту в «колено», где находится навеска металла, наклоняя пробирку осторожно, чтобы не нарушить герметичность прибора. Для того чтобы исключить разгерметизацию прибора в ходе выделения водорода по реакции, вспомогательную бюретку следует аккуратно снижать по высоте, а рабочую поднимать, добиваясь тем самым соблюдения положения менисков воды на одном уровне. 11. Полное растворение металла по реакции фиксируется визуально: выделение пузырьков водорода и понижение уровня воды в рабочей бюретке прекращается. Удостоверившись, что раствор в пробирке охладился до комнатной температуры, записать в таблицу конечный уровень воды после окончания эксперимента. 12. Перевести объем выделившегося водорода, измеренный при данном атмосферном давлении V(H2), к объему при нормальных условиях V0, используя уравнение, объединяющее газовые законы Бойля–Мариотта и Гей–Люссака: где р0 – нормальное атмосферное давление (760 мм рт.ст.); V0 – объем водорода при нормальных условиях; То – нормальная температура по абсолютной шкале (273 К); р1 – давление водорода в условиях опыта (рн2,мм рт.ст.), V1 – объем водорода в условиях опыта (V (Н2), мл; Т – температура опыта (273 + t°С). 13. Рассчитать эквивалент металла по закону эквивалентов, используя пропорцию: Э(Ме), г – 11 200 мл (Н2) 14. Рассчитать атомную массу металла по формуле А (Ме) = Э (Ме) ∙ В(Ме). 15. Используя периодическую таблицу элементов Д.И. Менделеева, определить природу металла по опытному значению атомной массы (группа элементов в таблице совпадает со степенью окисления металла, т.е. с его валентностью 2. 16. Составить уравнение реакции найденного металла с соляной кислотой. 17. Вычислить относительную ошибку опыта: КОНТРОЛЬНЫЕ ВОПРОСЫ И ЗАДАЧИ 1. Что называется химическим эквивалентом? 2. Сформулируйте закон эквивалентов. 3. Сформулируйте закон парциальных давлений, установленный Дальтоном. 4. Как вычисляется эквивалент сложного вещества (оксидов, кислот, оснований и солей)? 5. Вычислите эквивалент хрома в оксиде, в котором содержится 52% хрома и 48% кислорода. 6. Окислением 2,8 г кадмия получено 3,2 г оксида. Вычислите эквивалент кадмия.
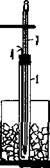
Работа № 2. Криометрия Цель работы – определение температуры кристаллизации (замерзания) раствора и использование этого физико-химического свойства для расчета молекулярной массы растворенного неэлектролита и степени диссоциации раствора электролита. Оборудование и реактивы 1. Прибор криометр (рис. 6.2), состоящий из: а) широкой стеклянной пробирки (1) для исследуемого раствора, закрепленной в штативе (2); б) пробки со вставленным в нее термометром (3) и металлической мешалкой (4); в) сосуда (криостата) (5) для охладительной смеси, которая готовится изо льда и 1-2 столовых ложек поваренной соли. 2. Мерный цилиндр. 3. Растворы неэлектролита и электролита.
Рис. 6.2. Прибор для криометрических измерений
|
|||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2021-03-10; просмотров: 214; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.145.9.200 (0.007 с.) |

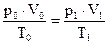 ,
,  – Vo (Н2), мл
– Vo (Н2), мл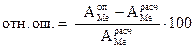 [%].
[%].