
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Концентрационные цепи и концентрационные гальванические элементыСодержание книги
Поиск на нашем сайте
Концентрационные цепи бывают двух родов. Концентрационные цепи первого рода содержат два металла или сплава, различающихся по концентрации активной массы или по составу сплава и погруженных в один и тот же раствор. Примером газовой концентрационной цепи первого рода может служить элемент, составленный из двух газовых, например хлорных, электродов с различными давлениями газа в приэлектродных пространствах и общим раствором электролита – соляной кислотой НСl: (-)Cl2(p1)Pt|HCl|Cl2 (p2),Pt(+); p2>p1 (3.19) Концентрационные цепи второго рода состоят из двух электродов одного металла, например Аg, покрытого своей нерастворимой солью АgС1, и погруженных в растворы HCl с различной активностью ионов хлора а1 и а2. (-)Ag,AgCl|HCl||HCl|AgCl,Ag(+) (3.20)
В случае разбавленных растворов вместо величин активностей а1 и а2 можно пользоваться величинами концентраций растворов С1 и С2. Скачок потенциала на границе раздела фаз в данном случае возникает за счет того, что на электроде, погруженном в менее активный (с меньшей концентрацией) раствор, протекает процесс окисления серебра по схеме: Аgo + Cl- → АgCl + е. На электроде, погруженном в более активный раствор (с большей концентрацией раствора НСl), протекает процесс восстановления хлорида серебра: АgCl + е → Аgo + Cl-.
При работе указанного элемента оба электрода термодинамически не изменяются, а ЭДС концентрационного элемента возникает за счет диффузии ионов из мест с большей их концентрацией в более разбавленный раствор, т.е. за счет выравнивания концентраций между двумя растворами. Поэтому такие гальванические элементы называются концентрационными элементами, или цепями с переносом. Без учета диффузионного потенциала, возникающего на границе раздела двух растворов за счет различной скорости движения ионов, электродные потенциалы анода Ea и катода Ек будут равны соответственно:
Так как Ек° = Еа°, а n = 1, то ЭДС (∆Е) такого концентрационного элемента
Для того чтобы рассчитать диффузионный потенциал, вначале следует рассмотреть процесс его возникновения. Переход НСl из раствора с более высокой активностью в менее активный осуществляется за счет диффузии ионов Н+ и С1-, скорость которой определяется их подвижностью, пропорциональной скорости движения ионов. Если градиент приложенного напряжения внешнего поля равен 1 В/см, то в данном случае скорость движения ионов называется абсолютной скоростью. Подвижность иона (λ+ и λ-) представляет собой произведение абсолютной скорости иона (V+ и V-) на число Фарадея λ+ = V+∙ F; λ- = V-∙ F. (3.24) Доля количества электричества, которую переносит данный ион, называется числом переноса иона: катиона:
аниона: (3.25)
Для бесконечно разбавленного раствора:
В рассматриваемом примере
Сумма tH+ и tCl- равна единице. Так как подвижность иона Н+ больше, чем иона С1-, то менее концентрированный раствор будет заряжаться согласно знаку более подвижного иона Н+, т.е. будет содержать больше положительных ионов, а более концентрированный раствор − больше отрицательных ионов. Вследствие этого и возникает диффузионный скачок потенциала на границе раздела фаз, одинаковых по природе, но разных по концентрации растворов. В общем случае ЭДС концентрационного элемента
где
|
|||||
|
Последнее изменение этой страницы: 2021-03-10; просмотров: 146; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.138.120.12 (0.008 с.) |

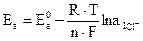 ; (3.21)
; (3.21)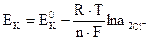 . (3.22)
. (3.22)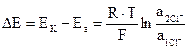 . (3.23)
. (3.23)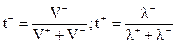 ;
;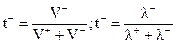 .
.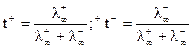 .
.
 . (3.26)
. (3.26)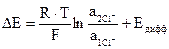 , (3.27)
, (3.27)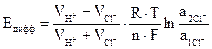 . (3.28)
. (3.28)


