
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Окислительно-восстановительные элементы
Окислительно-восстановительные гальванические элементы содержат окислительно-восстановительные электроды. К последним относятся все электроды, в реакциях на которых не участвуют ни металлы, ни газы, а только ионы и нейтральные молекулы. При реакциях на электродах в этом случае не происходит ни растворения, ни выделения каких − либо веществ из растворов электролитов, а электроды в данном случае служат только переносчиками электронов. Окислительно-восстановительные электроды представляют собой чаще всего платиновую или изготовленную из другого инертного материала пластинку, погруженную в раствор, содержащий одновременно и окисленную, и восстановленную форму одного и того же иона (например: Fe 3+ и Fe2+; Сг2О72- и Cr3+; MnO4- и Mn2+ и т.д.). Окислительно-восстановительные электрохимические реакции в данном случае связаны с изменением степени окисления элементов, входящих в состав ионов. В практике электрохимических измерений потенциалы окислительно-восстановительных электродов, как и электродов других типов, определяются по отношению к электроду сравнения. Обычно это стандартные хлорсеребряный или каломельный электроды, относящиеся к электродам второго рода. Процессы, протекающие при работе окислительно-восстановительных элементов, рассмотрим на конкретном примере. Электролитом первого электрода будет служить смесь растворов солей Fe2(SO4)3 и FeSO4, которая содержит ионы железа в различной степени окисления Fe3+ и Fe2+ , а второго − смесь растворов MnSO4 и KMnO4, содержащая ионы Mn2+ и MnO4-, в которых степень окисления марганца равна соответственно +2 и +7. Схематически эти окислительно-восстановительные электроды изображаются следующим образом: Pt│Fe3+, Fe2+ и Pt│Mn2+, MnO4- При погружении инертного электрода (Pt) в раствор, содержащий смесь двух солей FeSO4 и Fe2(SO4)3, на границе раздела фаз возникает окислительно-восстановительный потенциал, иначе называемый редокс (Red/Ox) потенциалом, за счет окислительно-восстановительной реакции между двумя ионами Fe2+ и Fe3+ в растворе Fe2+ - е ↔ Fe3+. Уравнение Нернста для такого Red/Ox потенциала запишется следующим образом: или при Т = 298 К где
На втором электроде протекает окислительно-восстановительный процесс MnO4- + 8H+ + 5 e ↔ Mn2+ + 4H2O, потенциал которого
или для Т = 298 К
Схема рассмотренного гальванического элемента может быть записана следующим образом: (-)Pt|Fe3+,Fe2+|| MnO4-,Mn2+,H+|Pt(+), (3.15) а протекающая в нем суммарная токообразующая реакция запишется так:
● в ионной форме: 5Fe2+ + MnO4- + 8H+ +5 e →5Fe3+ + Mn 2+ + 4H2O; (3.16) ● в молекулярной форме: 10FeSO4 + 2 KMnO4 + 8H2SO4 →5Fe2(SO4)3 + 2MnSO4 + K2SO4 + 8H2O (3.17)
Для определения стандартной ЭДС гальванического элемента, как уже было сказано выше, следует от потенциала катода с более положительным потенциалом (окислителя) вычесть потенциал анода (восстановителя) с менее положительным значением потенциала: ∆ E0 = Процессы окисления-восстановления на электродах будут происходить до тех пор, пока их потенциалы не станут равными и в системе не установится состояние равновесия.
|
|||||
|
Последнее изменение этой страницы: 2021-03-10; просмотров: 90; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.117.70.132 (0.007 с.) |
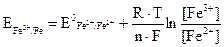
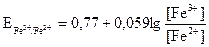 , (3.13)
, (3.13)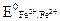 = 0,77 В − стандартный окислительно-восстановительный потенциал при [Fe3+] = [Fe2+] = 1 г-ион/л;
= 0,77 В − стандартный окислительно-восстановительный потенциал при [Fe3+] = [Fe2+] = 1 г-ион/л;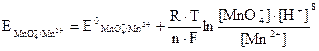
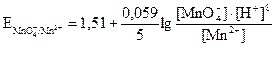 . (3.14)
. (3.14)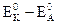 = 1,51-0,77 = 0,74 В (3.18)
= 1,51-0,77 = 0,74 В (3.18)


