Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Гликозиды написать формулу метил-альфа-D-глюкозогликозидСодержание книги
Поиск на нашем сайте
ГЛИКОЗИДЫ, соед., в к-рых остаток циклич. формы моно- или олигосахарида (гликозильный, или УГный, остаток) связан с др. орг. остатком (агликоном) через гетероатом; соотв. различают О-, N-, S-гликозиды и др. Связь м/у гликозильным остатком и агликоном наз. гликозидной. При обр-нии гликозидов возникает новый асимметрич. гликозидный центр. Его конфигурацию обознач По размеру цикла УГ остатка гликозиды делят на фуранозиды (5-членные), пиранозиды (6-) и септанозиды. (7-); по числу моносахаридных остатков в УГной части мол-лы - на моноозиды, биозиды, триозиды и олигозиды (соотв. производные моно-, ди-, три- и олигосахаридов). Присоед-ие гликозильного остатка к агликону (гликозилирование) повышает гидрофильность соед-ия, что играет важную роль в метаболизме. Мн. УГные остатки, особенно олигосахаридные, выполняют ф-ции специфич. маркеров пов-стей кл и биополимеров, обусл-ющих их узнавание др. кл. К О-гликозидам в широком смысле слова относ не только гликозиды с неУГными агликонами, но и внутр. ангидриды сахаров (внутр. гликозиды), олиго- и полисахариды. О-Гликозиды- малолетучие кристаллич. или аморфные в-ва. Гликозиды низших спиртов легко раств. в воде, спиртах, не раств. в малополярных орг. р-рителях. Соед. с полярными агликонами (напр., гликозиды полиолов) раств. в воде, соед. с крупными гидрофобными агликонами не раств. в воде и малополярных р-рителях. Для олигозидов с большими малополярными агликонами хар-рны пенообразующие св-ва. Гликозиды не облад хим. св-вами восст-ющих Сахаров, обусл-ными карбонильной группой, не подвержены мутаротации. Они легко ацилируются ангидридами и галоген-ангидридами к-т в пиридине с обр-нием сложных эфиров, алкилируются типичными алкилирующими агентами в сильнощелочных средах, обр-ют циклич. ацетали и кетали при конденсации с карбонильными соед., окисляются периодатами с расщеплением связей С—С, подвергаются к-тному гидролизу, алкоголизу, формолизу с расщеплением гликозидной связи. Скорость гидролиза в Наиб. степени зависит от размера цикла: фуранозиды гидролизуются на два порядка быстрее пиранозидов. Механизм гидролиза м. б. представлен след. схемой (знак ~ означает, что мол-ла гликозида может им Скор ф-тативного гидролиза, к-рый осущ-тся под дейст гликозидгидролаз, зависит от стр-ры агликона. Гликозиды с алифатич. и алициклич. агликонами устойчивы к действию р-ров щелочей, с ароматич. и нек-рыми гетероциклич. агликонами - неустойчивы. Так, щелочное расщепление К прир. О-гликозидам относятся сапонины, гликозиды сердечные, флавоноидные коф-ты (напр., рутин), гликолипиды, гликопротеины, нек-рые антибиотики. Хим. св-ва N-гликозидов сильно зависят от хар-ра заместителей при атоме N. Алифатич. и ароматич. N-Гликозиды, содержащие при N атом водорода, подвергаются мутаротации (подобно восстанавливающим сахарам) вследствие таутомерного превращения в форму шиффовых оснований, напр.: Они легко подвергаются к-тному и щелочному гидролизу. N-Гликозиламиды, в т.ч. N-гликозилмочевины, и соед., в к-рых гликозидный атом N включен в амидную стр-ру, не склонны к мутаротации и по устойчивости к гидролизу сходны с О-гликозидами. Алифатич. и ароматич. гликозиды, в к-рых гликозидный атом N обладает достаточно высокой основностью, подвергаются перегруппировке в 1-амино-1-дезоксикетозы (Амадори перегруппировка). Алифатич. и ароматич. N-гликозиды получают конденсацией восстанавливающих Сахаров с аминами; N-гликозиламиды и гликопептиды - восстановлением гликозилазидов с послед. N-ацилированием; нуклеозиды и их стр-рные аналоги-N-гликозилированием азотсодержащих гетероциклич. соединений ацилгликозилгалогенидами и их аналогами. К прир. N-гликозидам относятся нуклеозиды, нуклеотиды, нуклеиновые к-ты, гликопротеины, нек-рые смешанные биополимеры, в к-рых гликозидная связь соединяет УГные и пептидные цепи через амидный атом N остатка аспарагина. Многие N-гликозиды и стр-рные аналоги нуклеозидов, являясь антиметаболитами нуклеозидов, обнаруживают высокую физиол. активность и используются в кач-ве лек. препаратов, напр. фторафур, цитарабин. Для S-гликозидов хар-рны специфич. св-ва, связанные с возм-стью окислит.-восстановит. р-ций по атому S. К ним относятся гидрогенолиз над никелем Ренея, окислит. расщепление галогенами, окисление до сульфонов, обр-ние из S-гликозидов гликозилгалогенидов. Гидролиз S-гликозидов в отличие от гидролиза О-гликозидов может протекать в мягких условиях в присут. солей Hg и Cd, что позволяет вести селективную р-цию, не затрагивая О-гликозидные связи мол-лы. S-Гликозиды, аналогично ароматич. О-гликозидам, получают конденсацией тиолятов щелочных металлов с ацилгликозилгалогенидами. Специфич. методы - конденсация ацилгликозилгалогенидов с тиомочевиной с послед. гидролизом тиурониевой соли и частичный гидролиз диалкилдитиоацеталей Сахаров, катализируемый солями Hg.
|
||||
|
Последнее изменение этой страницы: 2017-01-24; просмотров: 260; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.141.198.13 (0.006 с.) |

 или
или  в завис от того, совпадает она или нет с конфиг-ей того углерод атома моносахарида, к-рый определяет принадлежность последнего к D- или L-ряду. Напр., в изомерных метил-О-глюкопиранозидах конфигурация
в завис от того, совпадает она или нет с конфиг-ей того углерод атома моносахарида, к-рый определяет принадлежность последнего к D- или L-ряду. Напр., в изомерных метил-О-глюкопиранозидах конфигурация 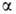 отражается ф-лой I, конфигурация
отражается ф-лой I, конфигурация 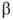 -ф-лой II:
-ф-лой II: 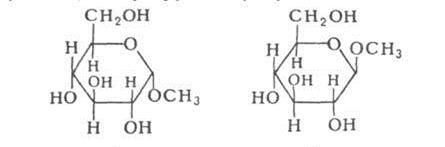
 или
или  конфигурацию):
конфигурацию): 
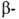 D-глюкопиранозидов с ароматич. агликоном дает 1,6-ангидроглюкозу (левоглюкозан), что явл препаративным методом синтеза последней.
D-глюкопиранозидов с ароматич. агликоном дает 1,6-ангидроглюкозу (левоглюкозан), что явл препаративным методом синтеза последней.