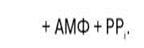Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Общ хар. Сахаров, тригалозный сахар
Углеводы (сахара) – обширная группа полигидроксикарбонильных природных соед. общ хим формула СnH2nOn, или Сn(Н2O)n т.е. Углеводы принято классифицировать на моносахариды, олигосахариды и полисахариды. УГ присутствуют во всех био объектах. В жив кл углеводы обычно составляют всего лишь около 2 % сухого остатка, тогда как в клетках растений – порой до 80-90 %. Полисахариды предст собой один из видов биополимеров, к-рые не кодируются генетич и синтезируются нематричным способом. УГ – это наиболее распростр-ные в биосфере орг-кие соед, они составляют больше половины всех органических веществ. Безусловным лидером среди углеводов является целлюлоза. УГ наряду с белками и липидами явл важнейшими хим соед, входящими в состав живых орг-мов. У ч-ка и жив УГ выполняют важные функции: энергетическую (главный вид клеточного топлива), стр-рную (обязательный компонент большинства внутриклеточных стр-р) и защитную (участие углеводных компонентов
иммуноглобулинов в поддержании иммунитета).
Углеводы (рибоза, дезоксирибоза) используются для синтеза нуклеиновых кислот, они являются составными компонентами нуклеотидных ко-ферментов, играющих исключительно важную роль в метаболизме живых существ. В последнее время все большее внимание к себе привлекают смешанные биополимеры, содержащие углеводы: гликопептиды и глико-протеины, гликолипиды и липополисахариды, гликолипопротеины и т.д. Эти вещества выполняют в организме сложные и важные функции. С нарушением обмена углеводов тесно связан ряд заболеваний: сахарный диабет, галактоземия, нарушение в системе депо гликогена, нетолерантность к молоку и т.д. Трегалоза (a-D-глюкопиранозил-(1®1)-a-D-глюкопиранозид) – невосстанавливающий резервный дисахарид грибов и насекомых. 4. Р. Малат+над=пируват+?
Оксидоредуктазы Оксидоредуктазы. К классу оксидоредуктаз относят ферменты, кат-ющие с участием двух субстратов ОВР, лежащие в основе био окисления. Сист-ческие названия их сост по форме «донор: акцептор оксидоредуктаза». Например, лактат: НАД+ оксидоредуктаза для лактатдегидрогеназы (ЛДГ). Различают следующие основные оксидоредуктазы: аэробные дегидро-геназы или оксидазы, кат-ющие перенос протонов (электронов) непосредственно на кислород; анаэробные дегидрогеназы, ускоряющие перенос протонов (электронов) на промежут субстрат, но не на кислород; цитохромы, кат-ющие перенос только электронов. К этому кл относят также гемсодержащие ф-нты каталазу и пероксидазу, кат-ющие реакции с уч-ем перекиси водорода.
Бэта окисление жирн кислот. окисление мол-лы ЖК в происходит в β-полож. В результ от молекулы ЖК послед-но отщеп-тся двууглеродные фрагменты со стороны карбоксильной гр. Место окисления – митох. Проц окисления ЖК склад-ся из след осн этапов. Активация ЖК. Активация ЖК протекает на наружной поверхности мембраны митохондрий при участии АТФ, коэнзима A (HS-KoA) и ионов Mg2+. Реакция катализируется ферментом ацил-КоА-синтетазой:
В результате реакции обр-тся ацил-КоА, являющийся активной формой ЖК. Считают, что активация ЖК протекает в 2 этапа. Сначала ЖК реагирует с АТФ с обр-нием ациладенилата, представляющим собой эфир ЖК и АМФ. Далее сульфгидрильная группа КоА действует на прочно связанный с ферментом ациладенилат с образованием ацил-КоА и АМФ. Транспорт ЖК внутрь митох. Коэнзимная форма ЖК, в равной мере как и свободные ЖКы, не обладает способностью проникать внутрь митох, где, собственно, и протекает их окисление. Переносчиком активированных ЖК с длинной цепью через внутреннюю митохондриальную мембрану служит карнитин. Ацильная группа переносится с атома серы КоА на гидро-ксильную группу карнитина с образованием ацилкарнитина, который диффундирует через внутреннюю митохондриальную мембрану:
Р-ция протекает при участии специфического цитоплазматического фермента карнитин-ацилтрансферазы. Уже на той стороне мембраны, к-рая обращена к матриксу, ацильная группа переносится обратно на КоА. Иными словами, после прохождения ацилкарнитина через мембрану митох происход обратная реакция – расщепление ацилкарнитина при участии HS-KoA и митохондриальной карнитин-ацилтрансферазы:
Внутримитохондриальное окислениеЖК. Проц окисления ЖК в митох клетки включает несколько последовательных энзиматических реакций. Первая стадия дегидрирования. Ацил-КоА в митох прежде всего подвергается ферментативному дегидрированию, при этом ацил-КоА теряет 2 атома водорода в α- и β-положениях, превращаясь в КоА-эфир ненасыщенной кислоты. Таким образом, первой реакцией в каждом цикле распада ацил-КоА является его окисление ацил-КоА-де-гидрогеназой, приводящее к образованию еноил-КоА с двойной связью между С-2 и С-3:
Сущ-ет несколько ФАД-содержащих ацил-КоА-дегидрогеназ, каждая из к-рых облад специф-тью по отнош к ацил-КоА с определ длиной углеродной цепи. Стадия гидратации. Ненасыщ ацил-КоА (еноил-КоА) при участии фермента еноил-КоА-гидратазы присоединяет молекулу воды. В результате образуется β-оксиацил-КоА (или 3-гидроксиацил-КоА):
Заметим, что гидратация еноил-КоА стереоспецифична, подобно гидратации фумарата и аконитата. В результате гидратации транс-Δ2-двойной связи образуется только L-изомер 3-гидроксиацил-КоА. Вторая стадия дегидрирования. Образовавшийся β-оксиацил-КоА (3-гидроксиацил-КоА) затем дегидрируется. Эту реакцию катализируют НАД+-зависимые дегидрогеназы:
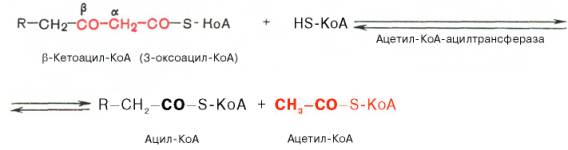
Тиолазная реакция. В ходе предыдущих реакций происходило окисление метиленовой группы при С-3 в оксогруппу. Тиолазная реакция представляет собой расщепление 3-оксоацил-КоА с помощью тиоловой группы второй молекулы КоА. В результате образуется укороченный на два углеродных атома ацил-КоА и двууглеродный фрагмент в виде ацетил-КоА. Данная реакция катализируется ацетил-КоА-ацилтрансферазой (β-ке-тотиолазой):
Обр-шийся ацетил-КоА подвергается окислению в цикле трикарбоновых к-т, а ацил-КоА, укоротившийся на два углеродных атома, снова многократно проходит весь путь β-окисления вплоть до образования бутирил-КоА (4-углеродное соед), к-рый в свою очередь окисляется до 2 мол-л ацетил-КоА. Например, при окислении пальмитиновой кислоты (С16) повторяется 7 циклов β-окисления. При окисл ЖК, содержащей n углер атомов, происходит n/2–1 цикл β-окисления (т.е. на один цикл меньше, чем n/2, так как при окислении бутирил-КоА сразу происходит образование 2 молекул ацетил-КоА) и всего получится п/2 молекул ацетил-КоА. Следовательно, суммарное уравнение β-окисления активированной кислоты можно записать так: Пальмитоил-КоА + 7ФАД + 7НАД+ + 7Н2O + 7HS-KoA –> 8Ацетил-КоА + 7ФАДН2 + 7НАДН + 7Н+. Баланс энергии. При каждом цикле β-окисления обр-тся 1 мол-ла ФАДН2 и 1 молекула НАДН. Последние в проц окисления в дыхательной цепи и сопряженного с ним фосфорилирования дают: ФАДН2 – 2 молекулы АТФ и НАДН – 3 молекулы АТФ, т.е. в сумме за один цикл образуется 5 молекул АТФ. При окислении пальмитиновой кислоты образуется 5 х 7 = 35 молекул АТФ. В процессе β-окисления пальмитиновой кислоты образуется 8 молекул ацетил-КоА, каждая из которых, «сгорая» в цикле трикарбоновых кислот, дает 12 молекул АТФ, а 8 молекул ацетил-КоА дадут 12 х 8 = 96 молекул АТФ. Таким образом, всего при полном β-окислении пальмитиновой кислоты образуется 35 + 96 = 131 молекула АТФ. С учетом одной молекулы АТФ, потраченной в самом начале на образование активной формы пальмитиновой кислоты (пальмитоил-КоА), общий энергетический выход при полном окислении одной молекулы пальмитиновой кислоты в условиях животного организма составит 131 – 1 = 130 молекул АТФ. Изменение свободной энергии ΔF при полном сгорании 1 моля пальмитиновой кислоты составляет 2338 ккал, а богатая энергией фосфатная связь АТФ характеризуется величиной 7,6 ккал/моль. Нетрудно подсчитать, что примерно 990 ккал (7,6 х 130), или 42% от всей потенциальной энергии пальмитиновой кислоты при ее окислении в организме, используется для ресинтеза АТФ, а оставшаяся часть, очевидно, теряется в виде тепла.
Следовательно, эффективность накопления энергии в результате окисления ЖК при стандартных условиях составляет ~ 40%, что близко к соответствующей величине для гликолиза, цикла трикарбоновых кислот и окислительного фосфорилирования Билет 4
|
|||||||
|
Последнее изменение этой страницы: 2017-01-24; просмотров: 161; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 52.14.126.74 (0.009 с.) |