Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Произв. Моносахаридов: кислоты, гликозиды, аминосахара
Реакции полуацетального гидроксила. Уже отмечалось, что моносахариды как в кристаллическом состоянии, так и в растворе в основном существуют в полуацетальных формах. Полуацетальный гидроксил отличается большей реакционной способностью и может замещаться другими группировками в реакциях со спиртами, карбоновыми кислотами, фенолами и т.д. Продукт реакции называют гликозидом. Соответственно α- и β-изоме-рам моносахаридов существуют α- и β-глюкозиды. Например, при реакции метилового спирта с глюкозой (допустим, в β-пиранозной форме) в присутствии неорганических кислот образуется продукт алкилирования ме-тил-β-D-глюкопиранозид:
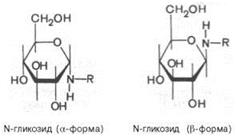
Ацилированию и метилированию способны подвергаться и остальные группы моносахаридов, но при намного более жестких условиях. Если в реакцию вступают спирты, фенолы или карбоновые кислоты, продукты реакции называют О-гликозидами. Следовательно, метил-β-D-глюкопира-нозид и ацетил-β-D-глюкопиранозид являются О-гликозидами (связь осуществляется через кислород). Природные О-гликозиды, большинство из которых образуется в результате жизнедеятельности растений, существуют преимущественно в β-форме. Важным классом гликозидов являются N-гликозиды, в которых глико-зидная связь осуществляется через азот, а не через кислород. N-гликозиды рассматривают как производные моносахаридов, у которых гликозидная часть молекулы связана через атом азота с радикалом органического соединения R, не являющегося углеводом. Как и О-гликозиды, N-гликозиды могут быть построены как пиранозиды или как фуранозиды и иметь α-и β-форму:
К N-гликозидам принадлежат исключительно важные в обмене веществ продукты расщепления нуклеиновых кислот и нуклеопротеидов (нуклеоти-ды и нуклеозиды), АТФ, НАД, НАДФ, некоторые антибиотики и т.п. (см. главу 3). Реакции с участием карбонильной группы. Линейная форма в кристаллич препаратах моносахаридов и их растворах присутствует в незначительных количествах, но ее участие в таутомерном равновесии обеспечивает моносахаридам все свойства, присущие альдегидам (в альдозах) или кетонам (в кетозах). Способность альдоз и кетоз присоединять спирты представлена ранее. Рассмотрим некоторые другие их свойства.
Окисление моносахаридов. Обработка альдоз слабыми окислителями приводит к превращению альдегидной группы в положении атома С-1 в карбоксильную группу с образованием так называемых альдоновых кислот. Альдоновой кислотой может быть D-глюконовая кислота, которая образуется при окислении альдегидной группы D-глюкозы. Фосфорилированная форма D-глюконовой кислоты играет важную роль в качестве промежуточного продукта углеводного обмена. Другой пример – D-галактоновая кислота – продукт окисления альдегидной группы D-га-лактозы.
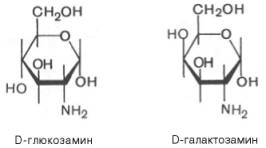
В альдуроновых, или уроновых, кислотах окислена (с образованием карбоксильной группы) первичная спиртовая группа, а альдегидная группа остается неокислен-ной. Уроновая кислота, образующаяся из D-глюкозы, носит название D-глюку-роновой кислоты, а образующаяся из D-галактозы – D-галактоуроновой кислоты. Уроновые кислоты весьма важны в биологическом отношении, многие из них являются компонентами полисахаридов. Восстановление моносахаридов. Моносахариды легко гидрируются по связи С—О и при этом превращаются в многоатомные спирты (сахароспирты). D-глюкоза, например, образует спирт сорбит, а D-манноза – маннит. Восстановление D-фруктозы приводит к эквимолекулярной смеси эпимеров – D-маннита и D-cop-бита, так как в результате гидрирования второй атом углерода становится асимметричным. Такого рода восстановление может осуществляться и ферментативным путем. Аминосахара. Это производные моносах-дов, гидроксильная гр к-рых —ОН замещ аминогруппой —NH2. В зависимости от положения аминогруппы в молекуле аминосахара различают 2-амино-, 3-амино- и 4-аминосахара и т.д. По числу аминогрупп выделяют моноаминосахара и диаминосахара. Аминосахара облад всеми св-ми аминов, обычных моносахаров, а также специфическими свойствами, обусловленными пространственной близостью гидроксильных и аминных групп. В организме ч-ка и жив наиболее важными аминосахарами являются D-глюкозамин и D-галактозамин:
Аминосахара входят в состав мукополисахаридов животного, растительного и бактериального происхождения, являются углеводными компонентами различных гликопротеинов и гликолипидов.
Роль тиреоидных гормонов Щитовидная железа играет исключительно важную роль в обмене веществ. Об этом свидетельствуют резкое изменение основного обмена, наблюдаемое при нарушениях деятельности щитовидной железы, а также ряд косвенных данных, в частности обильное ее кровоснабжение несмотря на небольшую массу (20–30 г). Щитовидная железа состоит из множества особых полостей – фолликулов, заполненных вязким секретом – коллоидом. В состав коллоида входит особый йодсодержащий гликопротеин с высокой мол. массой – порядка 650000 (5000 АМКных остатков). Этот глико-протеин получил название йодтиреоглобулина. Он предст собой запасную форму тироксина и трийодтиронина – основных гормонов фолликулярной части щитовидной железы. Помимо этих гормонов (биосинтез и функции которых будут рассмотрены ниже), в особых клетках – так называемых парафолликулярных клетках, или С-клетках щитовидной железы, синтезируется гормон пептидной природы, обеспечивающий постоянную концентрацию кальция в крови. Он получил название «кальцитонин». Впервые на существование кальцито-нина, обладающего способностью поддерживать постоянный уровень кальция в крови, указал в 1962 г. Д. Копп, который ошибочно считал, что этот гормон синтезируется паращитовидными железами. В настоящее время кальцитонин не только выделен в чистом виде из ткани щитовидной железы животных и человека, но и полностью раскрыта 32-членная АМКная последовательность, подтвержденная химическим синтезом. Кальцитонин человека содержит дисульфидный мостик (между 1-м и 7-м АМКными остатками) и характеризуется N-концевым цистеином и С-концевым пролинамидом. Кальцитонины быка, овцы, свиньи и лососевых рыб мало отличаются друг от друга как по структуре и концевым АМКам, так и по гипокальциемической активности. Биологическое действие кальцитонина прямо противоположно эффекту паратгормона: он вызывает подавление в костной ткани резорбтивных процессов и соответственно гипокальциемию и гипофосфатемию. Таким образом, постоянство уровня кальция в крови человека и животных обеспечивается главным образом паратгормоном, кальцитриолом и кальцитонином, т.е. гормонами как щитовидной и паращитовидных желез, так и гормоном – производным витамина D3. Это следует учитывать при хирургических лечебных манипуляциях на данных железах. Считается установленным, что все йодсодержащие гормоны, отличающиеся друг от друга содержанием йода, являются производными L-тиронина, который синтезируется в организме из АМКы L-тирозина. Из L-тиронина легко синтезируется гормон щитовидной железы тироксин, содержащий в 4 положениях кольцевой структуры йод. Следует отметить, что гормональной активностью наделены 3,5,3'-трийодтиронин и 3,3'-дийодтиронин, также открытые в щитовидной железе. Биосинтез гормонов щитовидной железы регулируется тиротропином – гормоном гипоталамуса.
В настоящее время еще полностью не изучены ферментные системы, катализирующие промежуточные стадии синтеза этих гормонов, и природа фермента, участвующего в превращении йодидов в свободный йод (2IДI2), необходимый для йодирования 115 остатков тирозина в молекуле тиреоглобулина. Последовательность реакций, связанных с синтезом гормонов щитовидной железы, была расшифрована при помощи радиоактивного йода [131I]. Было показано, что введенный меченый йод прежде всего обнаруживается в молекуле монойодтирозина, затем - дийодтирозина и только потом – тироксина. Эти данные позволяли предположить, что монойод- и дийодтирозины являются предшественниками тироксина. Однако известно также, что включение йода осуществляется не на уровне свободного тироксина, а на уровне полипептидной цепи тиреоглобулина в процессе его постсинтетической модификации в фолликулярных клетках. Дальнейший гидролиз тиреоглобулина под действием протеиназ и пептидаз приводит к образованию как свободных АМК, так и к освобождению йодтиронинов, в частности тироксина, последующее депонирование которого способствует образованию трийодтиронина. Эта точка зрения кажется более правдоподобной с учетом универсальности постсинтетической химической модификации при биосинтезе биологически активных веществ в организме.
Катаболизм гормонов щитовидной железы протекает по двум направлениям: распад гормонов с освобождением йода (в виде йодидов) и дезами-нирование (отщепление аминогруппы) боковой цепи гормонов. Продукты обмена или неизмененные гормоны экскретируются почками или кишечником. Возможно, что некоторая часть неизмененного тироксина, поступая через печень и желчь в кишечник, вновь всасывается, пополняя резервы гормонов в организме. Биологическое действие гормонов щитовидной железы распространяется на множество физиологических функций организма. В частности, гормоны регулируют скорость основного обмена, рост и дифференцировку тканей, обмен белков, углеводов и липидов, водно-электролитный обмен, деятельность ЦНС, пищеварительного тракта, гемопоэз, функцию сердечнососудистой системы, потребность в витаминах, сопротивляемость организма инфекциям и др. Точкой приложения действия тиреоидных гормонов, как и всех стероидов (см. далее), считается генетический аппарат. Специфические рецепторы – белки – обеспечивают транспорт тиреоидных гормонов в ядро и взаимодействие со структурными генами, в результате чего увеличивается синтез ферментов, регулирующих скорость окислительно-восстановительных процессов. Естественно поэтому, что недостаточная функция щитовидной железы (гипофункция) или, наоборот, повышенная секреция гормонов (гиперфункция) вызывает глубокие расстройства физиологического статуса организма.
Гипофункция щитовидной железы в раннем детском возрасте приводит к развитию болезни, известной в литературе как кретинизм. Недостаточная функция щитовидной железы в зрелом возрасте сопровождается развитием гипотиреоидного отека, или микседемы. У больных отмечаются слизистый отек, патологическое ожирение, резкое снижение основного обмена, выпадение волос и зубов, общие мозговые нарушения и психические расстройства. Кожа становится сухой, температура тела снижается; в крови повышено содержание глюкозы. Следует отметить еще одно поражение щитовидной железы – эндемический зоб. Болезнь обычно развивается у лиц, проживающих в горных местностях, где содержание йода в воде и растениях недостаточно. Недостаток йода приводит к компенсаторному увеличению массы ткани щитовидной железы за счет преимущественного разрастания соединительной ткани, однако этот процесс не сопровождается увеличением секреции тиреоидных гормонов. Повышенная функция щитовидной железы (гиперфункция) вызывает развитие гипертиреоза, «зоб диффузный токсический». При гиперфункции щитовидной железы и, в частности, токсическом зобе показано оперативное удаление всей железы или введение 131I (β- и γ-излу-чение частично разрушает ткань железы) и антагонистов тироксина, тормозящих синтез тиреоидных гормонов. К подобным веществам относятся, например, тиомочевина, тиоурацил (или метилтиоурацил).
Снижают функцию щитовидной железы тиоцианат и вещества, содержащие аминобензольную группу, а также микродозы йода. Оксиредуктазы ОКСИДОРЕДУКТАЗЫ, класс ферментов, катализирующих обратимые окислит.-восстановит. р-ции, в к-рых происходит перенос восстановит. эквивалентов (двух атомов Н, двух электронов или гидрид-иона Н-) от восстановителя (спе-цифич. субстрат р-ции) к окислителю (относительно не-специфич. субстрат), напр.:
АН 2 - восстановитель, В - окислитель П/клсы оксидоредуктаз (их 17) сформированы по типу окисляемого в-ва (восстановителя), подп/клсы - по типу окислителя (акцептора восстановит. эквивалента). Оксидоредуктазы всех подп/клсов, для к-рых акцептором служит не О2, а любое др. соед., наз. дегидрогеназами, или редуктазами, если акцептор О2- оксидазами. В тех случаях, когда атом О включается в состав субстрата, ферменты наз. оксигеназами (при включении в молекулу одного атома О монооксиге-назами, двух атомов О-диоксигеназами), если атом О включается в виде группы ОН-гидроксилазами. К оксидоредуктазам относится большая группа ферментов (ок. 20% от общего их числа). Многие оксидоредуктазы (ок. 170 ферментов) в качестве акцепторов используют никотинамидные коферменты (см. Ниацин)-никотинамидадениндинуклеотид (НАД) и никотин-амидадениндинуклеотидфосфат (НАДФ). Эти дегидрогена-зы (напр., алъдегиддегидрогеназа, лактатдегидрогеназа)выполняют важные ф-ции, участвуя в гликолизе, дыхании, брожении, а также на начальном этапе окислит, распада АМК при деградации белков. Нек-рые дегидрогена-зы АМК (напр., глутаматдегидрогеназа)могут катализировать синтез АМК, участвуя в ассимиляции NH3 микроорганизмами и растениями. Считается, что восстановит. эквиваленты от восстановленного НАД (т. е. от НАДН) переносятся в клетке на О2 через дыхат. цепь переноса электронов (см. Окислительное фосфорилирование), где своб. энергия этих эквивалентов расходуется для запасания энергии в виде макроэргич. связи АТФ; восстановит. эквиваленты НАДФН расходуются для биосинтетич. целей.
Ряд дегидрогеназ в качестве акцептора содержит химически прочно связанный с ферментом флавинмононуклеотид или флавинадениндинуклеотид (соотв. ФМН и ФАД; см. Рибофлавин). В таких флавопротеидах ФМН или ФАД восстанавливаются в результате окисления НАДН или НАДФН, а затем передают восстановит. эквиваленты др. компонентам цепи переноса электронов при дыхании, напр. цитохромам или непосредственно на О2. Др. продукт р-ций, катализируемых флавопротеидными оксидоредуктазами,-Н2О2. Ферменты, использующие Н2О2 в качестве акцепторов восстановит. эквивалентов (напр., каталаза), иаз. пероксидазами. (См. также Глутатионредуктаза, Липоксигеназы, Монофенол-монооксигеназы, Нитратредуктазы, Рибонуклеозид-дифос-фат-редуктазы, Сукцинатдегидрогеназа, Супероксиддисму-тазы, Тетрагидрофолатдегидрогеназа, Трансгидроге-наза, Цитохром-с-оксидаза.) Вит В3 Пантотеновая кислота в качестве витамина была открыта в 1933 г. Р. Уильямсом и соавт. в составе «биоса» – группы веществ природного происхождения, стимулирующих рост дрожжей. Он оказался чрезвычайно широко распространенным во всех живых объектах (микроорганизмы, растения, ткани животных), в связи с чем было предложено название «пантотеновая кислота» (от греч. pantoten – повсюду). В 1938 г. эти же авторы выделили ее из дрожжей и печени в высокоочищенном состоянии в форме кристаллической кальциевой соли, а в 1940 г. была расшифрована ее структура, подтвержденная химическим синтезом. Пантотеновая кислота является комплексным соединением β-аланина и 2,4-диокси-3,3-диметилмасляной кислоты.
Пантотеновая кислота представляет собой вязкую светло-желтую жидкость, хорошо растворимую в воде; она малоустойчива и легко гидро-лизуется по месту пептидной связи под действием слабых кислот и щелочей. При недостаточности или отсутствии пантотеновой кислоты у человека и животных развиваются дерматиты, поражения слизистых оболочек, дистрофические изменения желез внутренней секреции (в частности, надпочечников) и нервной системы (невриты, параличи), изменения в сердце и почках, депигментация волос, шерсти, прекращение роста, потеря аппетита, истощение, алопеция. Все это многообразие клинических проявлений пантотеновой недостаточности свидетельствует об исключительно важной биологической роли ее в метаболизме. Биологическая роль. Пантотеновая кислота входит в состав кофер-мента А, или коэнзима А (КоА). Название «коэнзим А» (кофермент ацилирования) связано с тем, что это соединение участвует в ферментативных реакциях, катализирующих как активирование, так и перенос ацетильного радикала СН3СО; позже оказалось, что КоА активирует и переносит также другие кислотные остатки (ацилы). В результате образования ацил-КоА происходит активация карбоновой кислоты, которая поднимается на более высокий энергетический уровень, создающий выгодные термодинамические предпосылки для ее использования в реакциях, протекающих с потреблением энергии. Строение КоА расшифровал Ф. Линен. В основе структуры лежит остаток 3'-фосфоаденозин-5'-дифосфата (отличается от АТФ наличием у 3'-гидроксила фосфатной группы), соединенный с остатком пантотеновой кислоты, карбонильная группа которой в свою очередь связана с остатком β-меркаптоэтиламина (тиоэтиламина).
Реакционноспособным участком молекулы КоА в биохимических реакциях является SH-группа, поэтому принято сокращенное обозначение КоА в виде SH-KoA. О важнейшем значении КоА в обмене веществ (как будет показано далее – см. главы 9–11) свидетельствуют обязательное непосредственное участие его в основных биохимических процессах, окисление и биосинтез высших жирных кислот, окислительное декарбоксилирование α-кетокислот (пируват, α-кетоглутарат), биосинтез нейтральных жиров, фосфолипидов, стероидных гормонов, гема гемоглобина, ацетилхолина, гиппуровой кислоты и др. Распространение в природе и суточная потребность. Уже отмечалось широкое, повсеместное распространение пантотеновой кислоты в природе. Основными пищевыми источниками ее для человека являются печень, яичный желток, дрожжи и зеленые части растений. Пантотеновая кислота синтезируется, кроме того, микрофлорой кишечника. Суточная потребность в пантотеновой кислоте для взрослого человека составляет 3–5 мг
|
|||||||||
|
Последнее изменение этой страницы: 2017-01-24; просмотров: 365; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.188.40.207 (0.031 с.) |