
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Кинетика фер-тативных процессов ур-ние михаэлис-Мэнтен
Общие принципы кинетики хим р-ций применимы и к ф-тативным р-циям. Известно, что любая хим р-ция хар-ризуется константой термодинамич равновесия. Она выражает состояние химического равновесия, достигаемого системой, и обозначается Кр. Так, для р-ции:
константа равновесия равна произведению конц-ций образующихся в-в, деленному на произведение конц-ции исходных в-в. Значение константы равновесия обычно нах из соотнош констант скоростей прямой (k+1) и обратной (k– 1) р-ций, т.е. Кp = k+1/k–1. В состоянии равновесия скорость прямой р-ции: v+1 = k + 1[ А ] • [ B ] равна скорости обратной р-ции: v–1 = k – 1 [ С ] • [ D ], т. е. v+1 = v–1 соотв-енно k+1[А]•[B] = k–1[С]•[D], или
Т.об., константа равновесия = отнош констант скоростей прямой и обратной р-ций. Величину, обратную константе равновесия, принято называть субстратной константой, или, в случае ф-тативной р-ции, константой диссоциации ф-т–субстратного комплекса, и обозначать символом KS. Так, в р-ции
т.е. KSравна отношению произведения конц-ции ф-та и субстрата к конц-ции ф-т-субстратного комплекса или отнош констант скоростей обратной и прямой р-ций. Константа KS зависит от хим природы субстрата и ф-та и определяет степень их сродства. Чем ниже значение KS, тем выше сродство ф-та к субстрату. При низкой конц-ции субстрата зависимость скор р-ции от конц-ции субстрата явл почти линейной и подчиняется кинетике первого порядка. Это означает, что скорость р-ции S —> Р прямо пропорц конц-ции субстрата S и в любой момент времени t определяется след кинетическим ур-нием:
При высокой конц-ции субстрата скор р-ции максимальна, стан-тся пост и не зависящей от конц-ции субстрата [ S ]. В этом случае р-ция подчиняется кинетике нулевого порядка v = k" (при полном насыщении ф-та субстратом) и целиком определ-ся конц-цией ф-та. Различают р-ции 2-ого порядка, скорость к-рых пропорциональна произведению конц-ций двух реагирующих в-в. В определенных условиях при нарушении пропорциональности говорят иногда о р-циях смешанного порядка. Изучая явление насыщения, Л. Михаэлис и М. Ментен разработали общую теорию ф-тативной кинетики. Они исходили из предположения, что ф-тативный процесс протекает в виде след хим р-ции:
Из ур-ния Михаэлиса–Ментен следует, что при высокой конц-ции субстрата и низком значении KS скор р-ции явл максим, т.е. v = Vmax. При низкой конц-ции субстрата, напротив, скорость р-ции оказывается пропорциональной конц-ции субстрата в каждый данный момент (р-ция первого порядка). Следует указать, что ур-ние Михаэлиса–Ментен в его классическом виде не учитывает влияние на скорость ф-тативного проц продуктов р-ции, напр в р-ции
В числителе представлены константы скоростей распада комплекса ES в двух направлениях (в сторону исходных Е и S и в сторону конечных продуктов р-ции Е и Р). Отношение k–1/ k+1представляет собой константу диссоциации ф-тсубстратного комплекса KS, тогда: Отсюда вытекает важное следствие: константа Михаэлиса всегда больше константы диссоциации ф-т-субстратного комплекса KSна величину k+2/k+1. Для определения численного значения Кm обычно находят ту конц-цию субстрата, при к-рой скорость ф-тативной р-ции v составляет половину от максимальной Vmax, т.е. если v = 1/2 Vmaх. Подставляя значение v в ур-ние Бриггса–Холдейна, получаем:
разделив обе части ур-ния на Vmах, получим
Т.об., константа Михаэлиса численно равна конц-ции субстрата (моль/л), при к-рой скорость данной ф-тативной р-ции составляет половину от максимальной. Определение величины Кm имеет важное значение при выяснении механизма действия эффекторов на активность ф-тов и т.д. Константу Михаэлиса можно вычислить по графику (рис. 4.13). Отрезок на абсциссе, соотв-ующий скорости, равной половине максимальной, будет представлять собой Кm. Пользоваться графиком, построенным в прямых координатах зависимости начальной скорости р-ции v0 от начальной конц-ции субстрата [S0], неудобно, поскольку максимальная скорость Vmaxявл в данном случае асимптотической величиной и определяется недостаточно точно.
Для более удобного графического представления экспериментальных данных Г. Лайнуивер и Д. Бэрк преобразовали ур-ние Бриггса–Хол-дейна по методу двойных обратных величин исходя из того принципа, что если существует равенство м/у двумя какими-либо величинами, то и обратные величины также будут равны. В частности, если
то после преобр-ния получаем ур-ние:
к-рое получило название ур-ния Лайнуивера–Бэрка. Это ур-ние прямой линии: у = ах + b. Если теперь в соотв-ии с этим ур-нием построить график в координатах 1/v (y) от l/[S] (x), то получим прямую линию (рис. 4.14), тангенс угла наклона к-рый будет равен величине Km/Vmax; отрезок, отсекаемый прямой от оси ординат, представляет собой l/Vmax(обратная величина максимальной скорости). Если продолжить прямую линию за ось ординат, тогда на абсциссе отсекается отрезок, соотв-ующий обратной величине константы Михаэлиса – 1/Кm (см. рис. 4.14). Т.об., величину Кm можно вычислить из данных наклона прямой и длины отрезка, отсекаемого от оси ординат, или из длины отрезка, отсекаемого от оси абсцисс в области отрицательных значений. Следует подчеркнуть, что значения Vmax, как и величину Кm, более точно, чем по графику, построенному в прямых координатах, можно определить по графику, построенному по методу двойных обратных величин. Поэтому данный метод нашел широкое применение в современной энзимологии. Предложены также аналогичные графические способы определения Кm и Vmaxв координатах зависимости v от v/[S] и [S]/v от [S]. Следует отметить нек-рые ограничения применения ур-ния Ми-хаэлиса–Ментен, обусловленные множественными формами ф-тов и аллостерической природой ф-та. В этом случае график зависимости начальной скорости р-ции от конц-ции субстрата (кинетическая кривая) имеет не гиперболическую форму, а сигмоидный хар-р наподобие кривой насыщения гемоглобина кислородом. Это означает, что связывание одной мол-лы субстрата в одном каталитическом центре повышает связывание субстрата с другим центром, т.е. имеет место кооперативное вз-действие, как и в случае присоединения кислорода к 4 субъединицам гемоглобина. Для оценки конц-ции субстрата, при к-рой скорость р-ции составляет половину максимальной, в условиях сигмоидного хар-ра кинетической кривой обычно применяют преобр-нное ур-ние Хилла:
|
||||||
|
Последнее изменение этой страницы: 2017-01-24; просмотров: 158; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.16.81.94 (0.008 с.) |



 где [S] – молярная конц-ция субс-та S; –d[S]/dt – скор убыли субстрата; k' – константа скорости р-ции, к-рая имеет размерность, обратную единице времени (мин–1 или с–1).
где [S] – молярная конц-ция субс-та S; –d[S]/dt – скор убыли субстрата; k' – константа скорости р-ции, к-рая имеет размерность, обратную единице времени (мин–1 или с–1).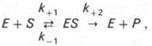 т.е. ф-т Е вступает во вз-действие с субстратом S с обр-нием промежуточного комплекса ES, к-рый далее распадается на свободный ф-т и продукт р-ции Р. Матем обработка на основе закона действующих масс дала возм-сть вывести ур-ние, названное в честь авторов ур-ем Михаэлиса–Ментен, выражающ кол-ное соотнош м/у конц-цией субстрата и скор ф-тативной р-ции:
т.е. ф-т Е вступает во вз-действие с субстратом S с обр-нием промежуточного комплекса ES, к-рый далее распадается на свободный ф-т и продукт р-ции Р. Матем обработка на основе закона действующих масс дала возм-сть вывести ур-ние, названное в честь авторов ур-ем Михаэлиса–Ментен, выражающ кол-ное соотнош м/у конц-цией субстрата и скор ф-тативной р-ции: где v – скор р-ции при данной конц-ции субстрата [S]; KS– константа диссоциации ф-т-субстратного комплекса, моль/л; Vmax– максим скор р-ции при полном насыщении ф-та субстратом.
где v – скор р-ции при данной конц-ции субстрата [S]; KS– константа диссоциации ф-т-субстратного комплекса, моль/л; Vmax– максим скор р-ции при полном насыщении ф-та субстратом. и носит несколько ограниченный хар-р. Поэтому были предприняты попытки усовершенствовать его. Так, было предложено ур-ние Бриггса-Холдейна:
и носит несколько ограниченный хар-р. Поэтому были предприняты попытки усовершенствовать его. Так, было предложено ур-ние Бриггса-Холдейна: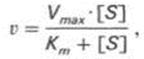 где Кm представляет собой константу Михаэлиса, являющуюся экспериментально определяемой величиной. Она может быть представлена следующим ур-нием:
где Кm представляет собой константу Михаэлиса, являющуюся экспериментально определяемой величиной. Она может быть представлена следующим ур-нием:
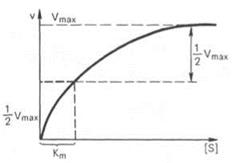 Кривая ур-ния Михаэли-са-Ментен: гиперболическая зависимость начальных скоростей катализируемой ф-том р-ции от конц-ции субстрата.
Кривая ур-ния Михаэли-са-Ментен: гиперболическая зависимость начальных скоростей катализируемой ф-том р-ции от конц-ции субстрата.


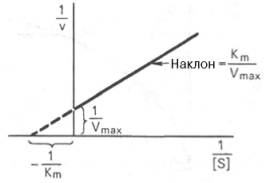 График Лайнуивера-Бэрка.
График Лайнуивера-Бэрка. или
или 




