
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Опыт 2. Свойства солей угольной кислоты.Содержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
а) В сухие пробирки поместить по 1 микрошпателю: CaCO3, Na2CO3, NaHCO3.. В каждую прибавить по 5-6 капель 1н раствора соляной кислоты. Наблюдать характерное шипение выделяющегося газа. Написать уравнения реакции. б) В пробирки внести по 4-5 капель растворов солей CaCl2, BaCl2, Pb(NO3)2. В каждую добавить такой же объем раствора Na2CO3. Что наблюдается? Составить уравнения реакций. в) В пробирки налить по 2 мл дистиллированной воды и по 2-3 капли раствора фенолфталеина. Затем в каждую внести по одному микрошпателю сухих солей: в одну - NaHCO3, в другую - Na2CO3. Отметить различие в интенсивности окраски индикатора. Объяснить наблюдения, используя табличные значения констант диссоциации (Кдис.) угольной кислоты. Составить уравнения гидролиза солей, рассчитать константы гидролиза. г) В одну пробирку налить 3-4 капли раствора соли меди, в другую - столько же соли алюминия. Затем в каждую добавить по 2-3 капли карбоната натрия. Наблюдать выпадение в осадок соответственно (CuOH)2CO3 и Al(OH)3, а также выделение углекислого газа в обеих пробирках. Объяснить наблюдения. Составить уравнения реакций, зная, что вода является участником реакции. д) Собрать прибор из пробирки и газоотводной трубки. В пробирку поместить 2-3 микрошпателя малахита (карбоната гидроксомеди (II) [CuOH]2CO3). Газоотводную трубку опустить в пробирку с 7-10 каплями известковой воды и осторожно нагреть пробирку с малахитом. Наблюдать выделение газа, изменение цвета соли, появление капель воды на выходе из пробирки с солью и помутнение известковой воды. Объяснить происходящие явления, написать уравнения реакций. Опыт 3. Получение кремниевой кислоты. а) В пробирку налить концентрированный раствор метасиликата натрия 5 мл и добавить 3 мл 20%-ного раствора соляной кислоты. Хорошо перемешать стеклянной палочкой. Вследствие образования кремниевой кислоты содержимое пробирки через некоторое время превращается в студнеобразную массу. Составить уравнения реакции. Сделать вывод о свойствах кремниевой кислоты. б) В пробирку налить 5 мл концентрированного раствора метасиликата натрия и пропустить в него углекислый газ из аппарата Киппа до появления студнеобразного осадка. Составить уравнение реакции.
Опыт 4. Гидролиз силикатов. В пробирку с 1 мл раствора метасиликата натрия внести 1-2 капли раствора фенолфталеина. Наблюдать изменение окраски индикатора. Какая среда в растворе соли? Составить уравнение реакции гидролиза по первой ступени.
Контрольные вопросы: 1. Написать электронные формулы атомов углерода и кремния. Какие степени окисления характерны для этих элементов? 2. В чем сходство и различие в свойствах углерода и кремния? 3. Какого типа химические связи образует углерод в органических соединениях? В каком гибридном состоянии может находиться углерод? 4. Какие простые вещества образует углерод? Чем различаются их структуры? 5. Какие оксиды образуют углерод и кремний? Какие кислоты и соли им соответствуют? 6. Какую среду имеют водные растворы карбоната и гидрокарбоната натрия? Дать объяснение, составить уравнения реакций гидролиза. 7. Какая среда в водном растворе силиката натрия? Составить уравнение гидролиза. 8. Какие соединения углерода входят в состав: воздуха, горных пород, подземных вод? 9. Какие из следующих солей растворяются в соляной кислоте: хромат бария, карбонат бария, сульфат бария? Почему? 10. Какая из солей образует осадок при взаимодействии с соляной кислотой: силикат натрия, карбонат натрия, сульфат натрия? 11. С какими из указанных веществ будет взаимодействовать оксид углерода (П): MgO, O2, H2, Cl2, KOH? Написать уравнения происходящих реакций. 12. Составить уравнения реакций, при помощи которых можно осуществить следующие превращения: CaCO3 ® CaO ® Ca(OH)2 ® Ca3(PO4)2 13. Составить уравнения реакций, при помощи которых можно осуществить следующие превращения: а).CO ® CO2 ® Na2CO3 ® CaCO3; б) Si® SiO2 ® H2SiO3 ®Na2SiO3 14. Coставить уравнения реакций, при помощи которых можно осуществить следующие превращения: а) CH4 ® CO2 ® MgCO3 ® MgCl2 ; б) Na2SiO3 ® H2SiO3 ® SiO2 ® CaSiO3 15. Какие полимерные кислоты образует кремний? 16. Приведите формулу оконного стекла. Написать уравнение реакции получения оконного стекла. 17. В колбах без этикеток находятся следующие соли: хлорид натрия, карбонат натрия и сульфат натрия. Как определить: в какой колбе какая соль? 18. Имеются три цилиндра, наполненные газами: оксидом азота (II), оксидом углерода (II), оксидом углерода (IV). Как определить: какой газ находится в каждом цилиндре? 19. Как доказать кислотный характер диоксида кремния?
20. Какой осадок образуется при добавлении к силикату натрия раствора нитрата аммония?
Азот, фосфор.
Фосфор на валентном уровне имеет незаполненные 3d-орбитали, поэтому его валентность повышается до 5 и возможны sp3d2, sp3d- и sp3 - типы гибридизации. При химических реакциях азот и фосфор не теряют электронов и не превращаются в катионы. Незначительное сродство к электрону объясняет их неспособность превращаться в элементарные анионы. В обычных условиях азот встречается в виде простого вещества N2 - бесцветный газ, без запаха, плохо растворим в воде и органических растворителях, tкип. = -195,8°C. Молекула N2 исключительно прочна (Едисс. = 945 кДж/моль) за счет тройной связи между атомами азота NºN и поэтому N2 обладает низкой реакционной способностью. Элементарный фосфор химически более активен, чем азот и в свободном состоянии в природе не встречается. Атомы фосфора объединяются в двухатомные Р2, четырехатомные Р4 и полимерные Р2n - молекулы. Молекулы Р2 (аналогичные N2) существуют лишь при температурах выше 1000°С, распад на атомы начинается лишь выше 2000°С. Известны несколько аллотропных модификаций фосфора. Белый фосфор - кристаллический порошок, ядовит, самовозгорается на воздухе при 50 °С, поэтому хранят его под водой и в темноте. При длительном нагревании (280 - 340°С) переходит в красный фосфор - кристаллический порошок, устойчив (температура самовозгорания более 250 °С), не ядовит, химически инертен, используется в спичечном производстве. Черный фосфор можно получить из белого при t=200°С и Р=12000 атм. Черный фосфор химически устойчив, не ядовит, температура самовозгорания более 400°С. В технике белый фосфор получают прокаливанием фосфата кальция с углем и песком в электропечах при 1500°С: 2Ca3(PO4)2 + 10 C + 6 SiO2 = 6 CaSiO3 + 10 CO + P4 При обычных условиях на воздухе тонко измельченный белый фосфор самовоспламеняется: Р4 + 5О2 = 2Р2О5 При недостатке кислорода образуется оксид фосфора (III): Р4 + 3 О2 = 2Р2О3 При взаимодействии с хлором фосфор образует хлориды фосфора (III) и (V), которые легко гидролизуются: 2Р + 3Cl2 = 2PCl3 2P +5Cl2 + 2PCl5, PCl3 + 3H2O = H3PO3 + 3HCl PCl5 + 4H2O = H3PO4 + 5HCl Азот и фосфор при нагревании с металлами образуют нитриды и фосфиды - электропроводные твердые термостойкие кристаллы с высокими температурами плавления. Например, при взаимодействии с кальцием азот образует нитрид кальция, который легко гидролизуется с образованием аммиака NH3: 3Ca + N2 = Ca3N2 Ca3N2 + 6H2O = 3Ca(OH)2 + 2NH3
Фосфор при взаимодействии с активными металлами образует фосфиды, например: 3Li + P = Li3P Фосфиды разлагаются с образованием фосфина РН3 – ядовитого газа плохо растворимого в воде: Ca3P2 + 6H2O = 3Ca(OH)2 + 2PH3 Аммиак – бесцветный газ с резким запахом, хорошо растворим в воде и раствор имеет щелочную среду:
NH4OH - слабое основание, поэтому все соли аммония гидролизуются. Соли аммония термически неустойчивы и при нагревании разлагаются:
C кислородом азот образует целый ряд оксидов, отвечающих степеням окисления: +1, +2, +3, +4, +5. Далее, в таблице 1, приведена характеристика этих оксидов и их свойств. Высшие оксиды азота являются кислотными и, соединяясь с водой, образуют следующие кислоты: N2O3 + H2O = 2HNO2 2NO2 + H2O = HNO3 + HNO2 N2O5 + H2O = 2HNO3
Азотистая кислота непрочная и при нагревании разлагается по уравнению: 2HNO2 = NO + NO2 + H2O Азот проявляет различные степени окисления и для его соединений характерны окислительно-восстановительные реакции (см. диаграмму Латимера для азота).
Таблица Получение и свойства оксидов азота
Соли азотистой кислоты (нитриты) разлагаются при действии сильных кислот: 2KNO2 + H2SO4 = K2SO4 + NO + NO2 + H2O В кислой среде под действием анионов-окислителей (ClO3--, MnO4, Cr2O72) нитриты окисляются по схеме NO2- + H2O - 2e = NO3- + 2H+ (j°NO3-/ NO2- = 0,93 в), а при действии восстановителей (I-, S2-, Fe2+ и т.д.) - восстанавливаются: NO2- + 2H+ - 1e =NO + H2O (j°NO2- / NO = 0,99 в)
Диаграмма Латимера для азота: а) в кислой среде
б) в щелочной среде
-0,86 0,88 -0,46 +0,76 +0,94 -3,4
+0,16 +0,73 -2,86
Наиболее важными соединениями азота являются азотная кислота и её соли - нитраты. С химической точки зрения HNO3 - сильная кислота и сильный окислитель. В зависимости от концентрации HNO3 и химической активности реагирующего с ней вещества продукты восстановления самой кислоты могут быть разными. Металлы, стоящие правее водорода, восстанавливают азотную концентрированную кислоту до NO2, а разбавленную - до NO по схемам: NO3- (конц.) + 2H+ + 1e ® NO2 + H2O NO3- (разб.) + 4H+ + 3e ® NO + 2H2O Активные металлы восстанавливают концентрированную HNO3 до N2O или N2: 2NO3-(конц.) + 10 H+ + 8e ® N2O + 5H2O 2NO3-(конц.) + 12H+ + 10e ® N2 + 6H2O, а разбавленную HNO3 - до солей аммония: NO3-(разб.) + 10H+ + 8e ® NH4+ + 3H2O
То есть, чем более разбавлена азотная кислота и чем активнее металл, тем глубже идет реакция восстановления. Следует учитывать, что наряду с основным продуктом образуются примеси других продуктов восстановления. Концентрированная азотная кислота пассивирует чистое железо, хром и алюминий, т.к. на поверхности металлов образуются плотные оксидные пленки этих металлов, препятствующие протеканию реакции. Металлы Au, Pt, Ir, Rh, Na, Te, Nb с азотной кислотой не взаимодействуют. Другие металлы при окислении азотной кислоты обычно образуют нитраты. Важнейшее их свойство - способность разлагаться при нагревании по следующим схемам:
Неметаллы обычно восстанавливают HNO3 до NO, сами при этом окисляются ею до соответствующих кислот (сера - до H2SO4, уголь - до H2CO3, фосфор - до H3PO4). Фосфор образует с кислородом два оксида: Р2О3 – оксид фосфора (III) и Р2О5 – оксид фосфора (V) Характер оксидов кислотный, им соответствуют кислоты: фосфористая (Н3РО3) и фосфорная (Н3РО4) Окислительно- восстановительные свойства соединений фосфора отражены в диаграмме Латимера для фосфора.
Диаграмма Латимера для фосфора а) в кислой среде -0,276 -0,50 -0,51 -0,06
б) в щелочной среде -1,3 -1,665 -1,82 -0,874
Оксид фосфора (III) Р2О3, растворяясь в холодной воде, образует фосфористую кислоту: Р2О3 + 3Н2О (холодная) = 2Н3РО3, обладающую как восстановительными, так и окислительными свойствами. При действии таких сильных окислителей, как кислород, галогены, положительные ионы металлов, в том числе благородных металлов, она окисляется до фосфорной кислоты H3PO4. При действии сильных восстановителей, таких, как щелочные и щелочноземельные металлы, цинковая пыль и др., Н3РО3 восстанавливается до фосфина РН3. Фосфин - чрезвычайно ядовитый газ, сильный восстановитель, на воздухе самопроизвольно воспламеняется: PH3 + 2O2 = H3PO4 Соли фосфористой кислоты называются фосфитами, соли фосфорной кислоты - фосфатами. Оксид фосфора (V) - Р2О5 - белое кристаллическое вещество, типичный кислотный оксид, может присоединять одну, две или три молекулы воды, образуя соответственно три типа кислот: P2O5 + H2O = 2HPO3 (метафосфорная кислота) P2O5 + 2H2O = H4P2O7 (дифосфорная кислота) P2O5 + 3H2O = 2H3PO4 (ортофосфорная кислота) Наибольшее значение имеет ортофосфорная кислота Н3РО4 - белое, твердое вещество. Это кислота средней силы,диссоциирует ступенчато (К1=7,6×10-3; К2 = 6,2 × 10-3; К3 = 4,4 × 10-13), растворима в воде, образует три типа солей: дигидрофосфаты (NaH2PO4), гидрофосфаты (Na2HPO4) и ортофосфаты (Na3PO4). В водных растворах фосфаты гидролизуются. Все дигидрофосфаты растворимы в воде. Из гидрофосфатов и фосфатов в воде растворимы только соли щелочных металлов и аммония. Лабораторная работа № 13.
|
||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-08-16; просмотров: 499; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.188.188.152 (0.009 с.) |

 Азот (1s22s22p3) и фосфор (1s22s22p63s23p3) являются типичными элементами V А группы. Они относятся к неметаллам, являются электронными аналогами, в невозбужденном состоянии имеют по 3 неспаренных электрона и проявляют валентность равную трем. У азота четыре валентные орбитали, которые могут находиться в состоянии sp3-, sp2 -или sp- гибридизации, и максимальная валентность азота может быть равна 4.
Азот (1s22s22p3) и фосфор (1s22s22p63s23p3) являются типичными элементами V А группы. Они относятся к неметаллам, являются электронными аналогами, в невозбужденном состоянии имеют по 3 неспаренных электрона и проявляют валентность равную трем. У азота четыре валентные орбитали, которые могут находиться в состоянии sp3-, sp2 -или sp- гибридизации, и максимальная валентность азота может быть равна 4.
 NH3 + H2O NH4OH NH4+ + OH-
NH3 + H2O NH4OH NH4+ + OH- (NH4)3PO4 3NH3 + H3PO4
(NH4)3PO4 3NH3 + H3PO4 NH4NO3 N2O + 2H2O
NH4NO3 N2O + 2H2O NH4NO2 N2 + 2H2O
NH4NO2 N2 + 2H2O 2NO2 N2O4;
2NO2+H2O = HNO2+HNO3;
3NO2+H2O = 2HNO3+NO;
4NO2+2H2O+O2= 4HNO3;
2NO2+2NaOH=NaNO2+NaNO3+H2O;
2NO2 N2O4;
2NO2+H2O = HNO2+HNO3;
3NO2+H2O = 2HNO3+NO;
4NO2+2H2O+O2= 4HNO3;
2NO2+2NaOH=NaNO2+NaNO3+H2O;






 (NO2)
(NO2)

 NH3 N2H4 NH2OH
NH3 N2H4 NH2OH
 левее Mg MeNO2 + O2
левее Mg MeNO2 + O2 MeNO3 Mg - Cu MeO + NO2 + O2
MeNO3 Mg - Cu MeO + NO2 + O2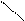
 правее Cu Me + NO2 + O2
правее Cu Me + NO2 + O2
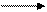
 H3PO4 H3PO3 H3PO2 P PH3
H3PO4 H3PO3 H3PO2 P PH3




