Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Пенообр-ли в пр-ве пастильн. Изд. И сбив. КонфСодержание книги
Поиск на нашем сайте
В ассорт-т КИ вх. значит-е кол-во видов изделий пористой стр-ры (пастила, зефир, сбивные конфеты и т. п.). Для получения такой стр-ры в рец-ру этих изд-й вводят пенообр-ли, а в рецептуру халвы для подобной цели предусмотрено внесение экстракта мыльного корня. Пенообр-ли из белков молока не уступают яичному белку; кровяной альбумин получают из сыворотки крови, высушенной распылительным сп-бом. В кач-ве пенообр-лей в конд. пр-ти прим-ся яич. белки, препар. из белков молока, кровян. альбумин, желатин, экстракт мыльного корня. Яичный белок. Его используют как в натуральном, так и в консервированном виде - высушенный или замороженный. Значительно меньшее применение находят белки, законсервированные сахаром. Перед использованием мороженый белок оттаивают и фильтруют. Сухой белок растворяют в холодной воде. Соотношение белка и воды зависит от пенообразующей способности данной партии белка и определяется экспериментально. Замороженный яичный белок хранят при температуре не выше минус 12° С и относительной влажности воздуха 80-85%, сухой - при температуре от 10 до минус 2° С и относительной влажности воздуха не выше 70%. Белок яйца составляет ≈ 92,6 % СВ. При сильном сбив. он увелич. в объеме за счет насыщ-я массы пузырьками воздуха. Пенообразующ. сп-ть белков при постепенном + воды ↑ся. При + сах. или жира пенообраз. сп-ть белков ↓ся. Мыльный корень. Он представляет собой корневище растения мыльника, произрастающего на Украине и в Средней Азии. Этот корень содержит значительное количество (4—15%) сапонина — поверхностно-активного вещества, являющегося пенообразователем. Прежде мыльный корень использовали для стирки вместо мыла. Отсюда и произошло его название. Сапонин является глюкозидом и при гидролизе выделяет глюкозу. Растворы сапонина дают обильную стойкую пену. Многие сапонины обладают гемолитическим действием, поэтому применение мыльного корня строго ограничено. Вред. действие сапонина уменьшается в присутствии жиров и сопутствующих им веществ (лецитина и т. п.)- Поэтому отвар мыльного корня разрешается применять в производстве халвы, которая содержит значит-е кол-во жира. Мыльный корень поступает на конд. фабрики в высушенном виде, обрезками длиной 15-20 см. Вл-ть корня должна быть не выше 13%. Корень не должен быть плесневелым и не должен иметь других видов порчи.
Пенообразователи из белков молока. Прим-ся как заменители яич. белка. Получ-е пенообр-лей из белков молока основано на щелоч., кислотном или ферментативном гидролизе белкового комплекса молока. Продукт гидролиза высушивают. По пенообразующ. сп-ти он не уступает яичному белку. Кровяной альбумин. Представляет собой сыворотку крови, высуш. распылительным способом. Прим-ся кровян. альбумин в кач-ве пенообр-ля. Желатин. В конд. пром-ти исп-ся не только как студнеобр-ль, но и как пенообраз-ль. Пенообразующ. сп-ть желатина зав. от содерж. в нем глюкозы. Чем больше глюкозы, тем выше пенообразующ. и ниже студнеобразующая сп-ть.
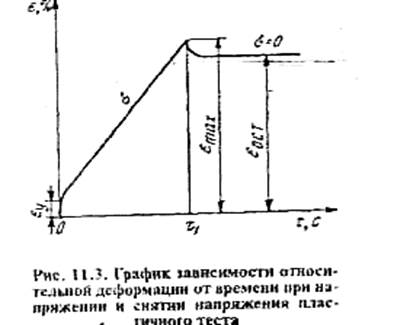
23. ХАР-КА ФИЗ-ХИМ СВ-ТВ СЫРЬЯ ДЛЯ ПР-ВА САХ.ПЕЧ. ВЛИЯНИЕ КОМП-ТОВ РЕЦ-РЫ И ПАР-РОВ ЗАМЕСА... Сах. печ. отлич-ся знач-й пористостью, хрупкостью, хорошей набух-тью. Изготавл. его из пластич. теста при опред-х технол. режимах. Наиб. важной стадией технол. процесса яв-ся замес теста, при кот. происх. смеш-е целого ряда рец-х комп-тов и образ-е кл-го каркаса.Чем > в тесте своб. воды, тем быстрее при перемеш. с мукой происх. образ-е теста. Для обра-я пластич. теста с ограниченно набухш. белками муки τ замеса д. б. миним-й и достаточной для формир-я однородного теста. Влияние муки. Ведущ. роль в образ-ии теста принадлежит белков. в-вам пш. муки, кот. в присут. воды способны набухать. При этом нераствор. в воде глиадинов. и глютенинов. фракции белка при замесе образ. белков. стр-рный каркас, кот. в виде тонк. пленок и нитей пронизывает всю массу теста. Из св-тв муки наиб. важн. яв-ся кол-во и кач-во кл-ны. От содерж. и кач-ва кл-ны в знач. степени зав. водопоглотительная сп-ть муки, а следов-но, влаж-ть теста и его структурно-механич. св-ва. Чем выше кач-во кл-ны, тем больше мука поглощ. воды при замесе теста. ↑ет влаж. теста, следов-но удлиняется процесс выпечки. При исп-ии муки с сильной кл-ной наблюд. деформация изд-й в процессе выпечки. П.э. для получ. рыхлого, пластично-вязкого теста необх. исп-ть пш. муку со слабой и средней по кач-ву кл-ной, а для упруго-эластич. теста — муку с сильной кл-ной. Влияние сахара. В вод. р-ре мол-лы сахаров покрыв-ся гидратными оболочками, что ↑ет их межмолекулярный объем, ↓ет скорость диффузии при осмотич. набух. белков муки. Особенно высокогидратированными яв-ся мол-лы сах-зы. При темп-ре 20 °С они связыв. и удерж. от 8 до 12 мол-л воды. След-но, чем > сахара в рец-ре теста, тем < в его жидкой фазе своб. воды, участв-щей в 1ую очередь в гидратации и набух. коллоидов муки. Для замеса сах. теста исп-ся мало воды и много сахара. При замесе сах. теста своб. влага отсутствует. Этим и объясняется огранич-е набух-е белков муки. Кроме того, сахар ↑ет осмотич. давл. в жид. фазе теста, что также ↓ет набух. коллоидов муки. Т.о., изменяя содерж. сах. в тесте, м/о регулировать процесс набух. белков и крахм. муки и получ. тесто с различ. физ. св-вами. Влияние жира. Важн. роль в образ. теста играют жиры. При этом имеет знач-е не только хим. состав жира, но и его физич.сост-е. Жиры д.быть пластичными. В этом случае они образ. в тесте тончайшие пленки, обволакивающие и смазывающ. частицы муки. При пр-ве печ. в тесто + от 5 до 35 % жира к m муки (в зав-ти от сорта изделий). Значит-я часть этого жира, если он находится в тесте в расплавленном сост., связ-ся кл-ной и крахм. Мех-зм взаимодействия липидов муки и вносимых жиров с комп-тами теста в значит-й мере зав. от хим. состава и св-тв исп-го жира и муки. Важн. роль при этом играют входящ. в состав жира триглицериды насыщ. и ненасыщ. к-т. Чем >содержание в жире триглицеридов ненасыщ. жир. к-т, тем он > сорбируется белками.Адсорбируясь на пов-ти белков. мицелл и крахм. зерен, жир препятствует набух. коллоидов муки и ↑ет содерж-е жидк. фазы-теста. →ослабл-ся св. между комп-тами тв. фазы теста→более пластичное. Влияние воды. Вода способствует набух. коллоидов муки, раствор-ю составн. частей муки и кристаллич. сырья, вносимого в тесто. Кол-во воды, идущ. на замес, зависит от вида теста и водопоглотит-й сп-ти муки, кот. в свою очередь зав. от кол-ва и кач-ва кл-ны, влаж-ти, выхода и крупноты помола муки, кот. при ↓ии вл-ти муки на 1 %, а также с ↑ем выхода муки, ↑ся на 1,8...1,9%. Чем крупнее частицы, тем < их удел. пов-ть, след-но, они связ-ют < воды за дан. отрезок времени.На водопоглот. сп-ть муки оказ. влияние присутствующ. в тесте др. в-ва, прежде всего сах. и жир. Мол-лы сах. связ. большое кол-во мол-л воды, ↓ая набухание коллоидов муки. Водопог-ая сп-ть муки при + 1 % сах. ↓ся на 0,6 %. С ↑ем доли сахара в тесте кол-во коллоидно-связ-ой воды будет ↓ся, а кол-во гидратированной мол-ми Сахаров воды — ↑ся, что разжижает тесто. На замес сах. теста часто поступает эмульсия, в кот. мол-лы воды полностью гидратированы мол-ми сах-зы и др. раствор-х в-тв. Отсутствие своб. воды огранич. набух-е коллоидов муки, что позволяет получ. пластич. тесто при небольшом кол-ве воды.Вл-ть сах. теста из муки высш. и 1 сортов при непр. замесе д.быть 15... 17 %, при период. замесе - 16,5...18,5 %. Влияние темп-ры. Темп-ра играет важн. роль в образ-ии теста с опр-ми физ. св-вами. С ↑ем темп-ры теста ↑ся частота колеб-ий отд-х цепочек макромол-л белка и крахм., ↑ скорость диффузии мол-л воды, происх. частич. дегидратация мол-л Сах., что ↑ет долю своб. воды. Все эти проц. способств. более полному набух. коллоидов муки и раствор. кристаллич. сырья. Для получ. пластич. теста замес осущ-ют при пониж. темп-ре смеси сырья (19...25 °С). Влияние продолж-ти замеса. Перемеш-е составных комп-тов теста в нач. стадии замеса вызывает смеш-е муки, воды и др. видов сырья и слипание набухающ. частичек муки в сплошную массу теста. Перемеш-е ускор. раствор-е кристаллич. сырья, набух-е коллоидов муки, способствуя более частым контактам частичек муки и пленок воды. При перемеш. достигается равномерное распред-е всех видов сырья в тесте, его однородность, что обеспеч. одноврем-е протек-е коллоидных и биохим. процессов во всей массе теста. Т. о., перемеш. (как технол. фактор) способств. и ускор. образ-е в тесте кл-го стр-го каркаса. τ замеса зав. от типа теста (сах. или затяж.). Для образ-я пластич. теста с огранич. набухш. белками муки τ замеса д.быть миним-ой и достаточной для формиров. однород. теста. Чем > масса своб. воды в тесте, тем при прочих равных усл-ях короче τ замеса, и наоборот. П.э. замес сах. теста ведут в ТММ с частотой вращ-я лопастей 15...20 об./мин в теч. 10... 15 мин. Влияние хим. разрыхлителей. Хим. разрых. исп-ся для придания печ. пористости. Разрыхляющ. действие основано на их разлож. с выдел-ем газообраз. в-тв. Осн. треб-е к ним - их распад должен происх. не при замесе теста, а при выпечке ТЗ. Наиб. часто в кач-ве разрых. исп-ся гидрокарбонат натрия и карбонат аммония. При разлож. гидрокарб. натрия наряду с выдел-ем СО2 образ-ся карбонат натрия, кот. придает изд-ям щел-ую р-цию. Недостатком карбоната аммония. яв-ся то, что аммиак не полностью удал-ся из изд-я при выпечке и сообщает ему неприятн. запах, кот. исчезает при охлажд. изделий. Обычно в рец-рах предусм-ся смесь гидрокарб. натрия и карб. аммония, чем достигается ↓ие щелочности изд-й и не ост-ся зап. аммиака.Пластичность теста сах. печ. рассч. по ф-ле: П=Еост/Еmax
Эта величина у сах. теста близка к единице
24 Кинетика и условия студнеобразования СО пектиновых веществ. СО может идти за счет пектиновых в-в, содержащихся в пюре и др. В горячей мармеладной массе пектиновые вещества находятся в растворенном состоянии. Их молекулы представляют собой длинные нити, покрытые гидратной оболочкой. Под действ-ем теплового движения они беспорядочно перемещаются в дисперсионной среде, к-ой явл-ся водный р-р сахара, органич. кислот, экстрактивных веществ яблочного пюре. Карбоксильные группы пектиновых веществ диссоциируют на ионы, п.э. молекулы представляют собой высокомолек анионы. Соответственно в водных оболочках, покрывающих пектиновые молекулы, образуется двойной электрический слой с определенным потенциалом. Водные р-ры СО отн-ся к лиофильным системам. Их лиофильность обусловлена тем, что на поверхности молекул пектиновых в-тв находится много полярных групп ОН, СО, СНО. Чтобы вызвать агрегатирование молекул пектина, н-о ↑ межфазное натяжение на границе частица/вода. Это достигается присутствием в р-ре сахара, к-ый ↑ поверхностное натяжение водных р-ров. Следовательно, чем больше концен сахара в дисперсионной среде, тем выше межфазное натяжение на границе макромолекул пектина с жидкой фазой, тем сильнее тенденция частиц дисперсной фазы к ассоциации и агрегатированию. Когда энергия взаимодействия молекул дисперсионной среды друг с другом значительно превосходит энергию их взаимодействия с в-вом дисперсной фазы, среда будет способствовать сильному притяжению между частицами дисперсной фазы. При пр-ве мармелада протекает с достаточной скоростью, когда конц-ция сахара в жидкой среде соотв-т насыщенному р-ру при t 70 °С. В таком р-ре все молекулы воды связаны и удерж-ся молекулами сахарозы. Сила этой связи значительно превосходит силу связи молекул воды с пектиновыми в-ми, поэтому такая дисперсионная среда способствует агрегированию пектиновых веществ. При добавлении сахара в р-р поверхностное натяжение дисперс среды ↑, ↑ разность полярностей м-у средой и молекулами пектина, что способствует их агрегированию. Полярность пектиновых молекул зависит от строения. Чем выше степень этерификации молекулы, тем ниже ее сродство с водой и меньше полярность. Такие пектиновые в-ва обладают большей склонностью к ассоциации и лучшей СО способностью. В достаточно концентр-х растворах при t 70...75 °С в результате теплового движения молекулы пектина могут сближаться и сталкиваться. Влияние тех или других сил зависит от расстояния м-у молекулами, их заряда, толщины диффузных слоев в гидратных оболочках и величины потенциала. Молекулы пектиновых в-в имеют на своей поверхности одноименный электрический заряд, п.э. при сближении на расстояние, при к-ром происходит перекрытие их диффузных слоев, они взаимоотталкиваются. Чтобы произошла коагуляция таких молекул, они должны за счет энергии теплового движения преодолеть определенный энергетический барьер. Если высота барьера значительно превышает среднюю энергию теплового движения пектиновых мицелл, то вероятность его преодоления и, соответственно, скорость коагуляции практически равны нулю. Для ↓ величины энергетического барьера до уровня, при котором он преодолевается молекулами пектина за счет энергии теплового движения, в жидкую фазу н-о ввести индифферентный электролит (например, кислоту) или потенциалопределяющие ионы (например, ионы Са++, Mg++). В первом случае снижается толщина диффузного слоя и высота его потенциала, во втором — уменьшается величина потенциала на поверхности молекул пектина. В обоих случаях это ведет к ↓ сил электростатического отталкивания и, следовательно, ↓ энергетического барьера. При определенных пороговых концентрациях электролита, к-е тем меньше, чем больше валентность ионов, толщину диффузного слоя можно уменьшить до критического значения, при котором высота энергетического барьера становится равной нулю. Такое состояние системы будет отвечать максимальной скорости коагуляции. Наиболее активной из используемых кислот является виннокаменная, а наименее активной — лимонная кислота. Количество кислоты, необходимой для студнеобразования, зависит от природы, степени ее диссоциации. Заряд диффузного слоя существенно зависит от величины рН и с понижением рН резко падает. Минимальная концентрация ионов водорода в жидкой фазе, при которой начинается образование пектинового студня, соответствует рН 3,46. Количество кислоты, необходимой для студнеобразования, меняется не только в зависимости от природы, но и от количества и качества пектина. Если пектин обладает слабой студнеобразующей способностью, то концентрацию кислоты следует повысить, но только в определенных пределах. Оптимальным значением рН среды для студнеобразования пектина хорошего качества является рН 3,0...3,2. Количество добавляемой кислоты зависит от концентрации сахара в растворе. Чем она выше, тем меньше требуется кислоты, и наоборот. При пр-ве фруктовых мармеладов практической нормой кислоты считается 0,8 % (в пересчете на яблочную) при содержании пектина хорошего качества в уваренной мармеладной массе 0,8...1,0 % и концентрации сахара 65...70 %. Таким образом, регулируя высоту энергетического барьера добавлением в систему электролита, можно управлять скоростью коагуляции пектиновых молекул и получать студни с заданными физическими свойствами. При полном исчезновении энергетического барьера каждое столкновение молекул пектина сопровождается их сцеплением, что отвечает порогу «быстрой» коагуляции. Благодаря тому, что макромолекулы имеют значительную длину и гибкость и могут входить в состав различных ассоциатов, в мармеладной массе образуется пространственная сетка. Образование студня есть не что иное, как процесс появления и постепенного упрочнения в застудневающей массе пространственной сетки. Для застудневания растворов высокомолекулярных веществ характерно, что связи образуются не по концам отдельных молекул, как это происходит при коагуляции коллоидных частиц, а могут возникать между любыми участками гибких макромолекул, лишь бы на них имелись группы, которые могут взаимодействовать друг с другом. После сформирования студня происходит постепенное упрочнение пространственной сетки за счет взаимодействия полярных групп макромолекул, ионизирующих групп, несущих электрический заряд различного знака, при этом происходит упорядочение отдельных участков молекул. Эти участки обычно ориентируются параллельно друг другу, так как такое расположение соответствует уменьшению свободной энергии системы.
25 Какую роль играют рецептурные компоненты в образовании затяжного печенья. Влияние муки вобраз-ии теста пренадлежит белковым вещ-вам пш муки, к-ые с водой способны набухать. При этом нерастворимые в воде глиадиновая и глютениновая фракции белка при замесе образуют белковый структурный каркас, к-й в виде тонких пленок и нитей пронизывает всю массу теста. Из свойств муки наиболее важными являются количество и качество клейковины. От содержания и качества клейковины зависит ВПС и W теста и его структурно-мех св-ва. Чем выше качество клейковины, тем больше мука поглощает воды при замесе теста. ↑ W теста, ↑ процесс выпечки. При использовании муки с сильной клейковиной наблюдается деформация изделий в процессе выпечки. Поэтому для получения рыхлого, пластично-вязкого теста н-о исп-ть муку со слабой и средней по качеству клейковиной, а для упруго-эластичного теста — муку с сильной клейковиной. Влияние сахара. В водном растворе молекулы сахаров покрываются гидратными оболочками, что ↑ их межмолекулярный объем, ↓ скорость диффузии при осмотическом набухании белков муки. Особенно высокогидратирован явл-ся молекулы сахарозы. При t 20 °С связывают и удерживают от 8 до 12 молекул воды. Следовательно, чем больше сахара в рецептуре теста, тем меньше в его жидкой фазе свободной воды, участвующей в гидратации и набухании коллоидов муки. При замесе затяжного теста свободная вода быстро проникает в межмицеллярное пространство белковых молекул, вызывая их набухание. Влияние жира. Жиры д. б. пластичными. В этом случае «и образуют в тесте тончайшие пленки, обволакивающие и смазывающие частицы муки. Значительная часть этого жира связ-ся клейковиной и крахмалом. Механизм взаимодействия липидов муки и вносимых жиров с компонентами теста зависит от хим состава и св-тв исполь-го жира и муки. Важную роль при этом играют входящие в состав жира триглицериды насыщенных и ненасыщенных кислот. Чем больше содержание в жире триглицеридов ненасыщенных жирных кислот, тем он больше сорбируется белками. Жиры изменяют св-ва пш крахмала при замесе теста в результате образ-я ими комплексов с амилазной фракцией. Адсорбируясь на поверхности белковых мицелл и крахмальных зерен, жир препятствует набуханию коллоидов муки и ↑ содерж-е жидкой фазы теста. Вследствие этого ослабляется связь между компонентами твердой фазы теста, что делает его пластичным. ПАВ замедляют гидратацию и огранич-т набух-ть крахмальных суспензий, ↓ кол-во растворимых фракций крахмала, ослабляют связи м-у набухшими гранулами крахмала. Влияние воды. Кол-во воды, идущее на замес, зависит от вида теста и ВПС, к-ая зависит от кол-ва и кач-ва клейковины, W, выхода и крупноты помола муки. Чем крупнее частицы, тем меньше их удельная поверхность, тем меньше связ-т воды. На ВПС муки оказывают влияние присутствующие в тесте сахар и жир. Молекулы сахара связывают большое количество молекул воды, снижая набухание коллоидов муки. ВПС муки при добавлении 1 % сахара уменьшается на 0,6 %. W затяжного теста 22...26 %. Эмульсия — это дисперсная система, состоящая из двух несмешивающихся жидкостей, одна из которых распределена в другой в виде капель. Важными технолог-ми показателями эмульсий явл-ся W и t, т.к. от них эмульсии зависят ее вязкость и устойчивость. Известно, что с ↑ t и W вязкость эмульсии ↓. От W эмульсии зависит вязкость. Для получения устойчивых эмульсий вязкостью не менее 1,0 Па-с используют эмульгаторы. При их выборе следует учитывать физ-хим св-ва всей системы и область применения эмульсии. Для затяжного теста W эмульсии (примерно 35 %)
|
|||||||||
|
Последнее изменение этой страницы: 2016-07-14; просмотров: 438; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.142.98.186 (0.016 с.) |