
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Принцип інтенсифікації процесівСодержание книги
Поиск на нашем сайте
Для інтенсифікації процесу (збільшення швидкості, підвищення потужності тощо) відповідно наведенним вище закономірностям треба збільшити різницю потенціалів, кінетичні коефіцієнти (константи), поверхню контакту фаз. Розглянемо ці засоби більш конкретно. Під інтенсифікацією звичайно розуміють скорочення часу технологічної операції. Засоби інтенсифікації визначимо виходячи з відомих теоретичних уявлень про основні технологічні процеси, які використовуються в технології. Загальні уяви про викладені вище закономірності технологічних процесів можуть бути виражені одним відомим феноменологічним лінійним рівнянням, відповідним першому закону термодинаміки
Де q — щільність потоку теплоти або маси; К — кінетичний коефіцієнт (залежний від фізико-хімічних властивостей матеріалу); С — рушійна сила. Це рівняння описує всі закони перенесення маси та енергії і проявляється конкретно в кожному виді переносу. Наприклад,
Аналізуючи наведені закономірності окремих технологічних операцій, можна зробити висновок про основні принципи або напрямки інтенсифікації: - збільшення рушійної сили процесу, тобто збільшення різниці температур, концентрацій, тисків, напруги, електричного струму, п'єзометричних висот та ін.; - збільшення (або оновлення) поверхні контакту фаз, тобто розширення можливостей контактування (зіткнення) різних потоків; - збільшення величин кінетичних коефіцієнтів. Методи інтенсифікації можуть мати різну природу та здійснюватися різними технічними засобами. Класифікація методів інтенсифікації наведена на рис. 2.2. Рушійною силою в процесах є градієнт переносимої субстанції: при перенесенні теплоти — градієнт температур, при перенесенні маси — градієнт концентрацій і т.д. Тобто рушійну силу можна підвищити збільшенням градієнту субстанції (концентрація, температура, тиск, напруга) в початковій фазі та зменшенням її в кінцевій. При внутрішньому перенесенні — різницею температур, вологи, тиску, концентрацій речовин в середині матеріалу та на його поверхні, а при зовнішньому — різницею субстанцій на поверхні та в середовищі робочого агенту. Збільшення поверхні контакту фаз здійснюють подрібненням, диспергуванням, розпилом, перемішуванням, запобіганням злипанню частинок, створенням зваженного або киплячого шару матеріалу, вібрацією, ударними та акустичними діями, своєчасним виведенням з процесу утворенних речовин, які "забруднюють" тобто скорочують поверхню контакту фаз. Для збільшення кінетичних коефіцієнтів існує значна кількість засобів. Основні із них засновані на руйнуванні пограничного шару або зменшенні його товщини, зміною властивостей та структури взаємодіючих фаз. Зміна властивостей або структури об'єкту технологічної обробки пов'язана зі змінами в ньому на атомно-молекулярному рівні. Це можна зробити за допомогою магнітних, електричних та акустичних коливань, нагріванням та охолодженням. Руйнування або зменшення товщини пограничного шару здійснюють збільшенням турбулентності потоків за рахунок збільшення швидкості робочого агенту, шорсткості (нерівностей) поверхні, імпульсними діями. Ці дії не тільки зменшують товщину або руйнують пограничний шар, але й збільшують поверхню контакту
Рис. 2.2. Класифікація методів інтенсифікації технологічних процесів фаз, тобто мають комбінований характер. Особливу увагу треба звернути на використання імпульсних збуджень для інтенсифікації (удар, вибух, пульсації швидкості, температур, тисків, степені та інтенсивності перемішування). Систематизуючи методи інтенсифікації, можна виділити мікроскопічний (міжмолекулярні, іоно-молекулярні, атомарні збурення) та макроскопічні (дії на групи атомів та молекул). Макроскопічний рівень відображає гідродинамічні та теплові фактори. Дії на макрорівні здійснюють на процеси переносу за рахунок конвекції макрочастинок, тобто режими обтікання частинок твердого матеріалу, які дозволяють змінювати швидкість взаємодії груп атомів та молекул. Математичний опис цих явищ засновано на рівняннях тепло-масо-переносу та аеро- гідромеханіки. Лімітуючі та визначаючі інтенсивність переносу фактори встановлюють введенням граничних та початкових умов і постійних параметрів в диференційних рівняннях переносу з наступним з'ясуванням їх ролі. При масообмінних процесах відрізняють тепловий, аеродинамічний та дифузійний пограничні шари. В дифузійному пограничному шарі, який безпосередньо прилягає до поверхні розподілу фаз, перенесення маси здійснюється молекулярним засобом, швидкість якого визначає швидкість масопереносу в цілому. Зменшення товщини шару приводить до зменшення опору в перехідній зоні. Товщина дифузійного шару визначається за виразом,
де Pe — число Пекле; v — швидкість робочого агенту, м/с; l — характерний геометричний розмір, м; D —- коефіцієнт дифузії, м/с. Якщо товщина аеродинамічного пограничного шару визначається за виразом
то в звуковому полі товщина пограничного шару залежить від частоти звуку
де v—коефіцієнт кінематичної в'язкості, м/с;
Re — число Рейнольдса. В газових середовищах число Прандтля Рг = Ре/Re ~ 1, тобто товщина пограничних аеродинамічного та дифузійного шарів значно не відрізняються. Зменшити товщину пограничного шару можна збільшенням швидкості потоку та частотою коливань. Вона також визначається розмірами, формою твердих частинок, властивостями матеріалу та умовами масообміну. Наприклад, при сушінні процес прискорюється при високих рівнях звукових коливань, (125...133) Дб, при частоті (6...10) КГц. Проте, витрати енергії при використанні акустичних коливань в (3...4) рази перевищують витрати при конвективному сушінні. Тобто його використання припустиме для важкосохнущих та дорогих матеріалів. Товщина пограничного шару при акустичних коливаннях знижується до (50... 100) Фізично це явище можливо було б з'ясувати за рахунок перепаду тиску на поверхні матеріалу, утворенням поверхневої кавітації та турбулізації робочого агенту, зниженням в'язкості рідини, прискоренням дифузії пари в капілярах, розрушенням защімлених бульбашок повітря в шпарах, які сприяють виведенню вологи з шпар. Із наведених кінетичних закономірностей виходить, що кожний етап будь-якого процесу необхідно проводити в найбільшій відстані від стану рівноваги, тобто при найбільшій різниці потенціалів, або максимальній рушійній силі процесу. Проте, при підвищенні ефективності процесу необхідно максимально використати різницю потенціалів, яка виникла, але не використовується. Наприклад, використання теплоти в дефлегматорі для підігріву бражки; використання вторинної пари випарних установок в наступних корпусах багатокорпусної установки, використання потенціальної сили тяжіння при переміщенні продуктів по самопливам і т.і. Якщо при проведенні будь-якої технологічної операції побічні різниці потенціалів не використовуються, то треба шукати можливість їх використання при виконанні інших технологічних операцій на наступних або попередніх етапах технологічного процесу. Рушійна сила хімічних реакцій, сорбційних процесів, ректифікації, тощо виявляється різницею робочих та рівноважних концентрацій реагуючих або приймаючих участь в масообміні речовин. У зв'язку з цим збільшення рушійної сили процесу може здійснюватись зі збільшенням робочої концентрації або зменшенням рівноважної або одночасною зміною обох величин. Ефективність підвищення тиску залежить від агрегатного стану реагуючих речовин. Підвищення тиску більш впливає на швидкість процесів в газовій фазі або при взаємодії газів з рідинами та твердими тілами та в меншій мірі на процеси в рідких та твердих фазах. Крім того, підвищення тиску зменшує об'єм газової фази та збільшує концентрації взаємодіючих речовин. Тобто підвищення тиску рівнозначне збільшенню концентрації реагентів. Вплив тиску визначається кінетичним рівнянням. Швидкість гомогенного процесу в газовій фазі можлна виразити через парціальний тиск
Де
n— номер речовини. Для реакції типу
якщо вона незворотна або перебігає далеко від стану рівноваги
де загальний порядок реакції
Парціальний тиск кожного компоненту пропорціональний загальному тиску Р, тобто тобто
Де Р — загальний відносний тиск, тобто відношення фактичного тиску до атмосферного. Тобто, швидкість реакції газових компонентів пропорціональна тиску в степені, що дорівнює порядку реакції. Тиск найбільш інтенсифікує реакції високого порядку, проте зі зростанням тиску може змінитися порядок реакції п та зменшитися константа швидкості. Для адсорбції, абсорбції та інших процесів перехід газового компоненту в тверду або рідку фазу визначаться за рівнянням
де F — площа контакту фаз. Якщо процес незвотний або далекий від рівноваги, то Тобто, n = 1 і, перетворюючи цей вираз, одержимо
Тобто швидкість цих процесів прямо пропорційна тиску. Для процесів десорбції газів та випарювання рідин прискорення процесу та підвищення виходу досягається зниженням тиску, тобто використанням вакууму. Для зворотніх процесів в газовій фазі рушійна сила процесу визначається рівнянням
Значення рівноважних парціальних тисків розраховують для заданого складу газової суміші за відомими константами рівноваги. Залежність константи рівноваги, що виражена в мольних часиках від тиску, визначають за рівнянням
Для модельної реакції типу
Ця формула відображує в кількісній формі принцип Ле-Ша-тельє. Зі збільшенням тиску Р для реакцій, які йдуть зі зменшенням об'єму ( В технології зміну тиску використовують для інтенсифікації випарювання, ректифікації, гідрогенізації, гідролізі полісаха- ридів та інших цілей в олієжировій, крохмалопатоковій та інших галузях виробництва. Інтенсифікацію процесу зміною температури використовують головним чином у сорбційних, десорбціїних та сушильних процесах. Рушійна сила процесів абсорбції, адсорбції, конденсації зображається так
Знижуючи температуру рідкої фази, зменшують парціальний тиск пари газового (парового) компоненту над нею, та відповідно збільшують рушійну силу Зниження температури в проточних апаратах частіше всього досягається подачею попередньо охолодженої в холодильниках рідини. Використовують також холодильні елементи (труби, змійовики), що розміщені безпосередньо в апараті, або охолодженням стінок апарату. Рушійна сила процесів десорбції та випарювання зображується як
Зрушення рівноваги та збільшеная швидкості цих процесів досягається підвищенням температури рідини перед подачею її в апарат (теплообмінники, трубчасті печі і т.і.) або безпосередньо в апаратах гарячими газами, гострою або глухою парою. Одночасна зміна температури та тиску розширює можливості збільшення рушійної сили процесу за рахунок обох складових. Використовують підвищення температури сушильного агенту і для інтенсифікації процесів сушіння. Швидкість сушіння продукту в значній мірі визначається потенціалом сушіння Е, рівним різниці сухого E= З підвищенням температури сушильного агенту потенціал сушіння збільшується. Визначення швидкості процесу можна дати виходячи з другого закону термодинаміки, відповідно з яким імовірність одержання максимально можливої кількості роботи (ексергія) в даній системі збільшується зі збільшенням різниці температур. Відведення продуктів реакції з реакційної зони збільшує су- марну швидкість зворотніх реакцій
за рахунок змен- шення
за рахунок зниження або повного усунення величини рівноважної концентрації. Якщо процес перебігає в газовій фазі, то відведення продукту в іншу (рідку або тверду) фазу приводить до зменшення величини рівноважної концентрації. З газової суміші продукт реакції можна відвести конденсацією, виборчою абсорбцією або адсорбцією. Наприклад при екстракції олії із насіння бензином, відокремлення його зі шроту виконують безперервним зниженням концентрації, конденсацією, а потім знову використовують його як екстрагент. Підвищення температури приводить до збільшення констант швидкостей реакцій, коефіцієнтів теплопередачі, тепловітдачі, масообміну, дифузії, т.і. В результаті сумарна швидкість процесу збільшується при підвищенні температури до деякої границі. Вплив температури реагуючих мас на константу швидкості реакції для процесів, які проходять в кінетичній області, визначається за формулою Ареніуса
яку звичайно перетворюють до вигляду
Де кінцевій температурах Е — енергія активації реагуючих речовин, Дж/моль; R — газова стала, яка дорівнює 8,3 Дж/моль-град. При підвищенні температури на 10 °С згідно з правилом Вант-Гоффа швидкість реакції збільшується в (2...4) рази. Проте, це правило приблизно виконується в області середніх температур (10...400) °С при енергіях активації порядку (60... 120) кДж/моль. Вплив температури на швидкість процесів в дифузійній області менший, ніж в кінетичній. Залежність коефіцієнту дифузії для газів від температури зображують спрощеною формулою
де Р — загальний тиск газу; a = (1,5...2,0) покажчик степені. Коефіцієнт диффузії D для газів змінюється в межах (0,1...1,0) Збільшення поверхні рідкої фази розподілом її у вигляді тонкої плівки на поверхні насадочних тіл (насадок), що заповнюють об'єм апарату або утворенням спеціальних плівкових течій, (на-садкові абсорбери для очищення газів, плівкові випарні апарати). Розвиток поверхні рідкої фази за рахунок диспергування, тобто розбризкуванням, розпиленням її пневматичним або механічним засобами в об'ємі або в течії газу, який проходить через порожнини камери або башти (розпилювальні сушарки для виробництва сухого молока, висушування крові, дріжджів, яєчного порошку, розчинної кави і т.і.). Розвиток поверхні взаємодії фаз диспергуванням газу в об'ємі рідини, тобто пропусканням (пробулькуванням) бульбашок газу через шар рідини в колонах з решетами або ковпачковими тарілками. Площа контакту дорівнює поверхні всіх бульбашок, а масопередачу називають бульбашковою (тарільчаті брагорек-тифікаційні апарати і ін). Створенням завислого шару, рухомої піни при пропусканні газу знизу наверх через решітку пінного апарату та через рідину, що в ній знаходиться з такою ж швидкістью, при якій сили тертя газу урівноважують масу рідини. Через інтенсивне переміщування фаз та безперервне оновлення поверхні рідини усуваються дифузійний опір та збільшується коефіцієнт масопередачі. Засоби збільшення поверхні для систем "газ-тверде тіло" та "рідина — тверде тіло" теж можна розподілити на чотири види. Перемішування подрібненого твердого матеріалу механічними мішалками на полицях апарату, що обтікаються зверху газом або рідиною. Тут теж оновлюється поверхня дотику фаз. Для розрахунків умовно приймають поверхню площі всіх полиць. Перемішування тонко подрібненого твердого матеріалу в об'ємі (в течії) газу або рідини, при якому площа контакту досягає граничної величини, цю дорівнює загальній поверхні всіх твердих частинок (апарати для очистки дифузійного соку, склеювання вина). Пропуском потоку газу або рідини через рухомий шар шматків або гранул твердого матеріалу, який лежить на колісни- ках або решетах (фільтруючий шар). Такий шар затримує тверді частинки, які знаходяться в течіях рідини (очищення водки, вин, соків та інших продуктів в шарі активованого вугілля). Перемішування в завислому (киплячому) шарі, який утворюється при пропусканні газу або рідини знизу наверх через шар зернистого матеріалу з такою швидкістю, при якій частинки пульсують в течії газу або рідини та не покидають границь завислого шару (сушіння харчових продуктів в киплячому шарі т.і.) Принципово нові засоби можуть бути розроблені на базі фундаментальних наук.
|
||||
|
Последнее изменение этой страницы: 2016-04-21; просмотров: 351; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.144.224.105 (0.012 с.) |







 —частота коливань, 1/с;
—частота коливань, 1/с; м. Щільність енергії при цьому складає (10...20)Вт/
м. Щільність енергії при цьому складає (10...20)Вт/ 

 — парціальний тиск речовини в газовій суміші;
— парціальний тиск речовини в газовій суміші;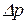 — рушійна сила процесу;
— рушійна сила процесу;
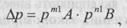



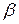 — коефіцієнт, що залежить від константи швидкості реакції та рушійної сили процесу;
— коефіцієнт, що залежить від константи швидкості реакції та рушійної сили процесу;
 - дійсна концентрація компонентів в газовий фазі.
- дійсна концентрація компонентів в газовий фазі.



 N — величина від'ємна) константа рівноваги збільшується, а рівноважна концентрація початкових компонентів відповідно зменшуються. Зворотнє явище перебігає при підвищенні тиску для реакцій, які йдуть зі збільшенням об'єму.
N — величина від'ємна) константа рівноваги збільшується, а рівноважна концентрація початкових компонентів відповідно зменшуються. Зворотнє явище перебігає при підвищенні тиску для реакцій, які йдуть зі збільшенням об'єму.
 і загальну швидкість процесу V.
і загальну швидкість процесу V.
 та мокрого
та мокрого  термометрів
термометрів
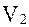 або збільшення рушійної сили гетерогеного процесу
або збільшення рушійної сили гетерогеного процесу


 — константи швидкості реакції при початковій та
— константи швидкості реакції при початковій та ;
;



