
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
В-48 Мас-спектрометричне дослідження речовиниСодержание книги
Поиск на нашем сайте
Мета: ознайомитись із методами сучасної мас-спектрометрії та навчитись визначати питомий заряд частинок. Устаткування: комп’ютерна програма “Масспектро- метр”. Теоретичні відомості Мас-спектрометрія – це сучасний метод визначення елементного складу речовини незалежно від його агрегатного стану. Особливо важливе значення цей метод має для вивчення процесів формування тонких конденсованих шарів, оскільки дозволяє: 1) одночасно контролювати склад як молекулярного пучка, що осаджується, і конденсату, що утворився; 2) зміну складу і парціальних тисків залишкових газів; 3) термодинамічні характеристики процесів сорбції, випаровування і конденсації; 4) визначення ізотопного складу речовини. Розвиток в останній час мас-спектрометрії вторинних йонів дає можливість отримувати інформацію про елементарні акти взаємодії частинок на поверхні твердих тіл. В мас-спектрометричному методі процеси випаровування зазвичай вивчають, аналізуючи молекулярні пучки, що витікають через ефузійний отвір комірки Кнудсена, яка містить речовину в твердому стані, що перебуває в рівновазі із своєю парою за певної температури. Знання термодинамічних характеристик потрібне не тільки для розуміння процесів випаровування і конденсації, але і для створення, наприклад, фізико-технологічних передумов виготовлення тонких конденсованих плівок із складних сполук, а також прогнозування їх властивостей. Для аналізу складу молекулярного пучка, залишкових газів і визначення термодинамічних характеристик зазвичай використовують мас-спектрометри, що мають досить високі чутливість (~ 10-8 А/Па) і роздільну здатність (М/ΔМ > 1000). Високотемпературна мас-спектрометрія в якості джерел молекулярних пучків частинок досліджуваних сполук застосовує кнудсенівський (випаровування із ефузійної комірки) і ленгмюрівський (випаровування з відкритої поверхні) методи. Мас-спектрометричний метод використовує основну властивість речовини – масу молекул (атомів), а точніше – відношення маси до заряду: m/e (або ж питомий заряд: е / m). За допомогою мас-спектрометра можна отримати інформацію про склад як залишкових газів, так і молекулярного пучка речовини, що випаровується.
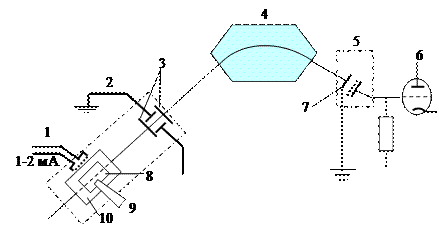
Під дією електронів молекули залишкових газів або пара досліджуваної речовини йонізуються. Для ідентифікації утворених йонів використовується розмежування, розділення в просторі або в часі частинок аналізованої речовини у відповідності з відношенням m/e маси до заряду в умовах високого вакууму. Молекули досліджуваної речовини йонізуються в йонізаційній камері 10 (рисунок 48.1) під дією електронів, що емітують з катоду 1. Утворені йони прискорюються в електростатичному полі U і фокусуються у вузький пучок в йонно-оптичній системі мас-спектрометра. Потім йони проходять через камеру аналізатора, яка поміщена в поперечне магнітне поле секторного типу, що створюється електромагнітом 4 з полюсними наконечниками у формі трапеції. Якщо знехтувати початковими швидкостями йонів, то можна вважати, що у всіх йонів після прискорення буде однакова енергія:
де m – маса йона; e – його заряд; U – прискорююча напруга; υ – швидкість йона на виході із джерела йонів. В поперечному магнітному полі йони зазнають дії сили Лоренца, яка викривлює їх траєкторію, надаючи їм доцентрового прискорення:
де В – індукція магнітного поля; R – радіус йонної траєкторії.
Із виразів (48.1) і (48.2) отримуємо
Таким чином, в магнітному полі йонний пучок ділиться на кілька траєкторій, в кожній з яких є йони тільки з одним значенням m/e. Часто використовуються так звані “180 – градусні мас-спектрометри”, в яких заряджені частинки змінюють напрям свого руху на 180о (рисунок48.2). Такі мас-спектрометри використовуються, наприклад, для поділу (сортування) ізотопів, тобто ядер атомів з однаковим зарядом, але з різними масовими числами. Вперше такі дослідження провів Астон, який довів, що майже всі елементи складаються з ізотопів. Він зробив узагальнення, яке назвав правилом цілих чисел: істинні атомні маси всіх елементів є цілі числа. Всі відхилення атомних мас у таблиці елементів від цілих чисел пояснюються тим, що багато простих речовин є сумішами ізотопів. У мас-спектрометрах заряджені частки рухаються в камері, у якій створений високий вакуум, в однорідному магнітному полі. Частки влітають у камеру, попередньо пролетівши через селектор швидкостей. Траєкторії часток – це дуги кола радіусом
Комп'ютерна модель дозволяє змінювати індукцію магнітного поля B і швидкість часток υ. Дослід з розділенням ізотопів може бути виконаний для ізотопів вуглецю, неону й урану, а також для ізотопів невідомої речовини.
Порядок виконання Завдання 1 Ознайомлення із можливостями комп’ютерної моделі. 1. Змінюючи у вікні інтерфейсу величину індукції магнітного поля від мінімального до максимального значень, спостерігати за зміною форми траєкторії і зміною радіусів траєкторії для вибраних ізотопів почергово. Значення швидкості частинок вибрати постійним. 2. Для фіксованого (оптимального) значення В змінювати значення швидкості вказаних ізотопів і спостерігати за зміною їх траєкторії руху в магнітному полі. Завдання 2 Визначення маси відомих ізотопів. 1. Встановити для відповідного ізотопу (перша п’ятірка студентів за списком – С; друга – Ne; третя – U) такі значення індукції магнітного поля В і швидкості частинок υ, щоб їх траєкторія поміщалась в межах камери мас-спектрометра. 2. Враховуючи (48.4), визначити масу ізотопів в а.о.м. за допомогою формули
3. Порівняти отримані значення маси ізотопів із наведеними на інтерфейсі. Завдання 3. Визначення маси невідомих ізотопів. 1. Встановити у вікні значень В величину індукції магнітного поля згідно Вашого варіанту. Таблиця 48.1 – Варіанти завдань
2. Підібрати значення швидкості невідомих ізотопів таке, щоб в камері мас-спектрометра помістилось півколо їх траєкторії. 3. Знайшовши радіуси траєкторій, за допомогою формули (48.5) визначити масу невідомих ізотопів. 4. Проаналізувати отримані результати, визначити похибки вимірювань і визначити за допомогою довідників досліджувану речовину. Контрольні запитання 1. Які властивості чи процеси в твердих тілах можна досліджувати за допомогою методів мас-спектрометрії? 2. Який принцип використовується в роботі мас-спектрометрів? 3. Як однорідне магнітне поле впливає на рух заряджених частинок? 4. Як визначити напрям та величину сили Лоренца? 5. Що називають питомим зарядом? 6. Що таке ізотопи, ізобари, ізомери? Література 1. Структура и физические свойства твердого тела. Лабораторный практикум: Учеб. пособие / Под ред. проф. Л.С.Палатника.– Киев: Вища школа. 1983.–264 с. 2. Курик М.В., Цмось В.М. Фізика твердого тіла. Нав.посібник – К.: Вища школа, 1985, - 246 с. (Розділ 10). 3. Киттель Ч. Введение в физику твердого тела. – М.: Наука, 1978. – 791 с. (Глави 2,3). Додаткова література 4. Болеста І.М. Фізика твердого тіла. Навч. пос. – Львів: Видавн. центр ЛНУ імені Івана Франка.2003. – 480с. 5. Бушманов Б.Н., Хромов Ю.А. Фізика твердого тела: Уч. Пособие для вузов. – М.: Высшая школа, 1971. – 224 с. 6. Блейкмор Дж. Физика твердого тела / Пер. с англ. Под ред. Д.Т. Андрианова. – М.: Мир, 1988. – 608 с. 7. Епифанов Г.И. Физика твердого тела: Уч. Пособие. – Высшая школа, 1977. – 288 с.
|
|||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-04-19; просмотров: 152; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.144.4.54 (0.008 с.) |


 , (48.1)
, (48.1) , (48.2)
, (48.2)
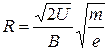 . (48.3)
. (48.3)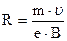 . (48.4)
. (48.4)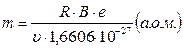 (48.5)
(48.5)


