

Мы поможем в написании ваших работ!
ЗНАЕТЕ ЛИ ВЫ?
|
Параметры орбит электронов в атомах
| Элемент
| Номер электрона
| Стацио-нарное состояние k
| Зарядовое число z/
| Радиус орбиты r/ ×10-10 , м
| Скорость электрона V/ ×106 м·с-1
| Полная энергия Е×10-19, Дж
| Период обращения Т×10-16, с
| 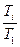
| | 1
| 2
| 3
| 4
| 5
| 6
| 7
| 8
| 9
| | H
| 1
| 1
| 1,00003
| 0,529177
| 2,18650
| 21,7272
| 1,52066
| 1
| | He
| 1
2
| 1
1
| 1,96780
1,39144
| 0,268926
0,380318
| 4,30423
3,04355
| 84,3949
42,1974
| 0,392570
0,785139
| 1
2
| | Li
| 1
2
3
| 1
1
2
| 2,95691
2,41431
1,24674
| 0,178967
0,219189
1,68783
| 6,46814
5,28121
1,36360
| 190,572
127,048
8,46986
| 0,173850
0,260775
7,82324
| 1
1.5
45
| | Be
| 1
2
3
4
| 1
1
2
2
| 3,95074
3,42144
2,31332
1,66578
| 0,133947
0,154669
0,915035
1,270736
| 8,64224
7,48440
2,53019
1,82195
| 340,209
255,157
29,1608
15,1204
| 0,0973840
0,129845
2,27229
4,38228
| 1
1,33333
23,3333
45
| | B
| 1
2
3
4
5
| 1
1
2
2
2
| 4,94960
4,42705
3,33860
2,71952
1,56195
| 0,106916
0,119536
0,634028
0,778360
1,35521
| 10,8274
9,68429
3,65163
2,97450
1,70840
| 533,990
427,192
60,7382
40,3011
13,2943
| 0,0620440
0,0775551
1,09094
1,64617
4,98421
| 1
1,25
17,5833
26,5
80,3333
|
Продолжение табл. 5.12
| 1
| 2
| 3
| 4
| 5
| 6
| 7
| 8
| 9
| | C
| 1
2
3
4
5
6
| 1
1
2
2
2
2
| 5,94902
5,43068
4,43068
4,34455
3,76249
1,81973
| 0,0889544
0,0974447
0,487223
0,562597
0,790644
1,16323
| 13,0137
11,8798
4,75192
4,11528
2,92829
1,99035
| 771,410
642,842
102,855
77,141039,0586
18,0466
| 0,0429485
0,0515381
0,644227
0,858969
1,69645
3,67211
| 1
1,2
15
20
39,5
85,5
| | N
| 1
2
3
4
5
6
7
| 1
1
2
2
2
2
2
| 6,94991
6,43437
5,36663
4,76760
3,73438
2,95035
2,06824
| 0,0761436
0,0822445
0,394431
0,443990
0,566831
0,717462
1,02346
| 15,2033
14,0755
5,21467
5,86988
4,08457
3,22701
2,26218
| 1052,83
902,428
156,943
123,862
75,9934
47,4335
23,3098
| 0,0314686
0,0367133
0,422203
0,534965
0,871941
1,39694
2,84266
| 1
1.16666
13,4166
17
27,7083
44,3916
90,3333
| | O
| 1
2
3
4
5
6
7
8
| 1
1
2
2
2
2
2
2
| 7,95424
7,43896
6,36339
5,80895
4,76475
3,97712
3,21400
2,00159
| 0,0665295
0,0711378
0,332647
0,364397
0,444256
0,532236
0,658608
1,05754
| 17,4004
16,2732
6,96014
6,35371
5,21158
4,35009
3,51540
2,18930
| 1379,11
1206,22
220,657
183,881
123,714
86,1940
56,2900
21,8319
| 0,0240235
0,0274668
0,300293
0,360352
0,535603
0,768751
1,17715
3,03509
| 1
1,14333
12,5
15
22,295
32
49
126,338
|
Продолжение табл. 5.12
| 1
| 2
| 3
| 4
| 5
| 6
| 7
| 8
| 9
| | F
| 1
2
3
4
5
6
7
8
9
| 1
1
2
2
2
2
2
2
2
| 8,96928
8,41393
7,39773
6,80720
5,80731
5,07379
4,30525
3,20895
2,26907
| 0,0590004
0,0628895
0,286137
0,310960
0,364500
0,417196
0,491670
0,659645
0,932879
| 19,6209
18,4061
8,09153
7,44561
6,35195
5,54963
4,70902
3,50990
2,48187
| 1753,55
1543,12
298,222
252,511
183,778
140,284
101,004
56,1135
28,0567
| 0,0188936
0,0214701
0,222189
0,262412
0,360554
0,472341
0,656029
1,18085
2,36171
| 1
1,13636
11,76
13,8888
19,0833
25
34,7222
62,5
125
| | Ne
| 1
2
3
4
5
6
7
8
9
10
| 1
1
2
2
2
2
2
2
2
2
| 9,98823
9,41699
8,38513
7,79801
6,80895
6,09276
5,33893
4,32081
3,46958
2,51680
| 0,0529815
0,0561953
0,252443
0,271449
0,310880
0,347423
0,396477
0,489900
0,610093
0,841105
| 21,8500
20,6004
9,17152
8,52936
7,44753
6,66418
5,83965
4,72605
3,79498
2,75284
| 2174,60
1932,97
383,143
331,368
252,641
202,288
155,328
101,735
65,5989
34,5175
| 0,0152354
0,0171399
0,172943
0,199964
0,262277
0,327561
0,426592
0,651315
1,01011
1,91966
| 1
1,125
11,35135
13,125
17,215
21,5
28
42,75
66,3
126
|
Продолжение табл. 5.12
| 1
| 2
| 3
| 4
| 5
| 6
| 7
| 8
| 9
| | Na
| 1
2
3
4
5
6
7
8
9
10
11
| 1
1
2
2
2
2
2
2
2
2
3
| 11,0004
10,4177
9,38120
8,80034
7,82755
7,11931
6,38444
5,39178
4,59499
3,72883
1,84363
| 0,0481065
0,0507971
0,225639
0,240532
0,270425
0,297327
0,331551
0,392591
0,460668
0,567676
2,58334
| 24,0643
22,7897
10,2611
9,63573
8,56117
7,78703
6,98324
5,89748
5,02596
4,07855
1,34436
| 2637,68
2365,66
479,586
422,030
333,885
276,198
222,121
158,420
115,057
75,7685
8,23206
| 0,0125606
0,0140048
0,138167
0,157007
0,198457
0,239907
0,298314
0,418267
0,575904
0,874532
12,0738
| 1
1,115
11
12,5
15,8
19,1
23,75
33,3
45,85
69,625
961,25
| | Mq
| 1
2
3
4
5
6
7
8
9
10
11
12
| 1
1
2
2
2
2
2
2
2
2
3
3
| 12,0053
11,4207
10,3929
9,81870
8,84445
8,14038
7,40986
6,44539
5,66962
4,79614
3,15396
2,24924
| 0,0440796
0,0463361
0,203675
0,215585
0,239333
0,260033
0,285669
0,328415
0,373352
0,441347
1,51007
2,11748
| 26,2627
24,9838
11,3676
10,7396
9,67398
8,90388
8,10484
7,04991
2,20138
5,24598
2,29985
1,64014
| 3141,62
2843,10
588,595
525,355
426,272
361,106
299,202
226,383
175,167
125,352
24,0922
12,2528
| 0,0105458
0,0116531
0,112576
0,126128
0,155445
0,183497
0,221461
0,292698
0,378277
0,528607
4,12552
8,11183
| 1
1,105
10,675
11,96
14,74
17,4
21
27,755
35,87
50,125
391,2
769,2
|
Теперь выражение (187) примет вид
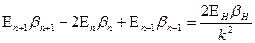 . (188) . (188)
Отсюда находим
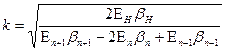 , (189) , (189)
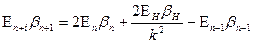 . (190) . (190)
Для элементов, порядковые номера которых отличаются на 2, 3 и 4 единицы, выполняются равенства:
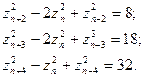 (191) (191)
Замечаем, что в правых частях уравнений (187) и (191) стоят числа, равные числу элементов в периодах периодической системы. Формулы для вычисления значений k для этих случаев имеют вид
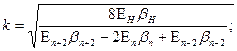
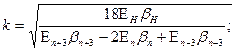 (192) (192)
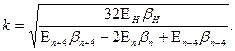
Полученные формулы для расчета ионизационных потенциалов не позволяют учитывать эффект движения. Ими можно пользоваться только в случаях, когда электроны в атомах движутся с малыми скоростями. Чтобы производить точные расчеты, с учетом эффекта движения, нужно знать скорости движения электронов в атомах. Выразив зарядовые числа в формуле (187) через орбитальные скорости электронов с помощью формулы (112), получим уравнение, позволяющее вычислять без учета эффекта движения орбитальные скорости любого электрона в любом атоме:
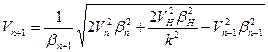 . (193) . (193)
Теперь полную энергию системы “электрон-атом” можно определить по формуле (104), которая с учетом зависимости (76/) преобразуется к виду
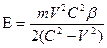 . (194) . (194)
Согласно теории относительности, если тело движется со скоростью, значительно меньшей скорости света, то его кинетическую энергию можно с достаточной точностью вычислить по формуле
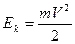 . .
Если тело движется с большой скоростью, то тогда кинетическая энергия будет равна
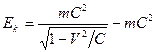 . (195) . (195)
Последняя формула выведена для частиц, ускоряемых в ускорителях, но считается верной для любых других возможных случаев. При выводе формулы (195) были допущены ошибки. Так, сила, с которой электрическое поле в ускорителе действует на частицу, равна
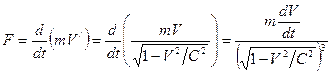 . (196) . (196)
Согласно этому выражению по мере увеличения скорости частицы сила, действующая на нее, непрерывно растет и при приближении скорости частицы к скорости света сила стремится к бесконечности. Однако это противоречит общепризнанному факту конечности скорости распространения взаимодействия. В соответствии с этим сила, действующая на частицу, наоборот, должна стремиться к нулю.
В первых скобках уравнения (196) мы вместо произведения mV записали mV/, тем самым показали, что не масса частицы m растет с увеличением ее скорости, а сама скорость является величиной, зависящей от эффекта движения. Как показано выше (76/),
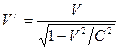 . .
Уравнение (196), записанное в таком виде, точно описывает зависимость силы, действующей на движущийся электрон в атоме, от его скорости. Согласно теории относительности кинетическая энергия равна
 . (197) . (197)
После интегрирования получим формулу (195). Эту формулу нельзя применять и для определения кинетической энергии электронов в атомах, так как при ее выводе допущена ошибка. В формуле (197) сомножитель V записан без учета эффекта движения. Правильное выражение для кинетической энергии имеет вид
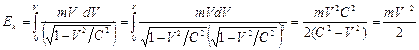 . (198) . (198)
Полная энергия системы “электрон-атом” будет равна
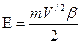 , (199) , (199)
что совпадает с формулой (104), полученной нами ранее, и формулой (194).
Сравнивая формулы (195) и (198), со всей очевидностью убеждаемся в ошибочности выводов, сделанных на основе формулы (195). Энергия не может превращаться в массу, а масса – в энергию. Бессмысленными, не отражающими реальную действительность являются такие понятия, как энергия покоя и полная энергия, масса покоя и релятивистская масса. В устойчивых атомах скорости электронов не превышают скорость света. Если скорость электрона равна скорости света, то его кинетическую энергию можно определить по формулам
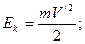 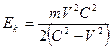 , ,
где V/=C=299,792458 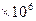 м/c; м/c; 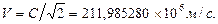 Она будет равна 409355,56·10-19 Дж = 0,255499532 МэВ. Она будет равна 409355,56·10-19 Дж = 0,255499532 МэВ.
В таблице 5.13 приведены ионизационные потенциалы для 36 элементов. Нумерация электронов идет в направлении от ядра к периферии атома. Расчет проводился последовательно: вначале для одноэлектронных ионов, затем для двухэлектронных и т.д. Значения k определялись по формуле (189), а ионизационные потенциалы по формулам (193, 199). Результаты расчетов хорошо согласуются с экспериментальными данными [73, 96, 97]. Теперь по методике, изложенной выше, можно рассчитать параметры орбит для всех 36 элементов. Никаких принципиальных трудностей нет для вычисления ионизационных потенциалов и параметров орбит электронов у всех элементов периодической таблицы.
Химические и ряд физических свойств элементов обусловлены энергией связи наружных электронов с атомами. Энергия связи, а следовательно, и свойства имеют периодическую зависимость от порядкового номера элемента в таблице Менделеева. Если сравнить первые потенциалы ионизации у всех атомов [78], то можно четко выделить семь периодов, что и отражено в таблице Менделеева. Если же сравнить потенциалы ионизации у всех ионов с разными зарядами ядер, но с одинаковым количеством электронов, то так же четко можно различить у известных нам элементов 12 периодов, которые приведены в таблице 5.14. В таблице приведен также 13-й период для элементов, которые, возможно, существуют во Вселенной в условиях, отличных от условий Солнечной системы.
Таблица 5.14 позволяет более точно установить зависимость химических свойств атомов от их строения. На рис. 5.10 показано, как идет заполнение электронных слоев в атомах. Орбиты изображены в масштабе по данным таблицы 5.12. В первом слое у всех атомов содержатся два электрона. В атоме водорода в этом слое имеется только один электрон. При переходе от атома к атому размеры слоя уменьшаются, но количество электронов не изменяется. Второй слой содержит восемь электронов. Заполнение этого слоя начинается в атоме лития и заканчивается в атоме неона. Заполнение третьего слоя начинается в атоме натрия и заканчивается в атоме аргона. В таблице 5.15 показано, как идет заполнение электронных слоев у всех атомов, приведенных в таблице 5.14. Число слоев в атоме соответствует номеру периода, в котором он находится. Максимально возможное число электронов в слое соответствует числу элементов в периоде, в котором начал заполняться этот слой. В первом слое оба электрона находятся в первом стационарном состоянии. Восемь электронов второго слоя находятся во втором стационарном состоянии. Электроны третьего и четвертого слоев находятся в третьем стационарном состоянии, а электроны всех остальных слоев – в четвертом.
Распределение электронов в атомах, принятое сегодня [98], ошибочно. Оно противоречит характеру изменения ионизационных потенциалов в атомах [78]. Согласно таблице 5.14 один период содержит два элемента, шесть периодов содержат по восемь элементов, четыре по десять элементов и два по четырнадцать элементов. В некоторых периодах наблюдается одинаковая закономерность изменения свойств элементов по мере увеличения числа электронов во внешнем слое атома. Такие периоды будем называть подобными. Так, подобными являются второй и третий периоды, начинающиеся с щелочных элементов; пятый, седьмой, десятый и тринадцатый, начинающиеся с элементов группы меди; четвертый, шестой, девятый и двенадцатый, содержащие по 10 элементов; восьмой и одиннадцатый, содержащие по 14 элементов.
Таблица 5.13
Энергия ионизации атомов
| №
| Символ элемента
| Номер электрона
| | 1
| 2
| 3
| 4
| 5
| 6
| 7
| 8
| 9
| 10
| 11
| 12
| | k = 1
| k = 2
| k = 3
| | 1
| 2
| 3
| 4
| 5
| 6
| 7
| 8
| 9
| 10
| 11
| 12
| 13
| 14
| | 1
| H
| 13,598
|
|
|
|
|
|
|
|
|
|
|
| | 2
| He
| 54,424
| 24,588
|
|
|
|
|
|
|
|
|
|
| | 3
| Li
| 122,49
| 75,641
| 5,2956
|
|
|
|
|
|
|
|
|
| | 4
| Be
| 217,85
| 153,95
| 18,213
| 9,3228
|
|
|
|
|
|
|
|
| | 5
| B
| 340,56
| 259,58
| 37,936
| 25,155
| 8,2981
|
|
|
|
|
|
|
| | 6
| C
| 490,70
| 392,58
| 64,477
| 47,913
| 24,463
| 11,260
|
|
|
|
|
|
| | 7
| N
| 668,36
| 553,04
| 97,857
| 77,470
| 47,435
| 29,602
| 14,534
|
|
|
|
|
| | 8
| O
| 873,67
| 741,07
| 138,06
| 113,88
| 77,202
| 54,759
| 35,118
| 13,618
|
|
|
|
| | 9
| F
| 1106,7
| 956,79
| 185,03
| 157,09
| 113,78
| 86,724
| 62,520
| 34,791
| 17,423
|
|
|
| | 10
| Ne
| 1367,9
| 1200,3
| 238,85
| 207,12
| 157,18
| 125,51
| 96,730
| 63,101
| 40,964
| 21,565
|
|
| | 11
| Na
| 1656,9
| 1471,9
| 299,51
| 264,00
| 207,41
| 171,11
| 137,76
| 98,040
| 71,327
| 47,287
| 5,1391
|
| | 12
| Mq
| 1974,2
| 1771,6
| 367,02
| 327,71
| 264,48
| 223,55
| 185,61
| 139,80
| 108,50
| 79,840
| 15,035
| 7,6463
| | 13
| Al
| 2320,1
| 2099,6
| 441,40
| 398,28
| 328,39
| 282,82
| 240,30
| 188,38
| 152,49
| 119,19
| 28,448
| 18,828
| | 14
| Si
| 2694,6
| 2456,2
| 522,64
| 475,72
| 399,16
| 348,94
| 301,83
| 243,80
| 203,31
| 165,37
| 45,192
| 33,493
| | 15
| P
| 3098,2
| 2841,6
| 610,77
| 560,04
| 476,79
| 421,93
| 370,21
| 306,06
| 260,97
| 218,39
| 64,860
| 51,369
| | 16
| S
| 3530,9
| 3256,1
| 705,81
| 651,25
| 561,30
| 501,78
| 445,45
| 375,18
| 325,48
| 278,24
| 88,600
| 72,268
| | 17
| Cl
| 3993,2
| 3700,0
| 807,76
| 749,37
| 652,71
| 588,51
| 527,57
| 451,15
| 396,84
| 344,94
| 115,36
| 96,190
| | 18
| Ar
| 4485,3
| 4173,4
| 916,64
| 854,41
| 751,02
| 682,15
| 616,58
| 534,01
| 475,06
| 418,49
| 145,14
| 123,14
| | 19
| K
| 5007,5
| 4676,7
| 1032,5
| 966,39
| 856,26
| 782,74
| 712,49
| 623,75
| 560,17
| 498,92
| 177,94
| 153,11
|
Продолжение табл. 5.13
| 1
| 2
| 3
| 4
| 5
| 6
| 7
| 8
| 9
| 10
| 11
| 12
| 13
| 14
| | 20
| Ca
| 5560,3
| 5210,4
| 1155,3
| 1085,3
| 968,43
| 890,17
| 815,31
| 720,39
| 652,17
| 586,24
| 213,77
| 186,09
| | 21
| Sc
| 6144,0
| 5774,7
| 1285,1
| 1211,2
| 1087,6
| 1004,6
| 925,07
| 823,96
| 751,08
| 680,45
| 252,62
| 222,10
| | 22
| Ti
| 6758,9
| 6370,1
| 1421,9
| 1344,1
| 1213,7
| 1126,0
| 1041,8
| 934,46
| 856,91
| 781,57
| 294,50
| 261,14
| | 23
| V
| 7405,6
| 6996,9
| 1565,7
| 1484,1
| 1346,8
| 1254,3
| 1165,5
| 1051,9
| 969,69
| 889,63
| 339,40
| 308,20
| | 24
| Cr
| 8084,3
| 7655,5
| 1716,6
| 1631,1
| 1486,9
| 1389,7
| 1296,1
| 1176,3
| 1089,4
| 1004,6
| 387,33
| 354,80
| | 25
| Mn
| 8795,7
| 8346,5
| 1874,5
| 1785,1
| 1634,1
| 1532,1
| 1433,8
| 1307,8
| 1216,1
| 1126,6
| 438,28
| 406,69
| | 26
| Fe
| 9540,3
| 9070,3
| 2039,6
| 1946,2
| 1788,3
| 1681,6
| 1578,5
| 1446,2
| 1349,9
| 1255,6
| 492,29
| 461,15
| | 27
| Co
| 10318
| 9827,4
| 2211,8
| 2114,5
| 1949,7
| 1838,1
| 1730,3
| 1591,7
| 1490,6
| 1391,5
| 549,35
| 518,66
| | 28
| Ni
| 11131
| 10618
| 2391,2
| 2289,9
| 2118,1
| 2001,7
| 1889,2
| 1744,2
| 1638,4
| 1534,5
| 609,48
| 579,24
| | 29
| Cu
| 11978
| 11444
| 2577,7
| 2472,5
| 2293,7
| 2172,5
| 2055,2
| 1903,8
| 1793,2
| 1684,5
| 672,67
| 642,89
| | 30
| Zn
| 12860
| 12304
| 2771,5
| 2662,2
| 2476,5
| 2390,9
| 2228,3
| 2070,5
| 1955,2
| 1841,7
| 739,94
| 709,69
| | 31
| Ga
| 13779
| 13200
| 2972,5
| 2859,2
| 2666,5
| 2535,5
| 2408,5
| 2244,4
| 2124,2
| 2005,9
| 808.28
| 779,40
| | 32
| Ge
| 14735
| 14133
| 3180,8
| 3063,5
| 2863,7
| 2727,8
| 2596,0
| 2425,5
| 2300,2
| 2177,2
| 880,07
| 852,27
| | 33
| As
| 15728
| 15102
| 3396,5
| 3275,2
| 3068,2
| 2927,3
| 2790,7
| 2613,7
| 2483,8
| 2355,7
| 956,22
| 928,23
| | 34
| Se
| 16759
| 16109
| 3619,5
| 3494,2
| 3279,9
| 3134,2
| 2997,6
| 2809,1
| 2674,4
| 2541,4
| 1034,8
| 1007,3
| | 35
| Br
| 17830
| 17155
| 3849,9
| 3720,7
| 3499,1
| 3348,3
| 3201,9
| 3011,9
| 2872,2
| 2734,3
| 1116,5
| 1089,4
| | 36
| Kr
| 18939
| 18240
| 4087,8
| 3954,5
| 3725,5
| 3569,8
| 3418,4
| 3221,9
| 3077,3
| 2934,5
| 1201,3
| 1174,7
|
Продолжение табл. 5.13
| №
| Символ элемента
| Номер электрона
| | 13
| 14
| 15
| 16
| 17
| 18
| 19
| 20
| 21
| 22
| 23
| 24
| | k=3
| | 1
| 2
| 15
| 16
| 17
| 18
| 19
| 20
| 21
| 22
| 23
| 24
| 25
| 26
| | 13
| Al
| 5,9858
|
|
|
|
|
|
|
|
|
|
|
| | 14
| Si
| 16,346
| 8,1517
|
|
|
|
|
|
|
|
|
|
| | 15
| P
| 30,178
| 19,726
| 10,487
|
|
|
|
|
|
|
|
|
| | 16
| S
| 47,308
| 34,828
| 23,334
| 10,360
|
|
|
|
|
|
|
|
| | 17
| Cl
| 67,457
| 53,466
| 39,613
| 23,814
| 12,968
|
|
|
|
|
|
|
| | 18
| Ar
| 90,632
| 75,127
| 59,811
| 40,742
| 27,630
| 15,760
|
|
|
|
|
|
| | 19
| K
| 116,83
| 99,812
| 83,032
| 60,914
| 45,726
| 31,726
| 4,3407
|
|
|
|
|
| | 20
| Ca
| 146,05
| 127,52
| 109,28
| 84,109
| 67,101
| 50,914
| 11,872
| 6,1132
|
|
|
|
| | 21
| Sc
| 178,30
| 158,25
| 138,55
| 110,32
| 91,498
| 73,474
| 24,760
| 12,771
| 6,562
|
|
|
| | 22
| Ti
| 213,57
| 192,01
| 170,85
| 139,57
| 118,92
| 99,060
| 43,268
| 27,492
| 13,58
| 6,819
|
|
| | 23
| V
| 256,16
| 230,49
| 206,18
| 171,84
| 149,36
| 127,67
| 64,799
| 46,705
| 29,31
| 14,66
| 6,740
|
| | 24
| Cr
| 296,18
| 271,12
| 244,34
| 209,14
| 184,73
| 159,30
| 90,563
| 69,041
| 49,20
| 30,96
| 16,50
| 6,766
| | 25
| Mn
| 343,32
| 314,91
| 286,25
| 248,15
| 221,85
| 195,34
| 119,30
| 95,449
| 72,41
| 51,28
| 33,67
| 15,64
| | 26
| Fe
| 391,35
| 361,58
| 331,18
| 290,18
| 262,26
| 234,62
| 151,15
| 124,88
| 99,44
| 74,62
| 53,86
| 30,65
| | 27
| Co
| 442,4
| 411,30
| 379,70
| 335,68
| 305,52
| 276,79
| 185,98
| 157,33
| 129,2
| 101,0
| 79,86
| 51,95
| | 28
| Ni
| 496,56
| 464,07
| 430,84
| 383,89
| 351,83
| 322,01
| 223,85
| 192,95
| 161,9
| 132,8
| 108,9
| 76,28
| | 29
| Cu
| 553,75
| 519,90
| 485,03
| 435,16
| 401,19
| 370,27
| 264,75
| 231,51
| 198,9
| 167,7
| 140,9
| 103,6
| | 30
| Zn
| 614,01
| 578,79
| 543,87
| 489,48
| 453,60
| 421,58
| 308,71
| 273,11
| 238,8
| 205,7
| 176,0
| 134,0
| | 31
| Ga
| 677,33
| 640,75
| 602,60
| 546,86
| 509,07
| 475,95
| 355,70
| 317,76
| 282,9
| 246,6
| 214,1
| 174,0
|
Продолжение табл. 5.13
| 1
| 2
| 15
| 16
| 17
| 18
| 19
| 20
| 21
| 22
| 23
| 24
| 25
| 26
| | 32
| Ge
| 743,73
| 705,78
| 665,98
| 607,30
| 567,60
| 533,38
| 405,75
| 365,45
| 330,0
| 290,7
| 255,3
| 217,0
| | 33
| As
| 813,20
| 773,88
| 732,44
| 670,72
| 629,20
| 593,88
| 458,86
| 416,20
| 380,2
| 337,8
| 299,5
| 259,1
| | 34
| Se
| 885,75
| 845,06
| 801,97
| 737,40
| 693,86
| 657,44
| 515,02
| 470,00
| 433,4
| 387,9
| 346,3
| 304,2
| | 35
| Br
| 961,40
| 916,03
| 874,58
| 807,06
| 761,60
| 724,07
| 574,24
| 526,76
| 489,5
| 441,0
| 396,8
| 352,4
| | 36
| kr
| 1040,1
| 996,69
| 950,29
| 879,80
| 832,41
| 793,78
| 636,52
| 586,89
| 548,6
| 497,1
| 450,1
| 403,6
|
Продолжение табл. 5.13
| №
| Символ элемента
| Номер электрона
| | 25
| 26
| 27
| 28
| 29
| 30
| 31
| 32
| 33
| 34
| 35
| 36
| | k = 3
| k = 4
| | 25
| Mn
| 7,432
|
|
|
|
|
|
|
|
|
|
|
| | 26
| Fe
| 16,19
| 7,896
|
|
|
|
|
|
|
|
|
|
| | 27
| Co
| 33,49
| 17,08
| 7,860
|
|
|
|
|
|
|
|
|
| | 28
| Ni
| 53,81
| 35,32
| 18,17
| 7,633
|
|
|
|
|
|
|
|
| | 29
| Cu
| 81,32
| 59,70
| 36,84
| 20,293
| 77,24
|
|
|
|
|
|
|
| | 30
| Zn
| 111,9
| 87,11
| 59,57
| 39,72
| 17,96
| 9,394
|
|
|
|
|
|
| | 31
| Ga
| 145,5
| 117,5
| 88,72
| 64,62
| 30,73
| 20,51
| 5,999
|
|
|
|
|
| | 32
| Ge
| 182,1
| 151,0
| 120,9
| 93,55
| 45,71
| 34,21
| 15,93
| 7,899
|
|
|
|
| | 33
| As
| 221,8
| 187,5
| 154,7
| 123,2
| 62,65
| 50,19
| 28,39
| 18,59
| 9,789
|
|
|
| | 34
| Se
| 264,5
| 227,1
| 191,5
| 155,8
| 81,55
| 68,26
| 42,95
| 30,82
| 21,16
| 9,752
|
|
| | 35
| Br
| 310,1
| 269,7
| 231,8
| 191,5
| 102,4
| 88,41
| 59,60
| 46,07
| 35,90
| 21,81
| 11,81
|
| | 36
| Kr
| 358,8
| 315,3
| 275,1
| 230,2
| 125,2
| 110,6
| 78,35
| 64,35
| 52,50
| 36,95
| 24,36
| 14,00
|
Таблица 5.14
Периодический закон
| Период
|
Номер элемента в периоде
| | 1
| 2
| 3
| 4
| 5
| 6
| 7
| 8
| 9
| 10
| 11
| 12
| 13
| 14
| | I
| H
| He
|
|
|
|
|
|
|
|
|
|
|
|
| | II
| Li
| Be
| B
| C
| N
| O
| F
| Nl
|
|
|
|
|
|
| | III
| Na
| Mq
| Al
| Si
| P
| S
| Cl
| Ar
|
|
|
|
|
|
| | IV
| K
| Ca
| Sc
| Ti
| V
| Cr
| Mn
| Fe
| Co
| Ni
|
|
|
|
| | V
| Cu
| Zn
| Ga
| Ge
| As
| Se
| Br
| Kr
|
|
|
|
|
|
| | VI
| Rb
| Sr
| Y
| Zr
| Nb
| Mo
| Tc
| Ru
| Rh
| Pd
|
|
|
|
| | VII
| Aq
| Cd
| Jn
| Sn
| Sb
| Te
| J
| Xe
|
|
|
|
|
|
| | VIII
| Cs
| Ba
| La
| Cl
| Pr
| Nd
| Pm
| Sm
| Eu
| Gd
| Tb
| Ду
| Ho
| Er
| | IX
| Tm
| Yb
| Lu
| Hf
| Ta
| W
| Rl
| Os
| Jr
| Pt
|
|
|
|
| | X
| Au
| Hq
| Tl
| Pb
| Bi
| Po
| At
| Rn
|
|
|
|
|
|
| | XI
| Fr
| Ra
| Ac
| Th
| Pa
| U
| Np
| Pu
| Am
| Cm
| Bk
| Cf
| Es
| Fm
| | XII
| Md
| No
| Lr
| Ku
| Ns
| 106
| 107
| 108
| 109
| 110
|
|
|
|
| | XIII
| 111
| 112
| 113
| 114
| 115
| 116
| 117
| 118
|
|
|
|
|
|
|
Таблица 5.15
|



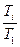
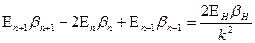 . (188)
. (188) 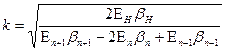 , (189)
, (189)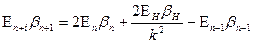 . (190)
. (190)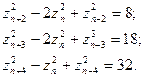 (191)
(191)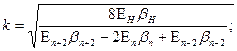
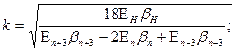 (192)
(192)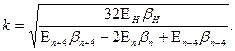
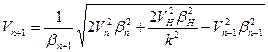 . (193)
. (193)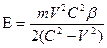 . (194)
. (194)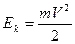 .
.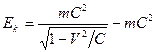 . (195)
. (195)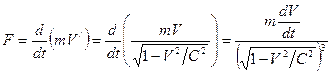 . (196)
. (196)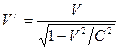 .
. . (197)
. (197)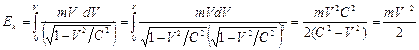 . (198)
. (198)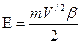 , (199)
, (199)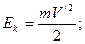
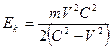 ,
,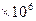 м/c;
м/c; 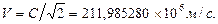 Она будет равна 409355,56·10-19 Дж = 0,255499532 МэВ.
Она будет равна 409355,56·10-19 Дж = 0,255499532 МэВ.


