
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Медико-биологическое значение гидроксикарбоновых кислотСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
Молочная кислота CH3CH(OH)COOH была впервые обнаружена Шееле (1780) в прокисшем молоке, отсюда и получила название. Благодаря наличию в молекуле асимметрического атома углерода молочная кислота может существовать в виде двух оптически активных энантиомеров – D- и L-форм – и оптически неактивной рацемической формы. Последняя представляет собой молочную кислоту брожения. L–Молочная кислота, образуется в мышечной ткани как продукт расщепления и дальнейшего превращения полисахарида гликогена. D–Молочная кислота может быть получена под действием микроорганизмов. Соли и сложные эфиры молочной кислоты называются лактатами. Важно отметить, что соли и эфиры L-молочной кислоты являются левовращающими, а соли и эфиры D–молочной кислоты – правовращающими. Яблочная кислота HOOCCH2CH(OH)COOH – представитель гидроксидикарбоновых кислот. Яблочная кислота, как и молочная, существует в виде двух энантиомеров. L–яблочная кислота, содержится в незрелых яблоках, плодах рябины и барбариса. Лимонная кислота – наиболее распространенная гидрокситрикарбоновая кислота. Она содержится в плодах цитрусовых (в лимонах её 6-8% от сухой массы), некоторых ягодах и фруктах. Лимонная кислота и её соли (цитраты) широко используются в пищевой промышленности и фармации. Салициловая кислота о -HOC6H4COOH представляет собой кристаллическое вещество, плохо растворимое в воде. По кислотности (р К а=2,98) она превосходит почти все монозамещённые бензойные кислоты, в том числе и с электроноакцепторными заместителями. Салициловая кислота обладает антисептическими свойствами и находит применение, как в медицине, так и как консервант некоторых пищевых продуктов. Но ещё более широко используются в медицинской практике производные салициловой кислоты по обеим функциональным группам. Главным образом, это сложные эфиры по карбоксильной группе – метилсалицат и фенилсалицат, имеющий торговое название салол, и по фенольному гидроксилу – ацетилсалициловая кислота, для которой одно из многочисленных торговых названий - аспирин.
Тема 5. УГЛЕВОДЫ. СТРОЕНИЕ И СВОЙСТВА МОНО-, ДИ-, И ПОЛИСАХАРИДОВ. АКТУАЛЬНОСТЬ ТЕМЫ Углеводы – гетерофункциональные соединения общей формулы Cn(H2O)m, что исторически и определило общее название данного класса соединений. Углеводы играют значительную роль в процессах жизнедеятельности животной и растительной клетки, выполняя энергетическую, резервную и структурные функции. Углеводы по праву считаются основой существования животных и растительных организмов. Основным моносахаридом растительной и животной клетки является глюкоза, топливная молекула, являющаяся основным источником энергии, участвующая в биосинтезе резервных полисахаридов: крахмала (растения) и гликогена (высшие животные). Глюкоза может окисляться как в аэробных, так и в анаэробных условиях, обеспечивая энергетические потребности организма более чем на 60%. Моносахариды рибоза и дезоксирибоза являются структурными компонентами нуклеиновых кислот – биополимеров, принимающих участие в сохранении и передаче генетической информации. В комплексе с белками углеводы образуют гормоны, ферменты, секреты слюнных и слизистых желёз. Полисахариды– гиалуроновая кислота и хондроитин сульфаты выполняют структурную функцию, являясь основными структурными компонентами мягких соединительных тканей. Полисахарид гепарин входит в состав липопротеинлипазы плазмы крови и ферментов свёртывания крови. Представления о химической природе углеводов, их строении и специфических свойствах лежат в основе понимания процессов переваривания углеводов, их метаболизма и путей энергетического обмена в организме человека.
ЦЕЛИ ОБУЧЕНИЯ ОБЩАЯ ЦЕЛЬ: Уметь классифицировать углеводы по их способности к гидролизу, по их химической природе, для объяснения особенностей их химического поведения и различия их биохимических функций.
КОНКРЕТНЫЕ ЦЕЛИ. УМЕТЬ: 1. Интерпретировать понятия моносахарид, линейная и циклическая структура моносахарида. 2. Интерпретировать химические поведение моносахаридов с точки зрения их химического строения. 3. Интерпретировать реакцию гидролиза как ключевуюреакциюметаболизма олиго- и полисахаридов. 4. Интерпретировать биологическую роль моно-, ди- и полисахаридов в процессах энергетического обмена. 5. Трактовать биологическую роль гетерополисахаридов соединительной ткани: хондроитин сульфата, гиалуроновой кислоты, гепарина. ТЕОРЕТИЧЕСКИЕ ВОПРОСЫ 1. Классификация углеводов. Моно-, олиго- и полисахариды. 2. Строение и свойства моносахаридов. Классификация по числу атомов углерода в молекуле и по природе старшей функциональной группы. 3. Оптическая изомерия в ряду моносахаридов. Углеводы D- и L-ряда. 4. Особенности поведения моносахаридов в водных растворах. Линейные и циклические формы (Приложение 12). 5. Строение, биологическая роль важнейших моносахаридов: рибоза, дезоксирибоза, глюкоза, галактоза, фруктоза. 6. Химические свойства моносахаридов. Реакции окисления, восстановления, образования гликозидов. 7. Строение и свойства дисахаридов. Гликозидная связь. Реакции гидролиза. Строение, свойства и биологическая роль дисахаридов: мальтоза, лактоза, сахароза (Приложение 13). 8. Строение и свойства гомополисахаридов: крахмал, гликоген, целлюлоза (Приложение 14). 9. Строение и биологические функции гетерополисахаридов: гиалуроновая кислота, хондроитин сульфат, гепарин (Приложение 15).
Основная литература. 1. Губський Ю.І. Біоорганічна хімія: Підручник. – Вінниця: Нова книга, 2004. – С.217-250
РЕШЕНИЕ ОБУЧАЮЩИХ ЗАДАЧ Задача 1. Напишите структурные формулы D- и L-рибозы. Укажите, конфигурация какого атома углерода определяет отнесение данных веществ к D- и L-ряду. Эталон решения: Рибоза является альдопентозой, т.е. содержит пять атомов углерода и альдегидную группу. D- иL- рибоза являются энантиомерами и представляют собой зеркальные отражения друг друга. Отнесение углевода к D- и L-ряду проводится по конфигурации последнего хирального центра в стандартной проекции Фишера.В ряду пентоз это атом углерода С4. Если в стандартной проекции Фишера ОН группа у атома С4 расположена слева, углевод относится к L ряду, если справа – к D ряду.
Задача 2. Напишите схему превращения D-глюкозы в циклическую a-форму (проекции Фишера, Толленса и Хеуорса). Эталон решения: Глюкоза является альдогексозой, ее структурная формула в стандартной проекции Фишера приведена ниже:
Конфигурация атома С5 в молекуле говорит о том, что представленная формула отвечает D- глюкозе. В водных растворах моносахариды образуют циклические полуацетали, образование которых связано с нуклеофильным присоединением ОН к карбонильной группе. Стабильными являются, пяти- и шестичленные циклические полуацетали, следовательно, в реакции циклизации участвует ОН группа при атоме углерода С5.
При циклизации атом углерода С1 становится хиральным, следовательно происходит образование равновесной смеси двух циклических форм, отличающихся только конфигурацией атома углерода С1 (аномеры). Для того, что бы превратить циклическую проекцию Толленса в проекцию Хеуорса воспользуемся следующими правилами: 1. Представим молекулу в виде шестичленной циклической структуры, проведем нумерацию атомов углерода как это представлено на схеме:
2. Проведем вертикальные линии, представляющие собой связи С-Н и С-ОН для каждого атома углерода. 3. Расставим Н и ОН группы, пользуясь следующими правилами: а) Для углеводов D-ряда все группы, записанные внутри цикла в проекции Толленса, в проекции Хеуорса пишутся внизу. В данном примере это ОН группы у атомов С2 и С4, и протон у атома С3. Все группы, записанные вне цикла в проекции Толленса, в проекции Хеуорса записываются сверху. В данном примере это протоны у атомов С2 и С4, и ОН группа у атома С3. б) Для углеводов D-ряда шестая СН2ОН группа всегда записывается наверху. в) Для первого атома углерода (полуацетальный атом углерода) ОН пишется внизу для a-аномера и наверху для b-аномера.
4. В условии данной задачи требовалось составить a-циклическую форму D- глюкозы. Ее название по заместительной номенклатуре IUPAC: a-D-глюкопираноза.
Задача 3. Напишите уравнение реакции гидролиза a-лактозы, назовите продукты реакции. Эталон решения: Лактоза являются восстанавливающим дисахаридом, следовательно, содержит свободную полуацетальную ОН группу и способна существовать как в двух формах a- и b. Молекула a-лактозы состоит из двух моносахаридных единиц: b-галактозы и a-глюкозы, следовательно, образует их при гидролизе, в результате разрываb-1,4-гликозидной связи:
НАБОР ЗАДАНИЙ ДЛЯ КОНТРОЛЯ САМОПОДГОТОВКИ Задание 1. Назовите следующее соединение.
А. Глюкоза В. Фруктоза С. Галактоза D. Рибоза Е. Дезоксирибоза
Задание 2. Для моносахаридов характерно явление оксо-цикло-таутомерии. Что обозначает данный термин? А. Обратимый переход моносахаридов в дисахариды В. Обратимый переход альдоз в кетозы С. Необратимый переход гексоз в пентозы D. Обратимый переход оксоформы в циклическую Е. Необратимый переход оксоформы в циклическую Задание 3. Дезоксирибоза входит в состав дезоксирибонуклеиновых кислот - ДНК. Укажите класс углеводов, к которому она относится: А. Пентоза В. Гексоза С. Кетоза D. Гомополисахарид Е. Дисахарид
Задание 4. Моносахариды – гетрофункциональные соединения, содержащие гидрокси- и карбонильную группы. Укажите название приведенного соединения: A. D-фруктоза B. b-D-2-дезоксирибофураноза C. α-D-гюкопираноза D. α-D-галактопираноза E. D-рибоза
Задание 5. В результате какой реакции можно получить из глюкозы глюконовую кислоту? А. Окисление бромной водой В. Окисление азотной кислотой С. Восстановление в присутствии катализатора D. Окисление KMnO4 Е. Нагревание в кислой среде Задание 6. Какой реагент может быть использован для превращения галактозы в галактаровую кислоту: А. С2Н5ОН В. НСl С. Н3РО4 D. NаОН Е. НNО3 Задание 7. В результате какой реакции из глюкозы можно получить шестиатомный спирт сорбит? А. Окисление бромной водой В. Окисление азотной кислотой С. Восстановление в присутствии катализатора D. Окисление гидроксидом меди (рективом Фелинга) Е. Нагревание в кислой среде Задание 8. Какие продукты образуются при гидролизе лактозы? А. β-D-галактопираноза и α- D-глюкопираноза В. α-D-галактопираноза и α- D-глюкопираноза С. β-D-фруктофураноза и α- D-глюкопираноза D. две молекулы α-D-глюкопиранозы Е. две молекулы β-D-фруктофуранозы Задание 9. Выберите невосстанавливающий дисахарид из следующих веществ: A. Лактоза B. Сахароза C. Мальтоза D. Целлобиоза E. Галактоза Задание 10. Какие типы гликозидной связи присутствуют в молекуле гликогена? А. α-1,4 и β-1,4-гликозидные В. α-1,4 и β-1,6-гликозидные С. α-1,4 и α-1,6-гликозидные D. только α-1,4-гликозидные Е. только β-1,4-гликозидные Задание 11. Какие структурные компоненты входят в состав гиалуроновой кислоты? А. β-D-глюкуроновая кислота и N-ацетил-6-сульфогалактозамин В. β-D-глюкуроновая кислота и N-ацетилглюкозамин С. β-D-глюкуроновая кислота и N-ацетилглюкозаминсульфат D. N-ацетилглюкозаминсульфат и N-ацетил-6-сульфогалактозамин Е. N-ацетил-6-сульфогалактозамин и D-идуроновая кислота Задание 12. Гетерополисахариды являются важными компонентами соединительной ткани. Где преимущественно обнаруживается хондроитинсульфат? А. Тучные клетки В. Суставная жидкость С. Хрящи D. Зубы Е. Лимфоциты Эталоныответов: 1 – A, 2 – D, 3 – A, 4 – C,5 – A, 6 – E, 7 – C, 8 – A, 9 – B, 10 – C, 11 – B, 12 - C. Приложение 12.
|
||||||||
|
Последнее изменение этой страницы: 2016-04-18; просмотров: 805; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.144.15.34 (0.012 с.) |

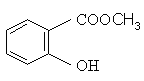 Метилсалацилат
Метилсалацилат  Аспирин
Аспирин











