
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Общая характеристика металловСодержание книги
Поиск на нашем сайте
Металлы выделяются среди других элементов периодической системы, прежде всего своими физическими свойствами: 1. Они являются особенно хорошими проводниками теплоты и электрического тока. 2. Они обладают металлическим блеском, т. е. хорошо отражают свет. 3. Они ковки и пластичны. 4. Они легко образуют сплавы. Несмотря на проявление общих свойств, различие между металлами нередко оказывается весьма существенным. Например, вольфрам плавится при 3380˚С, а цезий – при 28,5˚С. Вместе с тем у металлов, расположенных рядом друг с другом в периодической системе, часто проявляется близость свойств, в том числе химических. Такие металлы принято объединять в специальные группы. Выделяют следующие группы металлов: щелочные (Li, Na, K, Rb, Cs), щелочноземельные (Be, Mg, Ca, Sr, Ba), переходные элементы (элементы IB – VIIIB групп), лантаноиды ( Физические и химические свойства металлов в значительной мере определяются особенностями электронного строения их атомов. На внешнем электронном уровне атомов металлов обычно три и менее электрона. Например: Na 1s22s22p63s1, Cu 1s22s22p63s23p63d104s1, Fe 1s22s22p63s23p63d64s2, Al 1s22s22p63s23p1. Высокая электропроводность металлов обусловлена подвижностью их валентных электронов. С позиций зонной теории металлов важным является то, что при малом числе валентных электронов в атомах металла зона проводимости не полностью заполнена электронами и создаются благоприятные условия для электронной проводимости. Электропроводность металлов понижается с повышением температуры. Зонная теория объсняет причины различия свойств металлов, полупроводников и диэлектриков. Поверхность металлов отражает свет. Особенностью металлов является отражение света под разными углами, в отличие от многих неметаллов (сера, иод), которые отражают свет под малыми углами. Отражение света металлами связано с поглощением энергии света «свободными» электронами, которые переходят за счет поглощенной энергии в возбужденное состояние и быстро возвращаются в исходное (основное) состояние, испуская энергию в виде света в окружающее пространство. Обычно металлы практически полностью сохраняют спектр световых волн при их отражении. Но некоторые металлы, например золото, поглощают световые волны некоторых частот в большей мере, чем другие, и поэтому приобретают цвет. Ковкость (способность к расплющиванию) и пластичность (способность вытягиваться в проволоку и ленту)металлов прявляются в том, что их структура может деформироваться под действием внешних сил. Пластичность металлов уменьшается в ряду Плотность металлов, как и других прстых веществ, находится в периодической зависимости от порядкового номера элемента. К легким ( Вследствие ненасыщенности и ненаправленности металлической связи для кристаллических решеток металлов характерна высокая плотность упаковки. Большинство металлов кристаллизуется с образованием гексагональных или кубических (гранецентрированных или объемно центрированных) решеток. Самый твердый из металлов хром – режет стекло, а самые мягкие – калий, рубидий, цезий – легко режутся ножом. Металлы отличаются также своим отношением к магнитным полям. По этому свойству они делятся на три группы: - ферромагнитные металлы – способные намагничиваться под действием слабых магнитных полей (железо, кобальт, никель); - парамагнитные металлы – проявляют слабую способность к намагничиванию (алюминий, титан и большая часть лантаноидов); - диамагнитные металлы – не притягиваются к магниту и даже отталкиваются от него (висмут, олово, медь). Пыль и пары некоторых металлов токсичны. Как известно, токсичность характеризуется предельно-допустимыми концентрациями веществ в рабочей зоне, ПДК (
|
||||
|
Последнее изменение этой страницы: 2021-05-27; просмотров: 102; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.214 (0.01 с.) |

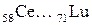 ) и актиноиды (
) и актиноиды (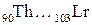 ). Из числа переходных металлов в особую группу выделяют платиновы металлы (Ru, Rh, Pd, Os, Ir, Pt). Все эти металлы являются s-, d- или f-элементами. К металлам относят также некоторые из р-элементов (Al, Ga, In, Sn, Tl, Pb, Bi), которые расположены в нижней части групп периодической системы.
). Из числа переходных металлов в особую группу выделяют платиновы металлы (Ru, Rh, Pd, Os, Ir, Pt). Все эти металлы являются s-, d- или f-элементами. К металлам относят также некоторые из р-элементов (Al, Ga, In, Sn, Tl, Pb, Bi), которые расположены в нижней части групп периодической системы.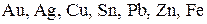 ... Золото можно прокатывать в листы, толщиной до 0,003 мм, которые используются для золочения.
... Золото можно прокатывать в листы, толщиной до 0,003 мм, которые используются для золочения. г/см3) относятся s -металлы и алюминий, скандий и титан, минимальную плотность имеет литий (
г/см3) относятся s -металлы и алюминий, скандий и титан, минимальную плотность имеет литий ( г/см3), к тяжелым относятся в основном d -металлы 5-7-го периодов. Максимальную плотность имеет осмий (
г/см3), к тяжелым относятся в основном d -металлы 5-7-го периодов. Максимальную плотность имеет осмий (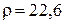 г/см3). Температура плавления металлов также имеет периодическую зависимость от порядкового номера элемента. К лекгоплавким относятся в основном s - и p -элементы, а также d -элементы II группы. К тугоплавким (t пл выше 15000С) принадлежат, в основном, d -металлы IV-VIII групп. Минимальную температуру плавления имеет ртуть (
г/см3). Температура плавления металлов также имеет периодическую зависимость от порядкового номера элемента. К лекгоплавким относятся в основном s - и p -элементы, а также d -элементы II группы. К тугоплавким (t пл выше 15000С) принадлежат, в основном, d -металлы IV-VIII групп. Минимальную температуру плавления имеет ртуть (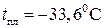 ), максимальную – вольфрам (
), максимальную – вольфрам ( ).
). ). К наиболее токсичным относятся металлы (ПДК -
). К наиболее токсичным относятся металлы (ПДК - 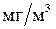 ): Be (10-3), Hg (10-3), Pb (10-2), Cd (10-2), Ag (10-2), Ni, Rh, Tl, In (10-1).
): Be (10-3), Hg (10-3), Pb (10-2), Cd (10-2), Ag (10-2), Ni, Rh, Tl, In (10-1).


