

Мы поможем в написании ваших работ!
ЗНАЕТЕ ЛИ ВЫ?
|
Важнейшие единицы СИ и их соотношение с единицами других систем
Таблица 2.
Приставки для дольных и кратных единиц СИ
| Приставка
| Символ
| Множитель
| Приставка
| Символ
| Множитель
| | Пико
| п
| 10-12
| деци
| д
| 10-1
| | Нано
| н
| 10-9
| кило
| к
| 103
| | Микро
| мк
| 10-6
| мега
| М
| 106
| | Милли
| м
| 10-3
| гекта
| Г
| 109
| | Санти
| с
| 10-2
| терра
| Т
| 1012
|
Таблица 3.
Термодинамические характеристики некоторых веществ при 298 К
| Вещество
|  , кДж/моль , кДж/моль
| 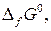 кДж/моль кДж/моль
|  , Дж/(моль ∙К) , Дж/(моль ∙К)
| | Ag (к)
| 0,00
| 0,00
| 42,69
| | AgBr (к)
| -99,16
| -94,9
| 107,1
| | AgCl (к)
| -127,07
| -109,7
| 96,11
| | AgI (к)
| -64,2
| -66,3
| 144,2
| | Ag2O (к)
| -30,56
| -10,82
| 121,81
| | AgO (к)
| -44,6
| -40,8
| 57,78
| | Al (к)
| 0,00
| 0,00
| 28,32
| | Al2O3 (к, корунд)
| -1676
| -1580
| 50,94
| | Au
| 0,00
| 0,00
| 47,65
| | AuCl3 (к)
| -118,4
| -48,53
| 146,64
| | Ba
| 0,00
| 0,00
| 66,94
| | BaO (к)
| -557,9
| -528,4
| 70,29
| | BaCO3 (к)
| -1202
| -1139
| 112,1
| | BaSO4 (к)
| -1352
| -1465
| 131,8
| | Be
| 0,00
| 0,00
| 9,54
| | BeO (к)
| -598,7
| -581,6
| 14,1
| | BeCO3 (к)
| -983,6
| -944,7
| 199,4
| | Bi
| 0,00
| 0,00
| 56,9
| | BiCl3 (к)
| -379,1
| -318,9
| 189,5
| | Br2 (ж)
| 0,00
| 0,00
| 152,3
| | Br2 (г)
| 30,92
| 3,14
| 245,35
| | С (алмаз)
| 1,83
| 2,85
| 2,38
| | С (графит)
| 0,00
| 0,00
| 5,74
| | СО (г)
| -110,5
| -137,14
| 197,54
| | СО2 (г)
| -393,51
| -394,38
| 213,68
| | СОСl2 (г)
| -219,5
| -205,3
| 283,6
| | ССl4 (г)
| -106,7
| -63,95
| 309,7
| | СH4 (г)
| -74,85
| -50,79
| 186,19
| | С2H2 (г)
| 226,75
| 209,2
| 200,8
| | С2H4 (г)
| 52,28
| 68,11
| 219,4
| | С2H6 (г)
| -84,68
| -32,89
| 229,5
| | С3H6 (г)
| 20,42
| 62,7
| 226,9
| | С3H8 (г)
| -104,0
| -23,49
| 269,9
| | С4H8 (г)
| -0,13
| 71,5
| 307,4
| | С4H10 (г)
| -124,7
| -17,15
| 310,0
| | С6H6 (г)
| 82,93
| 129,7
| 269,2
| | С6H6 (ж)
| 49
| 124,5
| 172,8
| | СH3OH (ж)
| -238,6
| -166,23
| 126,8
|
Продолжение табл. 3
| Вещество
|  , кДж/моль , кДж/моль
| 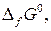 кДж/моль кДж/моль
|  , Дж/(моль∙К) , Дж/(моль∙К)
| | СH3OH (г)
| -201,2
| -161,9
| 239,7
| | С2H5OH (г)
| -235,3
| -167,4
| 278,0
| | С2H5OH (ж)
| -277,7
| -174,76
| 160,7
| | ССl4 (г)
| -106,7
| -64,0
| 309,7
| | Са (к)
| 0,00
| 0,00
| 41,42
| | CaCO3 (к)
| -1207,1
| -1128,76
| 92,88
| | CaCl2 (к)
| -785,8
| -750,2
| 113,8
| | CaO (к)
| -635,5
| -605,2
| 39,7
| | Ca(OH)2 (к)
| -986,2
| -898,5
| 83,4
| | СаSO4 (к)
| -1424
| -1318,3
| 106,7
| | СaSO3 ּ2H2O (к)
| -1762,3
| -1565,2
| 184,1
| | Cd (к)
| 0,00
| 0,00
| 51,76
| | CdO (к)
| -256,1
| -225,0
| 54,8
| | Cd(OH)2 (к)
| -553,2
| -470,2
| 95,4
| | Сl2 (г)
| 0,00
| 0,00
| 222,96
| | Cr (к)
| 0,00
| 0,00
| 23,76
| | Cr2O3 (к)
| -1141
| -1058
| 81,1
| | CrO3 (к)
| -594,5
| -505,8
| 72,0
| | CuCl (к)
| -133,6
| -116,0
| 91,2
| | CuCl2 (к)
| -172,4
| -131,4
| 118,8
| | CuO (к)
| -165
| -127,0
| 42,64
| | CuS (к)
| -48,5
| -48,9
| 66,5
| | F2 (г)
| 0,00
| 0,00
| 202,9
| | Fe (к)
| 0,00
| 0,00
| 27,15
| | FeCO3 (к)
| -747,7
| -673,9
| 92,88
| | FeCl2 (к)
| -341,0
| -301,7
| 120,1
| | FeCl3 (к)
| -390,8
| -328,7
| 154,4
| | FeO (к)
| -263,8
| -244,3
| 58,79
| | Fe2O3 (к)
| -822,16
| -740,98
| 89,96
| | Fe3O4 (к)
| -1117,7
| -1014,2
| 146,4
| | FeS (к)
| -95,1
| -97,6
| 67,4
| | H (г)
| 217,94
| 203,26
| 114,6
| | H2 (г)
| 0,00
| 0,00
| 130,58
| | HBr (г)
| -35,98
| -53,5
| 198,5
| | HCl (г)
| -92,3
| -95,27
| 186,69
| | HCl (р)
| -166,9
| -131,2
| 56,5
| | HF (г)
| -268,61
| -270,7
| 173,51
| | HI (г)
| 25,94
| 1,3
| 206,3
| | HNO3 (ж)
| -174,3
| -80,3
| 156,6
|
Продолжение табл. 3
| Вещество
|  , кДж/моль , кДж/моль
| 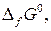 кДж/моль кДж/моль
|  , Дж/(моль∙К) , Дж/(моль∙К)
| | H2O (г)
| -241,82
| -228,61
| 188,7
| | H2O (ж)
| -285,84
| -237,2
| 70,08
| | H2O (к)
| -291,85
| -235,5
| 44,1
| | H2O2 (ж)
| -187,8
| -120,4
| 109,6
| | H2S (г)
| -20,17
| -33,01
| 205,6
| | H2SO4 (ж)
| -811,3
| -690,3
| 156,9
| | H3PO4 (ж)
| -1271,9
| -1147,25
| 200,8
| | Hg (ж)
| 0,00
| 0,00
| 77,4
| | HgO (к)
| -90,8
| -58,3
| 70,3
| | HgCl2 (к)
| -230,1
| -185,8
| 144,35
| | Hg2Cl2 (к)
| -264,85
| -210,7
| 185,8
| | I2 (к)
| 0,00
| 0,00
| 116,73
| | I2 (г)
| 62,24
| 19,4
| 260,58
| | KCl (к)
| -435,9
| -408,3
| 82,7
| | K2O (к)
| -361,5
| -333,5
| 94,0
| | KOH (к)
| -425,8
| -380,2
| 59,41
| | LiOH (к)
| -487,8
| -443,9
| 42,7
| | Li2O (к)
| -598,7
| -562,1
| 37,9
| | Mg (к)
| 0,00
| 0,00
| 32,55
| | MgCl2 (к)
| -641,6
| -592,1
| 89,6
| | MgO (к)
| -601,24
| -569,4
| 26,94
| | Mg(OH)2 (к)
| -924,7
| -833,8
| 63,14
| | Mg(NO3)2 (к)
| -789,6
| -588,4
| 164,0
| | MgCO3 (к)
| -1112,9
| -1029,3
| 65,69
| | MgSO4 (к)
| -1278,2
| -1173,6
| 9163
| | Mn (к)
| 0,00
| 0,00
| 31,76
| | MnO2 (к)
| -519,4
| -464,8
| 53,14
| | MnSO4 (к)
| -1063,7
| -956,0
| 112,1
| | Mo (к)
| 0,00
| 0,00
| 28,6
| | MoO3 (к)
| -754,5
| -677,6
| 78,2
| | N2
| 0,00
| 0,00
| 191,5
| | NH3 (г)
| -46,19
| -16,66
| 192,5
| | N2H4 (ж)
| 50,4
| 149,2
| 121,3
| | NH4OH (р)
| -361,2
| -254,2
| 165,4
| | NH4Cl (к)
| -314,4
| -203,0
| 94,6
| | (NH4)2SO4 (к)
| -1179,3
| -900,3
| 220,3
| | NO (г)
| 90,37
| 86,71
| 210,62
| | NO2 (г)
| 33,5
| 51,8
| 240,45
| | N2O4 (г)
| 9,66
| 98,28
| 304,3
| | Na (к)
| 0,00
| 0,00
| 51,0
|
Продолжение табл. 3
| Вещество
|  , кДж/моль , кДж/моль
| 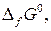 кДж/моль кДж/моль
|  , Дж/(моль∙К) , Дж/(моль∙К)
| | NaCl (к)
| -410,9
| -384,0
| 72,33
| | Na2O (к)
| -415,9
| -376,6
| 72,8
| | NaOH (к)
| -427,8
| -381,1
| 64,18
| | Na2SO4 (к)
| -1384,6
| -1266,8
| 149,4
| | Na2CO3 (к)
| -1130,9
| -1047,7
| 136,0
| | NaNO3 (р)
| -446,2
| -372,4
| 207,0
| | Ni (к)
| 0,00
| 0,00
| 29,86
| | NiO
| -239,7
| -211,7
| 38,0
| | O2 (г)
| 0,00
| 0,00
| 205,04
| | O3 (г)
| 142,3
| 163,4
| 238,8
| | O (г)
| 247,5
| 230,1
| 161,0
| | P (к, белый)
| 0,00
| 0,00
| 41,1
| | P (к, красный)
| -18,4
| -13,8
| 22,8
| | PCl3 (г)
| -306,5
| 286,3
| 311,7
| | PCl5 (г)
| -592,0
| -545,2
| 324,6
| | Pb (к)
| 0,00
| 0,00
| 64,9
| | PbO (к)
| -217,9
| -188,5
| 69,45
| | PbSO4 (к)
| -918,1
| -811,2
| 147,28
| | PbO2 (к)
| -276,6
| -219,0
| 76,44
| | S (к, ромб)
| 0,00
| 0,00
| 31,88
| | SO2 (г)
| -296,9
| -300,4
| 248,1
| | SO3 (г)
| -395,2
| -370,4
| 256,23
| | SO2Сl2 (ж)
| -381,1
| -315,8
| 217,2
| | Si (к)
| 0,00
| 0,00
| 18,7
| SiO2 ( -кварц) -кварц)
| -859,4
| -805,2
| 41,84
| | SiCl4 (г)
| -609,6
| -569,9
| 331,4
| | SiH4 (г)
| -61,9
| -39,3
| 203,8
| | Sn (к, белый)
| 0,00
| 0,00
| 51,55
| | SnO2 (к)
| -580,7
| -418,4
| 52,3
| | Ta (к)
| 0,00
| 0,00
| 41,4
| | Ta2O5 (к)
| -2045,1
| -1922,5
| 143,1
| | Ti (к)
| 0,00
| 0,00
| 30,6
| | TiCl4 (г)
| -758,9
| -714,0
| 353,1
| | TiCl4 (ж)
| -800,0
| -724,0
| 252,7
| | TiO2 (к, рутил)
| -941,0
| -881,6
| 50,2
| | W (к)
| 0,00
| 0,00
| 33,5
| | WO3 (к)
| -840,3
| -763,4
| 83,3
|
Окончание табл. 3
| Вещество
|  , кДж/моль , кДж/моль
| 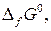 кДж/моль кДж/моль
|  , Дж/(моль∙К) , Дж/(моль∙К)
| | Zn (к)
| 0,00
| 0,00
| 41,59
| | ZnO (к)
| -349,0
| -318,2
| 43,5
| | ZnCl2 (к)
| -415,9
| -369,2
| 108,4
| | ZnS (к)
| -201,0
| -239,8
| 57,7
| | ZnSO4 (к)
| -978,2
| -870,2
| 124,6
| | Zr (к)
| 0,00
| 0,00
| 38,4
| | ZrO2 (к)
| -1762,3
| -1565,2
| 184,1
|
Таблица 4.
|



 кг/с2)
кг/с2)
 101325 Па
1 мм рт. ст. = 133,3 Па
101325 Па
1 мм рт. ст. = 133,3 Па
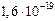 Дж
1 эрг = 10-7
Дж
1 эрг = 10-7
 , кДж/моль
, кДж/моль
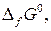 кДж/моль
кДж/моль
 , Дж/(моль ∙К)
, Дж/(моль ∙К)
 -кварц)
-кварц)



