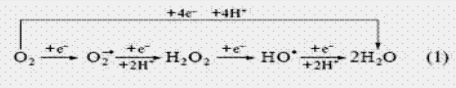Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Информацию, необходимую для восполнения исходного уровня, можно найти в следующей литературе.Содержание книги
Поиск на нашем сайте
1. Тюкавкина Н.А., Бауков Ю.И. Биоорганическая химия. - М.: Медицина, 1991. – С. 213-227, 291-294, 301-304, 313-361. 3.Лекции по биоорганической химии.
Содержание обучения. Содержание обучения должно обеспечивать достижение целей обучения, чему способствует граф логической структуры изучаемой темы (Приложение 1).
Основные теоретические вопросы, позволяющие выполнить целевые виды деятельности:
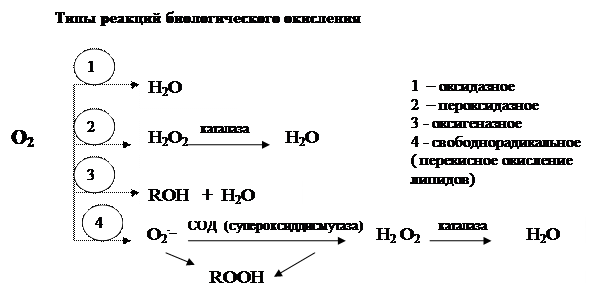
1. Типы реакций биологического окисления (оксидазный, оксигеназный, пероксидазный, свободнорадикальный) и их роль в метаболизме.. 2.Активные формы кислорода (АФК): синглетный кислород, пероксид водорода, гидроксильный радикал, пероксинитрид. Механизмы их образование в организме, причины токсичности. Физиологическая роль АФК. 3. Ферменты и коферменты, участвующие в ОВР (приложение 2). 4. Молекула аденозинтрифосфорной кислоты (АТФ) как основная форма сохранения химической энергии в клетке. Участие АТФ в реакциях энергетического сопряжения. 5. Способы синтеза АТФ в живых организмах (реакции фосфорилирования): субстратное фосфорилирование, фотофосфорилирование, окислительное фосфорилирование. 6. Транспорт АТФ и АДФ через митохондриальные мембраны. Роль митохондриальной креатинкиназы. 7. Источники витамина А и его биологическая роль (приложение 3). 8. Источники витамина Д, образование его активной формы, кальцитриола. 9. Участие витамина Д в метаболизме. 10. Участие витамина Е в метаболизме. 11. Биороль витамина К. 12. Биороль полиненасыщенных ВЖК. 13. Гипо-и гиперфункции жирорастворимых витаминов. Найти материал для освоения этих вопросов можно в одном из следующих источников. Обязательная литература. Губський Ю.Г. Біологічна хімія. - Київ-Тернопіль.: Укрмедкнига, 2000. - С. 411-417. 2. Тестовые задания по биологической химии/ Под ред.Б.Г.Борзенко. - Донецк, 2000. -С.44-73. 3. Лекции по биохимии. 4. Граф логической структуры (Приложение 1,2). 5. Инструкция к практическому занятию. Дополнительная литература 1. Березов Т.Т., Коровкин Б.Ф. Биологическая химия. - М.: Медицина, 1998.-С. 210-219 313-316 2. Березов Т.Т., Коровкин Б.Ф. Биологическая химия. - М.: Медицина, 1990. - С. 138-147 3. Николаев А.Я. Биологическая химия. - М.: Высшая школа, 1998.- С. 161, 167-171, 386-388, 478-480. 4. Марри Р., Греннер Д., Мейес П., Родуэлл В. Биохимия человека. - М.: Мир, 1993. - С.111-139
После изучения вышеперечисленных вопросов для самопроверки усвоения материала по изучаемой теме предлагается решить следующие целевые обучающие задачи. Целевые обучающие задачи. Задача 1.В эксперименте установлено, что окисление субстрата в клетке происходит по оксигеназному пути. Подберите соответствующую характеристику процесса: А. Реакцию катализирует анаэробная дегидрогеназа Б. Способствует включению кислорода в субстрат В. Сопровождается образованием эндогенной воды Г. Сопровождается синтезом АТФ Д. Осуществляется в митохондриях
Задача 2. Одним из методов борьбы с гипоксией является гипербарическая оксигенация. При несоблюдении режима этой процедуры высокая доза кислорода может вызвать острое отравление, даже с появлением “кислородных “ судорог. Активация какой реакции биологического окисления особенно опасна для ткани мозга при длительном вдыхании кислорода под давлением? А. Пероксидазной В. Оксигеназной С. Оксидазной Д. Свободнорадикального окисления Е. Микросомального окисления Задача3.Нарушение функции толстого кишечника вызвало у больного повы- шенное образование токсичного бензола. Какой из нижеуказанных процес- сов участвует в его обезвреживании? А. Свободно-радикальное окисление В. Микросомальное окисление С. Тканевое дыхание D. Окислительное фосфорилирование Е. Окислительное декарбоксилирование Задача 4 При обследовании больного с диагнозом пеллагра обнаружено снижение образование АТФ в миокарде. В чем причина развития гипоэнер- гетического состояния у пациента? А. Ингибирование монооксигеназных реакций В. Гипоксия С. Уменьшение гемоглобина D. Нарушение структуры митохондрий Е. Ингибирование пиридиновых дегидгогеназ Задача 5. Под действием жесткого ультрофиолетового облучения развивается мышечная дистрофия. Какое вещество может препятствовать этому нарушению? А. α-токоферол В. 1,25-диоксихолекальциферол С. Ретинол Д. Витамин Д3 Е. Филлохтнон Задача 6 У спасателя, работающего в радиационном очаге, начались некрозо-дистрофические процессы в печени. Что ему следует назначить в комплексе лечения? А. Ретинол В. Аскорбиновую кислоту С. Витамин К D. Лецитин Е. a-токоферол
Задача 7 Витамин D регулирует минеральный обмен в организме. Для усвоения каких минеральных элементов он необходим? А. Натрия В. Калия C. Кальция D. Железа Е. Кобальта
Задача 8 Сложный процесс образования в организме кальцитриола проходит через несколько стадий. Для какой из них требуется ультрафиолетовое облучение? А. 7-дегидрохолестерин® холекальциферол В. Холестерин ® холевая кислота С. Холекальциферол ® 25-гидроксихолекальциферол D. 25(ОН)-Д3 ® 1,25(ОН)2 -Д3) Е. Сквален ® ланостерин
Правильность решения проверьте, сопоставив их с эталонами ответов. Эталоны ответов к решению целевых обучающих задач: 2-Д; 3-В; 4-Е; 5-А; 6 – Е
Задания для самостоятельной работы к занятию «Исследование типов биологического окисления»
2. Выписать в общем виде уравнения реакций катализируемых пиридин- и флавинзависимыми дегидрогеназами.
SH2 + НАД+→ SH2 + ФАД→
Привести активные структуры в молекулах НАД+ и ФАД, которые являются акцепторами протонов и электронов в дегидрогеназных реакциях.
Краткие методические рекомендации к проведению заняття. На занятии проводится тестовый контроль исходного уровня знаний студентов и его коррекция. Проверяется выполнение домашнего задания. Затем студенты приступают к выполнению лабораторной работы, используя при этом инструкцию. После выполнения лабораторной работы необходимо оформить протокол,сделать выводы к работе, которые проверяет и контролирует преподаватель.Проводится итоговый тестовый контроль по теме, подводятся итоги работы.
Инструкция к практическому занятию «Исследование типов биологического окисления». РАБОТА №1: Открытие альдегиддегидрогеназы в молоке. Принцип работы: Фермент вырабатывается микроорганизмами, попадающими в молоко извне. По химической природе он относится к флавопротеинам, способным окислять альдегиды, в частности формальдегид. При добавлении к некипяченому молоку формальдегида метиленовой сини альдегиддегидрогеназа окисляет формальдегид в муравьиную кислоту, а освобождающийся при этом водород переносится на метиленовую синь, востанавливая ее в бесцветное соединение. Материальное обеспечение: кипяченое молоко, не кипяченое молоко, 0,04% раствор формальдегида, 0,01% раствор метиленовой сини, пробирки, пипетки. Ход работы: В одну пробирку вносять 15 капель кипяченого молока, а в другую – 15 капель не кипяченого. В каждую пробирку вносят по капле 0,4% раствора формальдегида и по капле 0,01% раствора метиленовой сини. Пробирки встряхивают и закрывают пробками, чтобы создать относительные анаэробныеусловия. Пробирки помещают в термостат при 37º С и отмечают через пять минут постепенное обесцвечивание метиленовой сини. ВЫВОДЫ:
РАБОТА №2 Обнаружение каталазы крови Принцип работы: Фермент каталаза относится к классу оксидоредуктаз. Этот фермент содержится во всех тканях и жидкостях организма, но особенно много его в строме эритроцитов и печени. В процессе окисления некоторых веществ образуется перекись водорода, ядовитая для организма, которая может в нем накапливаться. Биологическая роль каталазы заключается в разложении вредной для организма перекиси водорода на молекулярный кислород и воду:
каталаза
Фермент каталаза содержит гем. Материальное обеспечение: 3% раствор перекиси водорода, кровь. Ход работы: В пробирку вносять 10-15 капель 3% Н2О2 и 1 каплю крови. Отмечают выделение пузырьков кислорода. Подпись преподавателя:
Приложение 1.
Г р а ф логической структуры к теме: «Исследование типов биологического окисления».
Механизм антиоксидантного действия жирорастворимых витаминов
Приложение 2
ВЗАИМОСВЯЗЬ ОБМЕНА ВЕЩЕСТВ И ЭНЕРГИИ. ЦИКЛ АТР-АDР. Пищевые вещества
Метаболиты 4 Распад структурно- Катаболизм Анаболизм функциональных 2 компонентов 3 5 7 Энергия 6 Рис.1. Общая схема обмена веществ и энергии. 1 - пищеварение; 2,4- катаболизм; 3- анаболизм; 5- экзергонические реакции; 6,7- эндергонические реакции. 1. Обмен веществ включает три этапа: 1)поступление веществ в организм; 2) метаболизм, или промежуточный обмен; 3) выделение конечных продуктов обмена
1.1. Реакции катаболизма сопровождаются выделением энергии (экзергонические реакции), а её использование связано с реакциями анаболизма и физиологической активностью организма (эндергонические реакции).
1.2. Центральную роль энергетическом обмене выполняет АТР: а) в макроэргических связях АТР аккумулируется энергия, выделяемая в процессе катаболизма; б) энергия АТРиспользуется в реакциях анаболизма и обеспечивает различные виды работы в организме.
2. Процессы катаболизма в клетках животных сопровождаются потреблением кислорода, который необходим для реакций окисления. Ферменты, катализирующие окислительно-восстановительные реакции, называются оксидоредуктазами. Их подразделяют на 4 группы: 2.1. Дегидрогеназы катализируют перенос водорода от субстрата (S) на кофермент акцептор (А). SН2 + А → S + АН2 есть: две основные группы дегидрогеназ, которые различаются по используемым коферментам. 2.1.1. Пиридинзавасимые дегидрогеназы (кофермент НАД+ или НАДФ+). Никотинамид синтезируется в организме из триптофана или поступает с пищей (витамин РР). 2.1.2. Флавиновые дегидрогеназы (кофермент ФАД или ФМН). ФМН и ФАД образуются в организме из рибофлавина (витамин В2). 2.2. Оксидазы – катализируют перенос электронов от S на молекулярный кислород SН2 +1/2О2 → S + Н2О SН2 +О2 → S + Н2О2. 2.3. Оксигеназы катализирует включение кислорода в молекулу органического субстрата. Их подразделяют на две группы, в зависимости от: -диоксигеназы, количество атомов кислорода, которое взаимодействует с S: S + О2→SО2 - монооксигеназы: S -Н + О2 + АН2 → SОН + А + Н2 О - гидропероксидазы (пероксидазы и каталазы) катализируют разрушение перекиси водорода. 2Н2О2 → 2Н2О +О2. 2.4 Свободнорадикальное окисление Окисление субстратов свободными радикал-анионами: супероксидом О2· -, Н2О2, и наиболее активным радикалом – гидроксил анионом ОН· Пути образования свободных радикалов; - Реакции восстановления кислорода до Н2 О в дыхательной цепи - основной: источник свободных радикалов
- Некоторые метаболические процессы (микросомальное окисление, распад пуриеовых нуклеотидов, фагоцитоз идр.) Свободные радикалы вызывают образование органических гидропероксидов (ROOH) ДНК, белков и липидов.
Приложение 3
Биологическая роль жирорастворимых витаминов В состав жирорастворимых витаминов входят углеводородные изопреноидные радикалы, потому они являются компонентами биомембран, в составе которых выполняют специфические биофункции, в частности, мощных биоантиоксидантов (Е, А, К). В отличии от водорастворимых витаминов избыточное поступление витаминов А, Д, К вызывает гипервитаминозы благодаря их кумуляции в органах.
Витамин К относится к группе хинонов. Биологическая роль заключается в его влиянии на систему свертывания крови, т.к. он участвует в реакции карбоксилирования глутаминовой кислоты белковых факторов свертывания крови ІІ, УІІ, ІХ, Х в процессе их синтеза в печени.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2021-04-12; просмотров: 210; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.169 (0.011 с.) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

 2Н2О2 2Н2О + О2
2Н2О2 2Н2О + О2








 1
1