
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Проба с цетилтриметиламмониумбромидомСодержание книги
Поиск на нашем сайте
Принцип метода Гликозаминогликаны при взаимодействии с цетилтриметиламмониумбромидом формируют преципитат, интенсивность образования и осаждения которого зависит от их содержания в исследуемой пробе мочи. Ход работы К 5,0 мл свежей мочи прибавляют 1,0 мл 2,5 % раствора цетилтриметиламмониумбромида, инкубируют в течение 30 мин, наблюдая за образованием преципитата. Пробу ставят при комнатной температуре. Оценка результатов Пробу оценивают по шкале от 0 до 4+ в соответствии с интенсивностью образования преципитата и характером осадка. Проба даёт до 40 % ложноположительных результатов. Проба с толуидиновым синим Принцип метода Гликозамингликаны, при появлении их в моче, способны взаимодействовать с красителем толуидиновым синим, образуя соединение пурпурной окраски. Ход работы Одну каплю мочи наносят на бумагу, высушивают при комнатной температуре. Бумагу помещают в раствор толуидинового синего на 1 мин, затем обесцвечивают фон, погружая лист в 10 % раствор уксусной кислоты. Контроль (раствор хондроитинсульфата А (2 мг/мл) или моча больного мукополисахаридозом) обрабатывают параллельно опытной пробе. Оценка результатов Реакция положительна при развитии пурпурной окраски и может свидетельствовать о наличии гликозаминогликанов в моче. Клинико-диагностическое значение Проба с ЦТАБ положительна при мукополисахаридозах (особенно выражена у детей с синдромами Гунтера, Гурлера), синдроме Марфана, множественных экзостозах, ревматоидном артрите, кретинизме, карциноматозе. Проба с толуидиновым синим чувствительнее, чем проба с ЦТАБ, поэтому её целесообразно использовать для анализа всех «положительных» образцов, образующих с ЦТАБ осаждающийся преципитат. Оформление работы Указывают принципы методов, регистрируют результаты, сравнивают их и делают вывод о наличии/отсутствии патологических отклонений. Лабораторная работа 3. Актуальность Гликопротеины межклеточного матрикса имеют ковалентно присоединённые углеводные цепи гораздо меньшей длины, чем у протеогликанов. Моносахаридные остатки в составе олигосахаридных фрагментов гликопротеинов относятся к гексозам, в том числе присутствуют дезокси- и аминогексозы. Из гликопротеинов соединительной ткани выделены N‑ацетилгалактозамин и N‑ацетилглюкозамин. Во время синтеза N‑связанных гликопротеинов обычно обнаруживают глюкозу, но в зрелых гликопротеинах она отсутствует. Характерным сахаром N‑связанных гликопротеинов является манноза. В концевых отделах гликопротеинов встречается фукоза, но наиболее частым терминальным сахаром считают N‑ацетилнейраминовую кислоту, субтерминально к ней нередко расположена галактоза, которую также выделяют из состава кóрового олигосахарида протеогликанов. Гексозы важны для проявления структурных, соединительных, защитных, иммунных, регуляторных свойств гликопротеинов. Принцип метода Гликопротеины благодаря содержащимся в них гексозам проявляют способность осаждаться из сыворотки крови при действии 96% этанола. Освобождённые в результате последующего гидролиза гексозы взаимодействуют с орциновым реактивом, окрашивая раствор в жёлто-оранжевый цвет, интенсивность которого пропорциональна содержанию гексоз. Реактивы 1) Этанол 96°, 2) 0,1 М раствор NaOH, 3) орциновый реактив, 4) стандартный раствор гексоз (1 г/л). Материал для исследования Сыворотка крови. Ход работы Готовят три пробы: опытную, стандартную и контрольную. Опытная проба ‑ в центрифужную пробирку помещают 0,1 мл сыворотки крови и 2,5 мл этанола, перемешивают путем встряхивания, центрифугируют 15 мин при 3000 об/мин. Надосадочную жидкость сливают, пробирку осторожно опрокидывают на 30‑60 сек на фильтровальную бумагу. Оставшийся в пробирке белковый осадок растворяют, добавляя 0,5 мл 0,1 М раствора NaOH. Затем осторожно(!) доливают 4,5 мл орцинового реактива и тщательно перемешивают стеклянной палочкой. Стандартную пробу готовят, добавляя к 0,1 мл стандартного раствора (1 г/л) гексоз 0,4 мл 0,1 М раствора NaOH и 4,5 мл орцинового реактива. Контрольную пробу готовят путём добавления к 0,5 мл 0,1 М раствора NaOH 4,5 мл орцинового реактива. Все пробирки помещают в кипящую водяную баню на 15 мин, охлаждают под проточной водой. Опыт и стандарт фотометрируют против контроля в диапазоне длин волн 500‑560 нм (зелёный светофильтр) в кювете 10 мм. Расчёт Для расчёта результатов используют формулу:
где: СОП ‑ концентрация в крови гексоз гликопротеинов (г/л), ССТ ‑ концентрация гексоз в стандартном растворе (г/л), ЕОП и ЕСТ ‑ экстинкции опытной и стандартной проб. Нормальные величины Концентрация гексоз гликопротеинов в сыворотке крови ‑ 1,05‑1,15 г/л. Клинико-диагностическое значение работы Традиционно полагают, что увеличение уровня гликопротеинов (гексоз гликопротеинов) в крови отражает лишь процессы деструкции соединительных тканей при патологических процессах воспалительного и иного характера. Однако, как выяснилось, в ответ на повреждения печень усиленно синтезирует гликопротеины, многие из которых участвуют в репарации. Обладая биологически активными группами (например, сиаловыми кислотами, способными инактивировать ряд биологических агентов), гликопротеины проявляют защитные функции, направленные на ограничение патологического процесса (компенсаторная реакция). Оформление работы Указывают принцип метода, фиксируют показания прибора, производят расчёты, сравнивают нормальные величины с полученными данными, делают вывод о наличии/отсутствии патологических отклонений. Лабораторная работа 4. Сиаловые кислоты или N-ацетилнейраминовые кислоты играют важную роль в качестве строительных блоков гетерополисахаридов, входящих в состав гликопротеинов и гликолипидов. Сиаловые кислоты обычно являются концевыми остатками полисахаридных цепей гликопротеинов и гликолипидов. Гликолипиды встречаются в мембранах, главным образом, в плазматической. Гликопротеины содержатся в мембранах, цитозоле, жидкостях организма. Сиаловая кислота синтезируется из фосфоенолпирувата и N‑ацетилманнозамина‑6‑фосфата. В сыворотке крови определяют только связанные сиаловые кислоты. Принцип При добавлении трихлоруксусной кислоты к сыворотке крови идет мягкий гидролиз с отщеплением сиаловых кислот от сиалогликопротеинов. Сиаловые кислоты при нагревании с уксусно-сернокислым реактивом дают буровато-розовую окраску, интенсивность которой пропорциональна их концентрации. Материал для исследования Сыворотка крови. Реактивы 1) 10 % раствор трихлоруксусной кислоты (ТХУ), 2) уксусно-сернокислый реактив (реактив Гесса), 3) стандартный раствор сиаловых кислот (1 г/л). Проведение анализа Опытная проба. Для выделения сиаловых кислот в центрифужную пробирку вносят 1 мл сыворотки крови, 1 мл раствора ТХУ, перемешивают, закрывают фольгой, помещают точно на 5 мин в кипящую водяную баню для гидролиза гликопротеинов, охлаждают, центрифугируют 3‑5 мин при 1500 об/мин (или фильтруют через смоченный водой бумажный фильтр). Для проведения реакции на сиаловые кислоты переносят 0,4 мл надосадочной жидкости (фильтрата) в чистую пробирку, добавляют 5 мл реактива Гесса, закрывают фольгой, кипятят 15‑20 мин (появляется буровато-розовая окраска), охлаждают. Стандартная проба. Берут 0,4 мл стандартного раствора сиаловых кислот, обрабатывают с 5 мл реактива Гесса аналогично опыту. Интенсивность окраски обеих проб измеряют на колориметре против реактива Гесса, длина волны 540 нм (зелёный светофильтр), кювета 1 см. Расчёт При отсутствии стандартного раствора содержание сиаловых кислот в сыворотке крови можно выражать в условных единицах, для чего полученную величину экстинкции опытной пробы умножают на 1000. При наличии стандартного раствора расчёт результатов проводят по формуле:
где: СОП — концентрация в крови сиаловых кислот гликопротеинов (г/л), ССТ — концентрация сиаловых кислот в стандартном растворе (г/л), ЕОП и ЕСТ — экстинкции опытной и стандартной пробы. Нормальные величины Сыворотка крови 135‑200 усл.единиц или 2,0‑2,36 ммоль/л или 0,62‑0,73 г/л Практическое значение Концентрация сиаловых кислот в крови повышается при воспалениях (эндокардит, остеомиелит), туберкулезе, лейкемии, нефрозе, лимфогранулематозе, поражении гепатоцитов, деструкции соединительной ткани (коллагенозы и др.), резко растет при опухоли головного мозга, инфаркте миокарда. Снижение уровня сиаловых кислот ‑ при пернициозной анемии, гемохроматозе, болезни Вильсона и дегенеративных процессах в ЦНС. Оформление работы Указывают принцип метода, записывают результаты измереня, производят расчёт, сравнивают нормальные величины с полученными данными, делают вывод о наличии или отсутствии патологических отклонений. Вопросы для самоконтроля 1) Типы соединительных тканей, их морфофункциональные особенности. Межклеточный матрикс, химический состав, роль в организме. 2) Фибриллярные белки. Специфика аминокислотного состава и структуры коллагена, синтез, посттрансляционная модификация и ферменты, фолдинг, созревание, распад. Роль аскорбата в синтезе. Типы и группы коллагена, функции, роль в минерализации. 3) Особенности строения и функций эластина, эластин и коллаген. Адгезивные и антиадгезивные белки внеклеточного матрикса, строение и функции, роль в межклеточных взаимодействиях. Сахара гликопротеинов (гексозы и сиаловые кислоты). 4) Протеогликаны матрикса, классы, роль, синтез и распад. Строение углеводного кора, гликозаминогликанов. Сборка надмолекулярных комплексов. 5) Коллагеновые болезни, мукополисахаридозы и другие патологии соединительной ткани. Матриксные металлопротеиназы, гликозидазы. 6) Пульпа – вариант специализированной соединительной ткани, состав, свойства, функции. ТЕМА 10.2. Актуальность Костная ткань и большинство тканей зуба относятся к плотной оформленной соединительной ткани. Альвеолярный отросток челюстной кости ‑ часть скелета и подчиняется метаболическим закономерностям костной ткани. Особое место среди минерализованных тканей занимает эмаль в связи со спецификой происхождения, состава и функций. Межклеточное вещество специализированных видов соединительной ткани определяет их основные свойства. Важную функцию выполняют кальций-связывающие и адгезивные белки. Расположение нитей коллагена в матриксе твердых тканей обеспечивает выполнение главных функций этого белка ‑ придавать тканям прочность на разрыв и обеспечивать минерализацию костей, зубного дентина, цемента и периодонтальной связки. Помимо органических веществ твердые ткани характеризуются высоким содержанием минералов, среди которых преобладают фосфорнокислые соли кальция в виде апатитов. Образование и распад минеральной фазы твёрдых тканей организма тесно связаны с индивидуальным обменом кальция, фосфора, других макро- и микроэлементов. Наиболее значимым микроэлементом, повышающим устойчивость апатитов, является фтор. Зубы ‑ специализированный орган, где прямо соприкасаются закономерности «поведения» органических и минеральных веществ. Понимание взаимоотношений между обменом органических компонентов и минералов в тканях зуба далеко от совершенства, на что указывают нерешённые проблемы борьбы с кариесом, воспалительными и иными заболеваниями полости рта. Цель 1. Сформировать представление о химическом составе костной ткани и тканей зуба, о зависимости характеристик кристаллов гидроксиапатита от состояния минерального обмена в организме. 2. Освоить методы выявления основных неорганических веществ и белка в костной и зубных тканях, оценки концентрации кальция и фосфатов в плазме крови и моче, фторидов в воде. 3. Оценить проницаемость эмали зуба, акцентировать внимание на роли фтора в поддержании здоровья эмали зубов. Вопросы для самоподготовки 1) Происхождение, состав, построение, функциональная организация костной ткани. Сходство и различия кости, соединительной и хрящевой тканей. 2) Комплексы протеогликанов матрикса кости, фибриллярные белки и гликопротеины различной природы. Коллагены и специфичные для костной ткани матриксные белки, посттрансляционная модификация, назначение, функции. 3) Механизмы моделирования и ремоделирования кости, роль ферментов и простагландинов, особенности процессов в альвеолярном отростке челюстной кости. Влияние пирофосфата и бифосфонатов на резорбцию кости. 4) Регуляция метаболизма костной и зубных тканей с участием витаминов (А, С, К, D), гормонов (паратгормон, кальцитонин, глюкокортикоиды, половые, тиреоидные и др.), белковых факторов (морфогены, митогены, факторы хемотаксиса и хемоаттракции, кейлоны). 5) Рахит (ранние и поздние проявления). Остеомаляция. Остеопороз и его виды. Причины появления, сходство и различия заболеваний. 6) Происхождение, функциональная организация и взаимосвязи тканей зуба. 7) Сходство и различия кости и зубного цемента. Виды цемента, роль, химический состав, специфические белки, возможности регенерации. 8) Химический состав и функции дентина. Виды дентина (плащевой, интертубулярный и перитубулярный), происхождение, функции, особенности минерализации. Сходство и различия первичного, вторичного и третичного дентина. Дентинные канальцы. Дентинная жидкость: состав, происхождение, значение для тканей зуба. 9) Химический состав зубной эмали. Эмбриональная эмаль: синтез, созревание, значение наносфер, участие белков и ферментов в разные фазы образования эмали. Белки зрелой эмали. Факторы, влияющие на устойчивость и проницаемость эмали. Эмалевая жидкость. 10) Коллаген, неколлагеновые белки кости и зуба, роль в минерализации. Роль органических молекул (фосфолипидов, цитрата и др.) в накоплении Са, появлении первичных кристаллов в ходе минерализации. Щелочная фосфатаза. 11) Теории минерализации кости и твёрдых тканей зуба. Гомогенная и гетерогенная нуклеация. Роль клеток в накоплении минералов и минерализации, матриксные пузырьки. Факторы, влияющие на процессы кристаллизации. 12) Кальций и фосфат межклеточного матрикса, функции, обмен. Фосфаты кальция ‑ основа минеральной фазы (витлокит, монетит, брушит; ди-, три-, тетракальцийфосфаты, октакальцийфосфат, апатиты). Магний в организме, участие в минеральной фазе (струвит, невберит, апатит) твёрдых тканей. 13) Минеральные компоненты аморфной фазы твердых тканей, этапы преобразования в ГАП. Типы кристаллов. Сравнение кристаллов ГАП кости и тканей зуба. Механизм формирования кристаллов ГАП в эмали. 14) Условия образования вакансий, этапы изоморфного замещения элементов кристаллической решетки, роль в модификации апатитов. Механизмы и реакции поступления, последствия включения макро- и микроэлементов в кристаллы ГАП кости и твёрдых тканей зуба. Рахитоподобные состояния, «уровская болезнь» (Кашина-Бека) и другие патологии. 15) Фтор, роль в процессах жизнедеятельности. Источники фтора и потребность в нём. Влияние фтора на ткани зуба. Гипофтороз, флюороз зубов. 16) Поверхностные образования на зубах (кутикула, пелликула, зубной налёт): состав, механизмы образования. Роль микрофлоры в синтезе стромы налёта (декстраны, леваны, маннаны и др.), углеводно-фосфорный обмен в бляшке. Минерализации зубной бляшки, разнообразие минералов зубного камня. 17) Кариес. Причины, механизмы развития, профилактика. Особенности биохимических нарушений в разных тканях зуба. 18) Состояние зубов и питание: углеводы, белки, витамины и микроэлементы. Лабораторная работа 1. Костная ткань и ткани зуба – это варианты плотной оформленной соединительной ткани. Межклеточный матрикс минерализованных тканей содержит белки и сульфатированные гликозаминогликаны. Главный белок кости, дентина и цемента зуба – коллаген, также представлены адгезивные и антиадгезивные гликопротеины и Са-связывающие белки. Зубная эмаль содержит специфичные белки, нерастворимые в ЭДТА и НСl ‑ производные эмбриональных энамелинов и амелобластинов. Для поддержания структурно-функционального статуса кости и зуба важна минеральная фаза, распределенная в органической в виде тончайших включений. Их отличает высокая концентрация минералов (фосфаты Са и Mg, карбонаты Са, фторид Са и др.), в основном это кристаллы ГАП. Материал для исследования 1) Минерализаты кости, тканей зуба (готовят лаборанты: 5 г порошка кость/зуб инкубируют с 25 мл 0,5 % раствора Н2SО4 в течение суток, отфильтровывают), 2) гидролизаты кости и тканей зуба (готовят студенты на занятии). Реактивы 1) Молибденовый реактив, 2) 10 % раствор уксусной кислоты, 3) насыщенный раствор щавелевокислого аммония, 4) 10 % раствор НСl, 5) 5 % раствор ВаСl2, 6) 10 % раствор NaOН, 7) 1‑2% раствор СuSО4.
|
||||
|
Последнее изменение этой страницы: 2021-04-05; просмотров: 57; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.222.67.8 (0.01 с.) |

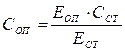 ,
,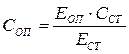 ,
,


