
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Нервная и мышечная ткани. Медиаторы
14. Разнообразие нервной и мышечной ткани. Локализация и функции, взаимодействие. Организация нервно-мышечной передачи, регуляция. 15. Значение синапса в разнообразии рецепторного аппарата клетки. Строение и функционирование синапса, роль Са2+, постсинаптической мембраны, ферментов. 16. Виды медиаторов нервной ткани, их роль. Аминокислоты – медиаторы, аминокислоты (тирозин, глутамат, триптофан и др.) в реакциях образования и инактивации медиаторов. Значение ГАМК-шунта ЦТК. 17. Механизмы действия медиаторов нервной ткани (норадреналин, ГАМК, ацетилхолин, дофамин), рецепторы постсинаптических мембран, роль Ca2+, ферментов, биологические эффекты. Медиаторы возбуждения и торможения. Модуляторы. Малые регуляторные пептиды мозга. 18. Нейропептиды, синтез и рецепция, роль в нервной ткани и организме, участие в болевых реакциях. Нервная ткань зуба, ноцицепторы челюстно-лицевой области, механизмы и биохимия зубной боли. Химизм боли после мышечной нагрузки. 19. Обмен углеводов и энергетика в нервной и мышечной ткани, роль глюкозы и О2, энергетические субстраты, значение гликолиза и глюконеогенеза, ЦТК и окислительного фосфорилирования, гипогликемии и гипоксии. АТФазы. 20. Липиды нервной ткани. Строение и функции миелина, роль липидного и белкового компонента, миелиновые болезни. Фосфор нервной ткани. Специфические белки. Прионы и болезни. Болезнь Альцгеймера, причины и последствия. 21. Сократительные, вспомогательные и регуляторные белки мышц, их роль. Механизм сокращения–расслабления, источники АТФ и потребление О2. Креатинфосфат. Патологии мышечной ткани, клиническая диагностика. 22. Особенности сердечной и гладкомышечной ткани. Жирные кислоты и миокард. Диагностика повреждений миокарда. Гормональная регуляция 23. Иерархия регуляторных систем организма (роль ЦНС, гипоталамуса, гипофиза). Место гормонов в регуляции метаболизма и функций органов. Механизм обратной отрицательной связи. Общие биологические признаки гормонов, классификации (по химическому строению, биологическим функциям, принадлежности к эндокринным железам). 24. Классификация гормонов по химическому строению, по биологическим функциям, по принадлежности к эндокринным железам. Роль либеринов, статинов, тропных гормонов. Обратная отрицательная связь в регуляции синтеза и действия гормонов.
25. Соматотропный гормон: химическая природа, место синтеза, органы-мишени, локализация рецепторов и механизм действия, влияние на обмен веществ. Регуляция синтеза и секреции гормона, состояния, связанные с нарушением действия гормона. 26. Характеристика антидиуретического гормона (вазопрессин): химическая природа, место синтеза, органы‑мишени, локализация рецепторов и механизм действия, влияние на обмен веществ и воды. Регуляция синтеза и секреции гормона. Состояния, обусловленные нарушением действия гормона. 27. Характеристика окситоцина: химическая природа, место синтеза, регуляция синтеза и секреции, органы‑мишени, локализация рецепторов и механизм действия, эффекты. 28. Характеристика паратгормона и кальцитонина: химическая природа, место синтеза, регуляция синтеза и секреции, органы‑мишени, локализация рецепторов и механизм действия, влияние на обмен кальция, фосфатов, витамина D3. Взаимодействие этих гормонов с гормонально активными формами витамина D3 в обмене кальция и фосфатов. 29. Гормоны поджелудочной железы глюкагон и инсулин: химическая природа, место синтеза, регуляция синтеза и секреции, органы‑мишени, локализация и механизм действия рецепторов, влияние на обмен углеводов, белков, липидов (ферменты, регулируемые гормоном). Состояния, обусловленные отсутствием или избытком действия гормона. 30. Современные представления о механизмах развития инсулинзависимого сахарного диабета. Важнейшие изменения гормонального статуса и обмена веществ при сахарном диабете, биохимические механизмы развития осложнений сахарного диабета и диабетической комы. 31. Характеристика тиреотропного гормона: химическая природа, место синтеза, регуляция синтеза и секреции, органы‑мишени, локализация рецепторов и механизм действия, эффекты. 32. Гормоны щитовидной железы тироксин и трийодтиронин: химическая природа, место синтеза, регуляция синтеза и секреции, органы‑мишени, локализация рецепторов и механизм действия, влияние на обмен углеводов, белков, липидов. Состояния, обусловленные отсутствием или избытком действия гормона.
33. Адреналин: химическая природа, место и химизм синтеза, органы‑мишени, локализация рецепторов и механизм действия, влияние на обмен углеводов, белков, липидов (ферменты, регулируемые гормоном). Регуляция синтеза и секреции гормона. Состояния, обусловленные нарушением действия гормона. Участие адреналина в адаптивных реакциях организма при стрессе. 34. Характеристика адренокортикотропного гормона: химическая природа, место и принципы синтеза, регуляция синтеза и секреции, органы‑мишени, локализация рецепторов и механизм действия, влияние на обмен веществ. Состояния, обусловленные отсутствием или избытком действия гормона. 35. Глюкокортикоиды: химическая природа, место и этапы синтеза, регуляция синтеза и секреции, органы‑мишени, локализация рецепторов и механизм действия, влияние на обмен углеводов, белков, липидов (ферменты, регулируемые гормоном). Состояния, обусловленные отсутствием или избытком действия гормона. Причины использования глюкокортикоидов в качестве противовоспалительных и противоаллергических лекарственных средств. Участие глюкокортикоидов в адаптивных реакциях организма при стрессе. 36. Минералокортикоиды: их химическая природа, место и этапы синтеза, регуляция синтеза и секреции, органы‑мишени, локализация рецепторов и механизм действия, влияние на обмен электролитов и воды. Взаимосвязь с вазопрессином, ренин-ангиотензин-альдостероновая система. 37. Лактотропный гормон: химическая природа, место и этапы синтеза, регуляция синтеза и секреции, органы‑мишени, локализация рецепторов и механизм действия, влияние на обмен веществ. 38. Характеристика гонадотропных гормонов: фолликулостимулирующий и лютеинизирующий гормоны: химическая природа, место и этапы синтеза, органы‑мишени, локализация рецепторов и механизм действия, влияние на женский месячный цикл. Регуляция синтеза и секреции гормонов. 39. Андрогены и эстрогены: химическая природа, место и этапы синтеза, регуляция синтеза и секреции, органы‑мишени, локализация рецепторов и механизм действия, влияние на обмен углеводов, белков, липидов, воздействие на костную ткань. Использование аналогов андрогенов и эстрогенов в качестве лекарственных средств. Практическая часть 1. Определение активности холинэстеразы в сыворотке крови. 2. Определение содержания АТФ, креатинфосфата в мышцах и нервной ткани. 3. Качественные реакции на компоненты тироксина, адреналина, инсулина.
Раздел 10. ТЕМА 10.1. Актуальность Основной тип тканей, на которые простираются законы стоматологии, ‑ это соединительные ткани. Они широко распространены в организме, отличаются преобладанием межклеточного вещества (матрикса) над клеточными элементами и выполняют целый ряд важнейших функций, с течением жизни претерпевают возрастные изменения. С соединительными тканями связано развитие процессов воспаления, метастазирования, деструкции с последующей репарацией и др. Знание химического состава соединительных тканей и понимание характерных метаболических процессов лежат в основе эффективной профилактики и лечения заболеваний стоматологического профиля.
Межклеточный матрикс соединительной ткани представлен комплексами белков и углеводов: гликопротеинов (коллагена, эластина, фибронектина и др.) и протеогликанов (больших, малых и мембраносвязанных). В отличие от гликопротеинов, содержащих менее 10 % углеводов, в протеогликанах более 95 % полисахаридов гликозаминогликановой природы. Благодаря высокой гидрофильности и свободе выбора конформации гликозаминогликаны занимают большие объёмы, образуя гели при довольно низких концентрациях самого полисахарида, что создаёт тургор тканей. Исследование гликопротеинов, протеогликанов, гликановых компонентов используют в диагностике заболеваний. При патологии матрикса соединительной ткани клиническое значение имеют пробы на гликозаминогликаны в моче. Деструкция матрикса сопровождается ростом количества сиаловых кислот и гексоз гликопротеинов в сыворотке крови. Сиаловые кислоты ‑ концевые компоненты углеводной части гликопротеинов, участвуют в инактивации ряда патогенов. При распаде коллагеновых волокон под действием коллагеназ и других металлопротеиназ образуются гликозиды гидроксилизина, свободный гидроксипроли, пиридинолин и возрастает их экскреция с мочой. Цель 1) Сформировать представление о многообразии форм соединительной ткани и их молекулярном составе для понимания механизмов возникновения и развития заболеваний, разработки мер профилактики и методов лечения. 2) Оценить метаболизм компонентов матрикса соединительной ткани путем определения свободного гидроксипролина и компонентов гликозаминогликанов в моче, гексоз и сиаловых кислот гликопротеинов в сыворотке крови. Вопросы для самоподготовки 1) Составные компоненты и типы соединительной ткани. 2) Коллаген. Аминокислотный состав, особенности пространственной структуры, стабилизирующие связи. Изоколлагены. Основные типы коллагена, их роль в организме. 3) Внутри- и внеклеточные этапы синтеза и созревания коллагена, поперечные сшивки, ферменты. Значение структурной организации волокон коллагена для процессов минерализации. 4) Катаболизм коллагена. Маркёры синтеза и распада коллагена. 5) Эластин. Особенности первичной структуры и пространственного строения. Роль в организме. Образование и организация поперечных сшивок эластина. Сходство и различия коллагена и эластина.
6) Адгезивные и антиадгезивные белки внеклеточного матрикса и их функции. Семейства фибронектина, ламинина и др. Состав сахаров углеводного компонента гликопротеинов, строение сиаловых кислот: нейраминовой и др. 7) Гликозаминогликаны: семейства, строение основных представителей, принципы синтеза из глюкозы, локализация и роль в организме. Строение сахаров углеводного кора протеогликанов. 8) Белковоуглеводные комплексы матрикса: принципы классификации, биологическая роль, механизмы синтеза и распада, роль долихола, кор и кóровые белки. Образование О- и N-гликозидных связей протеогликанов. Сборка надмолекулярных протеогликановых комплексов. 9) Болезни соединительной ткани (коллагенозы, мукополисахаридозы и др.). 10) Пульпа зуба как вариант соединительной ткани, особенности строения, органические и неорганические компоненты, основные характеристики. 11) Функции пульпы и её значение для метаболизма тканей зуба. Самостоятельная работа 1. Нарисовать схему надмолекулярного агрегата протеогликанов. 2. Изобразить строение линейного и разветвлённого кóра протеогликанов. 3. Изобразить узлы О‑гликозидной и N‑гликозидной связи углеводного компонента с кóровыми белками протеогликанов соединительной ткани. 4. Дополнить схему углеводно-энергетического обмена (см. темы 3.1, 4.1, 4.2, 9.1) реакциями глюкуронатного пути образования ГАГ из глюкозы в клетках соединительной ткани («путь уроновых кислот»), показать связь с гликогеногенезом и пентозофосфатным циклом. На схеме указать причину отсутствия синтеза аскорбата в организме человека. Лабораторная работа 1. Актуальность Строение полипептидных цепей коллагена уникально: каждую третью позицию на уровне первичной структуры занимает глицин. В регулярно повторяющемся трипептиде ГЛИ-X-Y положения X и Y чаще всего занимают пролин и 4‑гидроксипролин, некоторые формы коллагена имеют ограниченное количество 3‑гидроксипролина. Пирролидиновые кольца пролина обеспечивают стабилизацию α‑спирали коллагена. Гидроксилирование пролина осуществляют пролил-гидроксилазы в ходе посттрансляционной модификации коллагена, коферментами являются ионы железа (II) и аскорбиновая кислота. Коллагеназы, разрушая трёхцепочечную структуру коллагена, высвобождают пролин и гидроксипролин. Свободный пролин в организме не гидроксилируется. Свободный гидроксипролин не способен вновь встраиваться в коллаген, что позволяет использовать концентрацию этого метаболита в крови и моче в качестве индикатора распада коллагеновых волокон. Недогидроксилирование пролина является одной из главных причин потери зубов в случае развития цинги. Материал для исследования Свежая моча. Принцип При окислении и декарбоксилировании гидроксипролина образуется вещество, которое с n‑диметиламинобензальдегидом даёт окрашенное соединение розового цвета. Интенсивность окраски пропорциональна концентрации гидроксипролина в пробе.
Реактивы 1) 0,01 М раствор CuSO4, 2) 2,5 М раствор NaOH, 3) 6 % раствор пероксида водорода, 4) 6 М раствор Н2SO4, 5) реактив Эрлиха (5 % раствор n‑диметиламино-бензальдегида в n‑пропаноле или изопропаноле). Лаборанты заранее готовят калибровочный график на гидроксипролин, который студенты используют для расчетов в ходе выполнения работы. Проведение анализа
Расчет Из экстинкции опытной пробы (Еоп) вычитают экстинкцию контроля (Ек): Е = Еоп — Ек Полученную величину (E) используют для нахождения содержания гидроксипролина (мкг) в анализируемой пробе по прилагаемому калибровочному графику. Для дальнейших расчетов используют формулу:
где: Х ‑ содержание гидроксипролина в моче (мг/сут); Е ‑ содержание гидроксипролина в пробе (мкг, найдено по калибровочному графику с учётом разницы экстинкций опыта и контроля), V ‑ суточный объём мочи, мл, 1000 ‑ коэффициент пересчёта мкг в мг. Нормальные величины Моча 1‑8 мг/сут (экскреция свободного гидроксипролина) Клинико-диагностическое значение Концентрация гидроксипролина в биологических жидкостях является показателем метаболизма коллагена. Выделение гидроксипролина с мочой, его содержание в плазме/сыворотке крови зависят не столько от скорости синтеза коллагена и образования фибрилл, сколько от интенсивности распада коллагена. У молодых людей более высокий уровень гидроксипролина в моче вследствие более интенсивного обмена коллагена. С возрастом (особенно в старости) экскреция гидроксипролина заметно снижается, так как коллаген труднее расщепляется коллагеназой. Экскреция гидроксипролина увеличивается вследствие ускоренного распада коллагена при заболеваниях, связанных с поражением соединительной ткани (коллагенозы, гиперпаратиреоз, поражения костей, ревматизм и др.). Содержание гидроксилированных модификаций аминокислоты пролина в крови и моче наряду с активностью фермента коллагеназы отражают скорость катаболизма коллагена, поэтому их считают маркёрами распада коллагена. Коллагенолитическая активность увеличивается при воспалении, в заживающих ранах. В стоматологической практике повышенная концентрация гидроксипролина в крови и моче обнаруживается при тяжёлых формах парадонтоза. Повышенная активность коллагеназы обнаружена в тканях ротовой полости при периодонтите и пародонтозе. Имеются данные об устойчивости коллагена зубного дентина к действию бактериальной коллагеназы при кариесе вследствие активного гликозилирования данного белка, что сопровождается снижением количества пролина и гидроксипролина в тканях зуба. Оформление работы Указывают принцип метода, регистрируют результаты, производят необходимые расчеты, делают заключение о наличии/отсутствии патологических отклонений. Лабораторная работа 2. Актуальность Гликозаминогликаны белково-углеводных комплексов составляют основное вещество матрикса соединительной ткани. При нарушении обмена в соединительной ткани активируются ферменты деградации основного вещества, из которых наиболее известна β‑гиалуронидаза. Распад углеводного компонента протеогликанов способно катализировать множество лизосомальных гидролаз (α‑нейраминидаза, β‑галактозидаза, β‑гексозоаминидаза, α‑маннозидаза, β‑маннозидазы, α‑фукозидаза, эндо‑β‑N‑ацетилглюкозаминидаза, аспартилглюкозаминидаза и др.), в результате их действия возрастает содержание гликозаминогликанов в крови и моче. Генетически детерминированные дефекты ферментов приводят к нарушению деградации протеогликанов и накоплению продуктов их неполного распада в лизосомах, что становится причиной различных заболеваний. Реактивы 1) 2,5 % раствор цетилтриметиламмониумбромида (ЦТАБ) в 1 М цитратном буфере, 2) 1 М цитратный буфер, рН 5,75 (21 г цитрата растворяют в небольшом количестве дист. воды в мерной колбе, добавляют 12 г NaOH, охлаждают, доводят дист. водой до 100 мл), 3) 0,1 % раствор толуидинового синего (0,25 г краски растворяют в 100 мл ацетона и 25 мл дист. воды), 4) 10 % раствор уксусной кислоты, 5) раствор хондроитинсульфата А (2 мг/мл). Материал для исследования Свежая моча.
|
|||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2021-04-05; просмотров: 63; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.220.1.239 (0.038 с.) |
||||||||||||||||||||||||||||||||||||||||||
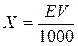 ,
,


