Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Классификация и номенклатура ферментов
В 1961 г. в Москве Комиссия по ферментам Международного биохимического союза (IUBМВ) приняла современную систематическую классификацию ферментов, учитывающую их реакционную и субстратную специфичность. Согласно классификации ферменты делят на классы – по типу катализируемой реакции, класс делят на подклассы – по природе атакуемой химической группы, подклассы делят на подподклассы – по характеру атакуемой связи или по природе акцептора или кофермента. Всего выделяют 6 классов:
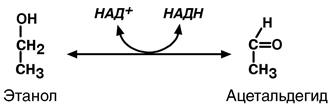
I. Оксидоредуктазы II. Трансферазы III. Гидролазы IV. Лиазы V. Изомеразы VI. Лигазы Каждому ферменту присвоен классификационный номер. Так, алкогольдегидрогеназа КФ 1.1.1.1. (оксидоредуктаза, действует на ОН‑группу донора с НАД+ в качестве акцептора, с 1-ым порядковым номером в своем подподклассе). Ферменты могут иметь тривиальное и систематическое название: 1. Тривиальное название сложилось исторически, более употребимо (пепсин, трипсин). Иногда к названию субстрата добавляют окончание "‑аза" (уреаза, амилаза, липаза). Однако у всех ферментов есть и систематическое название. 2. Систематическое название присваивают согласно современной классификации (http://www.chem.qmul.ac.uk/iubmb/enzyme/). Зачастую оно сложно в использовании, тогда его упрощают и вводят рабочее название. I класс. Оксидоредуктазы Ферменты катализируют окислительно-восстановительные реакции, лежащие в основе биологического окисления. Коферменты: НАД+, НАДФ+, ФАД, ФМН, убихинон, глутатион, липоат. В классе 22 подкласса, основные из них включают группы ферментов, действующие на: 1.1. CH-OH группу доноров; 1.2. альдегидную/кетоновую группу доноров; 1.4. CH-NH2 группу доноров; 1.5. CH-NН группу доноров; 1.6. НАДH или НАДФН в качестве доноров; 1.8. S‑содержащие группы доноров; 1.9. гем‑содержащие доноры; 1.11. Н2О2 в качестве акцептора; 1.12. водород в качестве донора; 1.13. один донор с включением О2; 1.14. два донора с включением О2; 1.15. О2• ‑ в качестве акцептора. На подподклассы делят в зависимости от акцептора – НАД+ / НАДФ+ (1.1.1., 1.2.1., 1.3.1., 1.4.1.), дисульфиды (1.2.4.), кислород (1.3.3.). Наиболее распространенные рабочие названия оксидоредуктаз: 1. Дегидрогеназы – оксидоредуктазы, катализируют дегидрирование субстрата, когда акцептор водорода – любая молекула, кроме кислорода.
2. Редуктазы – оксидоредуктазы, для которых перенос водорода от молекулы донора трудно доказуем. 3. Оксидазы – оксидоредуктазы, катализируют окисление субстратов с молекулярным кислородом в качестве акцептора электронов без включения кислорода в молекулу субстрата. 4. Монооксигеназы – оксидоредуктазы, катализируют внедрение 1 атома кислорода в молекулу субстрата с молекулярным кислородом в качестве донора. 5. Диоксигеназы – оксидоредуктазы, катализируют внедрение 2 атомов кислорода в молекулу субстрата с молекулярным кислородом в качестве донора. 6. Пероксидазы – оксидоредуктазы, катализируют реакции с пероксидом водорода в качестве акцептора электронов. Систематическое название оксидоредуктаз образуется так: донор электронов: акцептор электронов – оксидоредуктаза. Пример 1
Пример 2
Пример 3
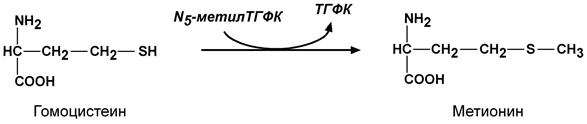
II класс. Трансферазы Катализируют реакции переноса различных групп от одного субстрата (донор) к другому (акцептор), участвуют в реакциях взаимопревращений различных веществ, обезвреживания природных и чужеродных соединений. Коферменты: пиридоксальфосфат, коэнзим А, ТГФК, метилкобаламин. В классе 9 подклассов – в зависимости от строения переносимых групп, на подклассы ферменты делят в зависимости от вида переносимой группы:
2.1. переносящие одноуглеродные фрагменты; 2.2. переносящие альдегидные и кетогруппы; 2.3. переносящие ацильные группы; 2.4. переносящие гликозильные группы; 2.6. переносящие азотсодержащие группы; 2.7. переносящие фосфорсодержащие группы; 2.8. переносящие сульфосодержащие групп;. 2.9. переносящие селенсодержащие группы. На подподклассы делят в зависимости от природы переносимой группы. Систематическое название трансфераз образуется так: Донор группы: акцептор группы – переносимая группа трансфераза. Пример 1
Пример 2
Пример 3
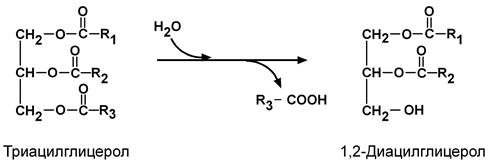
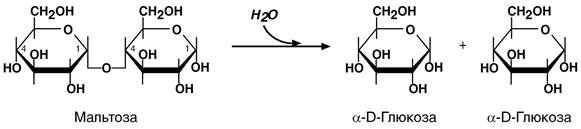
III класс. Гидролазы Гидролазы — осуществляют разрыв внутримолекулярных связей в субстрате (за исключением С-С связей) путем присоединения элементов Н2О. Гидролазы подразделяют на 13 подклассов. Коферменты у всех гидролаз отсутствуют. Ввиду сложности многих субстратов у ряда ферментов сохранены тривиальные названия: пепсин, трипсин, эластаза. Гидролазы сосредоточены в основном в желудочно-кишечном тракте и в лизосомах клеток тканей. Осуществляют распад макромолекул, образуя легко адсорбируемые мономеры. В основные подклассы гидролаз выделяют группы ферментов, катализирующих гидролиз: 3.1. сложных эфиров; 3.2. О-гликозидов; 3.3. простых эфиров; 3.4. пептидов; 3.5. непептидных азот-углеродных связей; 3.6. ангидридов кислот; 3.7. углерод-углеродных связей. Среди подподклассов выделяют, например, гидролазы карбоновых кислот (3.1.1.), гидролазы фосфомоноэфиров (3.1.3.). Наиболее часто встречаются следующие гидролазы: 1. Эстеразы – гидролиз сложноэфирных связей. 2. Липазы – гидролиз нейтральных жиров. 3. Фосфатазы – гидролиз моноэфиров фосфорной кислоты. 4. Гликозидазы – гидролизуют О- и S-гликозидные связи. 5. Протеазы, пептидазы – гидролиз белков и пептидов. 6. Нуклеазы – гидролиз нуклеиновых кислот. Систематическое название гидролаз образуется следующим образом: Гидролизуемый субстрат: отделяемая группа – гидролаза. Пример 1
Пример 2
Пример 3
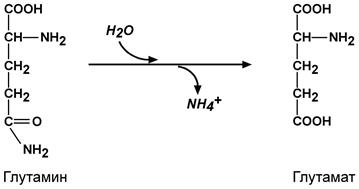
IV класс. Лиазы Лиазы — катализируют разрыв С–О, С–С, C–N и других связей, а также обратимые реакции отщепления различных групп субстратов по негидролитическому пути. Класс насчитывает около 230 ферментов. Выделяют 7 подклассов. Реакции сопровождаются образованием двойной связи или присоединением групп к месту двойной связи. Лиазы являются сложными ферментами, коферментами служат пиридоксальфосфат, тиаминдифосфат, магний, кобальт. На подклассы делят в зависимости от природы разрываемой связи: 4.1. углерод-углерод лиазы; 4.2. углерод-кислород лиазы; 4.3. углерод-азот лиазы; 4.4. углерод-сера лиазы; 4.5. фосфор-кислород лиазы. Среди подподклассов выделяют, например, карбоксилиазы (4.1.1.), гидролиазы (4.2.1.). Систематическое название ферментов класса лиаз образуют следующим образом: расщепляемый субстрат: отделяемая группа – лиаза. Пример 1
Пример 2
Пример 3
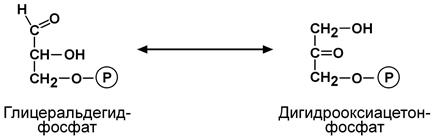
V класс. Изомеразы Изомеразы — катализ изомерных превращений в пределах одной молекулы. В классе более 80 ферментов, 6 подклассов. Изомеразы — сложные ферменты, коферментами являются дезоксиаденозилкобаламин, пиридоксалевые, пептидные (глутатион), фосфаты моносахаридов (глюкозо-1,6-дифосфат) и др. Изомеразы делят на подклассы по типу изомеризации: 5.1. Рацемазы, эпимеразы. Рацемазы — катализ взаимопревращений L-/D-изомеров, S-/R-изомеров. Эпимеразы изменяют конфигурацию при одном из хиральных атомов С: превращения рибулоза «ксилулоза, галактоза «глюкоза, манноза «галактоза, взаимопревращение a-/b-изомеров. 5.2. Цис-транс изомеразы. 5.3. Внутримолекулярные оксидоредуктазы.
5.4. Внутримолекулярные трансферазы – мутазы, осуществляют перенос химических групп внутри молекулы. 5.5. Внутримолекулярные лиазы. Среди подподклассов выделяют, например: действующие на аминокислоты и их производные (5.1.1.), на углеводы и их производные (5.1.3.), перемещающие двойные (С=С) связи (5.3.3.). Систематическое название изомераз образуется следующим образом: Субстрат – [ ] – реакция (где [ ] – обозначение, отражающее суть реакции, например, "номер изменяемого атома углерода", изменение "цис/транс", "кето/енол" или "альдозо/кетозо"). Пример 1
Пример 2
Пример 3
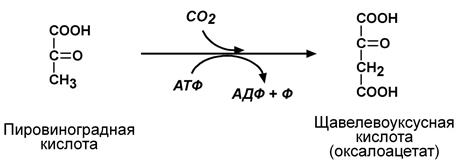
VI класс. Лигазы Лигазы (синтетазы) — ферменты, катализирующие присоединение друг к другу двух молекул с использованием энергии высокоэнергетических связей АТФ (или других макроэргов). Лигазы — сложные ферменты, содержат нуклеотидные, биотиновые, фолиевые коферменты. Выделяют 6 подклассов ферментов, формирующих связи: 6.1. Углерод-кислород. 6.2. Углерод-сера. 6.3. Углерод-азот. 6.4. Углерод-углерод. 6.5. Фосфор-кислород. 6.6. Азот-металл. Среди подподклассов выделяют, например: образующие связи аминоацил-тРНК (6.1.1.), синтезирующие соединения кислота-тиол (6.2.1.), амиды (6.3.1.). Систематическое название: Субстрат 1: субстрат 2 – лигаза. Пример 1
Пример 2
Приложение 4 Таблица основных гормонов
Примечание: 1) информацию представить по основным гормонам гипоталамуса, гипофиза, поджелудочной, надпочечников и половых желез, щитовидной и паращитовидных желез, гормонально активным формам витамина D3 (разделы 2,8), 2) дополнить графы таблицы по мере изучения частных вопросов биохимии и биохимии полости рта (разделы 9-12). Приложение 5
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2021-04-05; просмотров: 112; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.137.157.45 (0.056 с.) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||