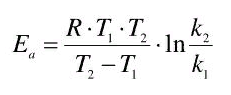Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Зависимость скорости реакции от температуры. Уравнение Вант-Гоффа. Температурный коэффициент реакции.Содержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
Скорость химической реакции зависит от многих факторов, среди которых находится температура. При повышении температуры увеличивается скорость движения молекул, возрастает число столкновений между ними и, соответственно этому доля активных молекул. Все это обусловливает увеличение скорости химических реакций с повышением температуры. Количественно зависимость скорости гомогенных реакций от температуры может быть выражена установленным опытным путём в приближенной форме правилом Вант - Гоффа: при повышении температуры на каждые 10оС скорость гомогенной химической реакции увеличивается в 2-4 раза. Уравнение, которое описывает это правило, следующее:
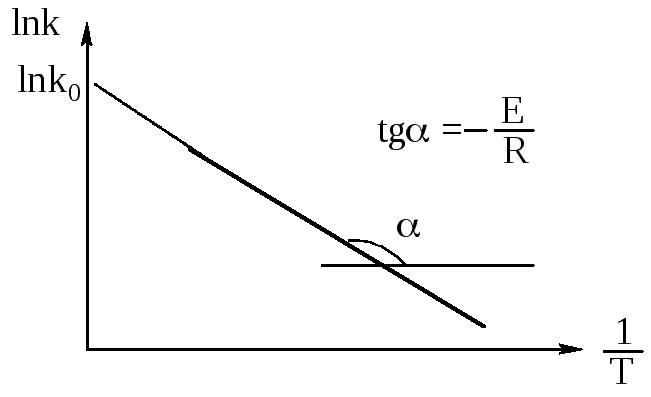
где γ = k Т+10 / k Т. Для большинства биохимических реакций температурный коэффициент Вант-Гоффа варьирует от 1,5 ¸ 3,0. Поэтому, если в результате какого-либо заболевания температура человеческого тела поднялась, например, с 36,50 до 39,50С, это значит увеличение скорости происходящих биохимических процессов в 1,13 – 1,39 раз, т. е. на 13-39%. Уравнение Аррениуса. Энергия активации Уравнение Аррениуса
Энергия активации
Катализ. Свойства катализаторов Катализ и катализаторы Катализ – это процесс изменения скорости химической реакции при помощи катализаторов – веществ, принимающих участие в химической реакции, но в состав конечных продуктов не входящих и в результате реакции не расходующихся. Одни катализаторы ускоряют реакцию (положительный катализ), другие – замедляют (отрицательный катализ). Отрицательный катализ называют ингибированием, а катализаторы, понижающие скорость химической реакции – ингибиторами. Различают гомогенный и гетерогенный катализ. Гомогенный катализ. При гомогенном (однородном) катализе реагирующие вещества и катализатор находятся в одинаковом агрегатном состоянии и между ними отсутствует поверхность раздела. Пример гомогенного катализа – реакция окисления SO 2 и SO 3 в присутствии катализатора NO (реагирующие вещества и катализатор являются газами).
Гетерогенный катализ. В случае гетерогенного (неоднородного) катализа реагирующие вещества и катализатор находятся в различных агрегатных состояниях и между ними существует поверхность (граница) раздела. Обычно катализатор – твердое вещество, а реагирующие вещества – жидкости или газы. Пример гетерогенного катализа – окисление NN 3 до NO в присутствии Pt (катализатор – твердое вещество).
|
|||||
|
Последнее изменение этой страницы: 2021-02-07; просмотров: 625; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.117.94.180 (0.007 с.) |

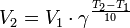
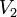 — скорость реакции при температуре
— скорость реакции при температуре 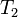 ,
, 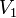 — скорость реакции при температуре
— скорость реакции при температуре 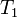 ,
, 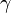 — температурный коэффициент реакции, численно равен отношению константы скорости при температуре Т + 10 к константе при температуре Т.
— температурный коэффициент реакции, численно равен отношению константы скорости при температуре Т + 10 к константе при температуре Т.