
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Давление пара разбавленных растворов неэлектролитов.Содержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте Первый закон Раул я Пример 1. Вычисление давления пара растворителя над раствором. Вычислите давление пара над раствором, содержащим 34,23 г сахара C12H22O11, в 45,05 г воды при 65ºС, если давление паров воды при этой температуре равно 2,5×104 Па. Решение: Давление пара над раствором нелетучего вещества в растворителе всегда ниже давления пара над чистым растворителем при той же температуре. Относительное понижение давления пара растворителя над раствором согласно закону Рауля выражается соотношением
где p o – давление пара над чистым растворителем; p – давление пара растворителя над раствором; n – количество растворённого вещества, моль; N – количество растворителя, моль. M (с12н22о11) = 342,30 г/моль; M (н2о) = 18,02 г/моль. Количество растворённого вещества и растворителя: n = 34,23/342,30 = 0,1 моль; N = 45,05/18,02 = 2,5 моль. p = p o – p o = 2,5×104 – 0,096×104 = 2,4×104 Па. Пример 2. Вычисление молекулярной массы неэлектролита по относительному понижению давления пара растворителя над раствором. Рассчитайте молекулярную массу неэлектролита, если 28,5 г этого вещества, растворённого в 785 г воды, вызывают понижение давления пара воды над раствором на 52,37 Па при 40ºС. Давление водяного пара при этой температуре равно 7375,9 Па. Решение: Относительное понижение давления пара растворителя над раствором равно
Находим: N = m(н2о)/M(н2о) = 785/18,02 = 43,56 моль; n = mx / Mx = 28,5/ Mx, здесь mx – масса неэлектролита, молярная масса которого Mx г/моль.
0,309 Mx = 28,298; Mx = 91,58 г/моль. Молекулярная масса неэлектролита равна ~ 92. Задачи для самостоятельного решения 127. Какую массу сахара C12H22O11 следует растворить в 800 г воды, чтобы получения раствора, давление пара которого на 33,3 Па меньше давления пара воды? Давление пара воды при 30ºС составляет 4245,2 Па. Вычислите массовую долю (%) сахара в растворе. Ответ: 13,0% 128. Какое количество неэлектролита надо растворить в 50 моль эфира, чтобы понизить давление пара при данной температуре на 2666 Па? Давление пара эфира при 30ºС равно 8,64×104 Па. Ответ: 1,6 моль 129. Вычислите молекулярную массу сероуглерода, если понижение давления пара над раствором, содержащим 0,4 моль анилина в 3,04 кг сероуглерода, при некоторой температуре равно 1003,7 Па. Давление пара сероуглерода при той же температуре 1,0133×105 Па. Ответ: 76,0 130. При некоторой температуре давление пара над раствором, содержащим 62г фенола C6H5OH в 60 моль эфира, равно 0,507×105 Па. Найдите давление пара эфира этой некоторой температуре Ответ: 0,51×105 Па 131. Вычислите давление пара раствора, содержащего 50 г этиленгликоля C2H4(OH)2 в 900 г воды. Давление пара воды при 50ºС равно 12334 Па. Ответ: 1,21×104 Па 132. Давление пара воды при 100ºС равно 1,0133×105 Па. Определите давление пара растворителя над раствором, содержащим 1,212×1023 молекул неэлектролита в 100 г воды при 100ºС. Ответ: 0,98×105 Па 133. Рассчитайте молекулярную массу эфира, если давление пара раствора, содержащего 155 г анилина C6H5NH2 в 201 г эфира, при некоторой температуре равно 42900 Па. Давление пара эфира при этой температуре равно 86380 Па. Ответ: 122,6 134. Какое количество воды приходится на 1 моль растворённого вещества в растворе, если давление пара водного раствора неэлектролита при 80ºС равно 33310 Па? Давление пара при этой температуре равно 47375 Па. Ответ: 2,4 моль 135. Определите давление водяного пара над раствором, содержащим 34,2 г сахара C12H22O11 в 90 г воды при этой температуре. Давление водяного пара при 65ºС равно 25003 Па. Ответ: 2,45×104 Па 136. Давление водяного пара над раствором 27 г глюкозы в 108 г воды при 100ºС равно 98775,3 Па. Вычислите молекулярную массу глюкозы. Ответ: 180 137. Рассчитайте, каково соотношение между числом молей растворённого вещества и растворителя в растворе и определите массовую долю (%) глюкозы в водном растворе, если величина понижения давления пара составляет 5% от давления пара чистого растворителя? Ответ: 34,5%; 19:1 138. В каком объёме воды следует растворить 16 г метилового спирта для получения раствора, давление пара которого составляет 1200 Па при 10ºС? Давление пара воды при той же температуре составляет 1227,8 Па. Вычислите массовую долю (%). Ответ: 389,0 г; 4,0% 139. Вычислите давление водяного пара, если массовая доля мочевины в растворе 10%. Давление пара воды при 100ºС равно 1,0133×105 Па. Ответ: 0,98×105 Па 140. Найдите молекулярную массу неэлектролита, если давление пара над раствором 10,5 г неэлектролита в 200 г ацетона равно 21854,40 Па. Давление пара ацетона (CH3)2CO при этой температуре равно 23939,35 Па. Ответ: 32,0 141. Рассчитайте молекулярную массу неэлектролита, если при 20ºС давление водяного пара над раствором равно 1399,40 Па. Массовая доля неэлектролита в водном растворе 63%. Давление паров воды при данной температуре равно 2335,42 Па. Ответ: 46,0
|
||
|
Последнее изменение этой страницы: 2019-05-20; просмотров: 3909; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.20 (0.009 с.) |

 =
=  ,
,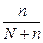 = 2,5×104 – 2,5×104
= 2,5×104 – 2,5×104  = 2,5×104 – 2,5×104×0,0385 =
= 2,5×104 – 2,5×104×0,0385 = .
.
 =
= 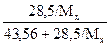 ; 0,309 Mx + 0,202 = 28,5;
; 0,309 Mx + 0,202 = 28,5;


