
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Фазовые равновесия. Правило фаз
Пример 1. Определение числа степеней свободы в гетерогенной равновесной системе. Найдите число степеней свободы в системе свинец – висмут, если из расплава Pb – Bi будут выпадать кристаллы Bi. Решение: под числом степеней свободы в равновесной гетерогенной системе понимают условия (температуру, давление, концентрацию веществ), которые можно произвольно изменять, не нарушая равновесия системы и не изменяя числа фаз в системе. Число степеней свободы С в равновесной гетерогенной системе подсчитывается с помощью правила фаз: С = К – Ф + n где: К – число независимых компонентов системы, достаточных для образования всех фаз данной системы. Определяется как разность между количеством индивидуальных веществ в данной системе и числом уравнений, связывающих эти индивидуальные вещества; Ф – число фаз в системе. При определении количества фаз учитываем агрегатное состояние веществ: все газообразные вещества образуют одну фазу, каждое твёрдое вещество образует отдельную фазу, взаимонерастворимые жидкости образуют отдельные фазы, взаиморастворимые жидкости образуют одну фазу; n – число параметров (температура и давление), действующих на систему. Для конденсированных систем (состоящих только из твердых и жидких фаз) давление не учитывается, и n = 1 (t). Для неконденсированных систем (содержащих газовую фазу n = 2 (t, Р). В данной системе число независимых компонентов равно – 2 (свинец и висмут), две фазы – расплав и кристаллы висмута. Число степеней свободы в этой гетерогенной системе: С = 2 – 2 + 1 = 1. Эта система имеет одну степень свободы, поэтому до известного предела можно изменять температуру или концентрацию компонентов системы, не нарушая равновесия системы. Задачи для самостоятельного решения
1. Определите число независимых компонентов, фазовый состав и степень свободы системы, состоящей из водного раствора сульфата калия К2SO4 и сульфата натрия Na2SO4, в присутствии паров воды и кристаллов обеих солей. 2. Определите число независимых компонентов, фазовый состав и степень свободы системы, состоящей из водного раствора сульфата калия К2SO4 и хлорида натрия NaCl, в присутствии кристаллов обеих солей. 3. Определите число независимых компонентов, фазовый состав и степень свободы системы, состоящей из водного раствора сульфата калия К2SO4 и хлорида калия КCl, в присутствии кристаллов сульфата калия К2SO4 и паров воды.
4. Определите число независимых компонентов, фазовый состав и степень свободы системы, состоящей из водного раствора сульфата натрия Na2SO4 и хлорида натрия NaCl, в присутствии кристаллов сульфата натрия Na2SO4. 5. Определите число независимых компонентов, фазовый состав и степень свободы системы, состоящей из водного раствора нитрата лития LiNO3, бромида натрия NaBr и хлорида кальция CaCl2, в присутствии паров воды и кристаллов всех солей. 6. Определите число независимых компонентов, фазовый состав и степень свободы системы, состоящей из водного раствора нитрата лития LiNO3, бромида натрия NaBr и хлорида кальция CaCl2, в присутствии паров воды и кристаллов нитрата лития LiNO3. 7. Определите число независимых компонентов, фазовый состав и степень свободы системы, состоящей из водного раствора нитрата лития LiNO3, бромида натрия NaBr и хлорида кальция CaCl2, в присутствии паров воды и кристаллов всех солей. 8. Определите число независимых компонентов, фазовый состав и степень свободы системы, состоящей из водного раствора нитрата лития LiNO3, бромида натрия NaBr и хлорида кальция CaCl2, в присутствии паров воды и кристаллов хлорида кальция CaCl2. 9. Определите число независимых компонентов, фазовый состав и степень свободы системы, состоящей из водного раствора нитрата лития LiNO3, бромида натрия NaBr и хлорида кальция CaCl2, в присутствии паров воды и кристаллов бромида натрия NaBr. 10. Определите число независимых компонентов, фазовый состав и степень свободы системы, состоящей из водного раствора нитрата никеля Ni(NO3)2, хлорида олова (II) SnCl2, иодида цинка ZnI2, в присутствии паров воды и кристаллов всех солей. 11. Определите число независимых компонентов, фазовый состав и степень свободы системы, состоящей из водного раствора нитрата никеля Ni(NO3)2, хлорида олова (II) SnCl2, иодида цинка ZnI2, в присутствии паров воды и кристаллов нитрата никеля Ni(NO3)2. 12. Определите число независимых компонентов, фазовый состав и степень свободы системы, состоящей из водного раствора нитрата никеля Ni(NO3)2, хлорида олова (II) SnCl2, иодида цинка ZnI2, в присутствии паров воды и кристаллов хлорида олова (II) SnCl2.
13. Определите число независимых компонентов, фазовый состав и степень свободы системы, состоящей из водного раствора нитрата никеля Ni(NO3)2, хлорида олова (II) SnCl2, иодида цинка ZnI2, в присутствии паров воды и кристаллов иодида цинка ZnI2. 14. Определите число независимых компонентов, фазовый состав и степень свободы системы, состоящей из водного раствора нитрата никеля Ni(NO3)2, хлорида олова (II) SnCl2, иодида цинка ZnI2, в присутствии кристаллов всех солей. 15. Определите число независимых компонентов, фазовый состав и максимальное число фаз системы, состоящей из раствора хлористого кальция CaCl2, хлористого стронция SrCl2 и хлористого бария BaCl2 в воде? 16. Определите число независимых компонентов, фазовый состав и максимальное число фаз системы, состоящей из свинца Pb, олова Sn и висмута Bi? 17. Определите число независимых компонентов, фазовый состав и степень свободы системы, в которой из жидкого расплава свинца Pb и сурьмы Sb частично выпали кристаллы сурьмы Sb. 18. Определите число независимых компонентов, фазовый состав и степень свободы системы, в которой из жидкого расплава свинца Pb и сурьмы Sb частично выпали кристаллы свинца Pb. 19. При 144°С жидкий расплав, состоящий из 40% кадмия Cd и 60% висмута Bi находится в равновесии с твердыми кристаллами кадмия и висмута. Определите число независимых компонентов, фазовый состав и степень свободы системы. 20. Найдите число степеней свободы в системе свинец – серебро, если из расплава Pb – Ag одновременно выделяются кристаллы свинца и серебра. 21. Найдите число степеней свободы в системе свинец – серебро, если из расплава Pb – Ag выделяются кристаллы свинца. 22. Приведите примеры однокомпонентных систем состоящих из одной, двух, трех фаз. 23. Приведите примеры двухкомпонентных систем, состоящих из одной, двух, трех и четырех фаз. 24. Возможно ли существование однокомпонентной системы, состоящей из четырех фаз? 25. Возможно ли существование пяти фаз в двухкомпонентной и трехкомпонентной системе? Диаграммы состояний
Пример 1. Золото Au и платина Pt в твёрдом состоянии образуют непрерывный ряд твёрдых растворов и смешиваются в жидком состоянии во всех соотношениях. Используя диаграмму состояния этих сплавов (рис.1.1): 1. построить кривую охлаждения сплава, состоящего из 40% золота Au и 60% платины Pt; 2. определить при 1400°С состав и количественное соотношение жидкой и твёрдой фаз для сплава, содержащего равные количества обоих компонентов.
состояния Au - Pt
Решение: 1. Для построения кривой охлаждения определим, через какие области диаграммы пройдет точка а. Выше линии АМВ точка движется в гомогенной области жидкого расплава. При достижении линии АМВ из жидкого расплава начинают выпадать кристаллы твёрдого раствора. В связи с этим составы жидкой и твёрдой фаз изменяются. Состав твёрдой фазы по мере понижения температуры изменяется по линии солидуса (линия АNВ), а состав жидкой фазы – по линии ликвидуса (линия АМВ). На кривой охлаждения наблюдаются два перегиба: в точке пересечения с линией ликвидуса и в точке пересечения с линией солидуса. 2. Для определения количественного соотношения твёрдой и жидкой фаз применимо правило рычага. Для этого от точки О (точка пересечения перпендикуляра, восстановленного из точки на оси концентраций, соответствующей сплаву из 50% платины и 50% золота, и прямой, проходящей через 1400°С) измеряем длину отрезков ОN и ОМ; соотношении их длин соответствует количественному соотношению интересующих нас фаз.
Допустим, что длина отрезка ОN равна 15 мм, а длина отрезка ОМ – 10мм. Тогда соотношение жидкой и твёрдой фаз составит 10: 15. Зная количество сплава, можно рассчитать и количество каждой фазы. Предположим, что вес сплава 5 кг. Это количество будет пропорционально всей длине линии МN, т.е. 10 + 15 = 25мм. Тогда количество твёрдой фазы будет равно 15: 25 = Х: 5, откуда Х = 3 кг. Состав определяется, если из конечных точек прямой МN опустить перпендикуляры на ось концентраций. Перпендикуляр, опущенный из точки М на ось концентраций, определяет состав жидкой фазы, а перпендикуляр, опущенный из точки N, дает состав твёрдой фазы. В нашем случае состав твёрдой фазы содержит около 65% платины Pt, а состав жидкой фазы – 30 % платины Pt. Задачи для самостоятельного решения
26. Эвтектика сплава Ag – Сu (рис. 1.2) имеет состав: 28% Сu и 72% Ag. Какая масса эвтектики содержится в 750 г твёрдого сплава, если сплав содержит 63% Сu и 37% Ag? Рис. 1.2 27. По диаграмме плавкости (рис. 1.2) найдите состав жидкой и твёрдой фаз в системе, содержащей 85% Ag и 15% Сu при 930 °С. Какая масса твёрдой фазы выделится из 2,3 кг сплава при этой температуре? 28. По диаграмме плавкости (рис. 1.2) найдите состав жидкой и твёрдой фаз в системе, содержащей 30% Ag и 70% Сu при 950 °С. Какая масса твёрдой фазы выделится из 10,5 кг сплава при этой температуре? 29. По диаграмме плавкости (рис. 1.2) найдите состав жидкой и твёрдой фаз в системе, содержащей 50% Ag и 50% Сu при 900 °С. Какая масса твёрдой фазы выделится из 1,5 кг сплава при этой температуре? 30. Сколькими степенями свободы обладает система, 33. При какой температуре будет затвердевать и плавиться сплав, содержащий 80% Аu и 20% Pt? Определите число степеней свободы для сплава данного состава при 1200°С (рис. 1.3). 34. При какой температуре будет затвердевать и плавиться сплав, содержащий 20% Аu и 80% Pt? Определите число степеней свободы для сплава данного состава при 1200°С (рис. 1.3). 35. По диаграмме плавкости системы Mg – Zn (рис. 1.4) определите формулу интерметаллического соединения, образуемого этими металлами. Какова масса химического соединения, содержащегося в 250 г сплава состава:
40% Zn и 60% Mg?
Рис. 1.3 Рис. 1.14
36. Определить с помощью диаграммы (рис.1.5) сколько хлорида калия KCl нужно прибавить к 2,5 кг хлорида лития LiCl, чтобы понизить температуру его затвердевания до 500°С. 37. Определите с помощью диаграммы (рис.1.5) сколько хлорида калия КCl выделится из 6500 г 80%-ного (по КCl) расплава при охлаждении до 600, 500, 400 и 361°С, 38. Определите с помощью диаграммы (рис. 1.5) сколько останется жидкости если охладить 1250 г 35 %-ного расплава до 450°С. 39. Определите с помощью диаграммы (рис.1.5) сколько хлорида калия KCl нужно прибавить к 4,8 кг хлорида лития LiCl, чтобы понизить температуру его затвердевания до 450°С. 40. Определите с помощью диаграммы (рис.1.5) сколько нужно прибавить хлорида лития LiCl к 1,8 кг хлорида калия KCl, чтобы понизить температуру его затвердевания до 550°С. 41. Определите с помощью диаграммы (рис.1.5) сколько нужно прибавить хлорида лития LiCl к 5,5 кг хлорида калия KCl, чтобы понизить температуру его затвердевания до 450°С.
42. На диаграмме (рис. 1.6), обозначьте следующие состояния системы висмут – кадмий Bi – Cd: точка А – чистый твёрдый висмут Bi в равновесии с жидким висмутом Bi; точка Б – чистый твёрдый кадмий Cd в равновесии с жидким кадмием Cd; точка В – жидкий сплав при 200°, содержащий 20 % кадмия Cd; точка Г – сплав, содержащий 15 % кадмия Cd в равновесии с кристаллами висмута Bi; точка Д – систему, состоящую из равных количеств твёрдого кадмия Cd и жидкого сплава, содержащего 75 % кадмия Cd; точка Е – жидкий сплав в равновесии с твёрдым кадмием Cd и висмутом Bi. 43. Определите с помощью диаграммы (рис. 1.6), сколько кадмия Cd выделяется из 350г 55%-ного расплава при охлаждении его до 150°С. 44. Определите с помощью диаграммы (рис. 1.6), сколько кадмия Cd выделяется из 1300г 65%-ного расплава при охлаждении его до 150°С. 45. Определите с помощью диаграммы (рис. 1.6), сколько кадмия Cd выделяется из 600г 75%-ного расплава при охлаждении его до 150°С. 46. Определите с помощью диаграммы (рис. 1.6), сколько кадмия Cd выделяется из 800г 80%-ного расплава при охлаждении его до 200°С. 48. Определите с помощью диаграммы(рис. 1.6), сколько кадмия Cd выделится из 1,5 кг 90 %-ного сплава, если его охладить до 350, 250 и 144°. 47. Определите с помощью диаграммы (рис. 1.6), сколько эвтектики получится из 1,5 кг сплава, содержащего 85 % кадмия Cd. 49. Определите с помощью диаграммы (рис. 1.6), сколько висмута Bi нужно прибавить к 150 г 70 %-ного сплава, охлажденного до 200°С чтобы выпавший кадмий Cd растворился. 50. Из скольких фаз состоит сплав, содержащий 20% Bi и80 % Cd при 250ºС? Сколькими степенями свободы обладает эта система (рис. 1.6)?
Перегонка. Состав смеси Пример 1. Рассчитайте, в каком весовом соотношении будут перегоняться вода и бромбензол, если при 95,25°С давление паров бромбензола равно 121 мм рт.ст., а воды – 639 мм рт.ст. Жидкости взаимонерастворимы. Решение: Молекулярная масса воды равна 18 г/моль, а бромбензола – 157г/моль. Для решения используем уравнение:
Т. о., отношение веса бромбензола к весу воды в дистилляте будут составлять 1,65. Т.е. на 100 кг перегнанной воды будет приходиться 165 кг бромбензола. Соотношение числа молей этих веществ составит 121: 639 = 1: 5, т.е. с 1 молем бромбензола будет перегоняться 5 молей воды.
Пример 2. Задача. Две жидкости А и В неограниченно растворимы друг в друге. Давление пара этой смеси при 150°С представляет линейную функцию от концентрации. Давление пара компонента А при этой температуре равно 800 мм рт.ст., а компонента В – 500 мм рт.ст. Вычислите отношение числа молей компонента А к числу молей компонента В в парах над смесью содержащей 5 мол.% компонента А. Определите состав смеси, кипящей при температуре 150°С под давлением 760 мм рт.ст. Решение: а) для определения соотношения компонентов А и В в паровой фазе найдём значения парциальных давлений этих компонентов над смесью, состоящей из 95 мол.% вещества В и 5 мол.% вещества А.
Подставив Ха = 0,05, Ра = 800 мм рт.ст и Рв = 500 мм рт.ст. получим: Ра = 0,005 × 800 = 40 мм.рт.ст. Рв = 0,95 × 500 = 495 мм рт.ст. Соотношение числа молей компонентов в паровой фазе равно соотношению парциальных давлений этих компонентов.
Т.о. при температуре 150°С над жидкой смесью, состоящей из 95 мол.% вещества В и 5 мол.% вещества А, в паровой фазе на 100 молей вещества В приходится 8 молей вещества А. Общее давление пара над смесью сумме парциальных давлений компонентов: 40 + 495 = 535 мм рт.ст. б) мольную долю вещества А в смеси, кипящей под давлением 760мм рт.ст. определяем по уравнению: Р = Ха(Ра – Рв) + Рв, 760 = Ха (800 – 500) + 500,
Следовательно, смесь, кипящая при температуре 150°С и давлении 760 мм рт.ст. содержит 0,87 мольных долей компонента (87 мол.%) А и 0,13 мольных долей (13 мол.%) компонента В. Задачи для самостоятельного решения 51. Камфара и вода нерастворимы друг в друге. Сколько следует отогнать водяного пара, чтобы получить в дистилляте 30 г камфары. Смесь воды и камфары кипит при 99°С и давлении 760 мм рт.ст. Молекулярный вес камфары равен 152. Давление паров воды составляет 733 мм рт.ст. при 99°С? 52. Нитробензол и воданерастворимы друг в друге. Рассчитайте,какое количество нитробензола отгонится с водяным паром при перегонке данной смеси, если общее количество дистиллята составляет 20 кг. Смесь начинает кипеть при температуре 99°С и давлении 760 мм рт.ст. Давление паров воды равно при этой температуре 733 мм рт.ст., а нитробензола – 27мм рт.ст. 53. При 50°С давление пара чистого дихлорэтана равно 236,2 мм рт.ст., а бензола – 268 мм рт.ст. Бензол и дихлорэтан взаиморастворимы. Давление пара смеси бензола и дихлорэтана в зависимости от концентрации выражается прямой линией. Определить состав жидкости (масс. %), при условии, что парциальные давления компонентов равны между собой. 54. Жидкая смесь содержит 25% бензола. Толуол имеет давление паров 290мм рт.ст., а бензол – 753 мм рт.ст. при 80°С. Каков весовой состав паров смеси этих веществ (масс. %)? 55. Давление паров чистого толуола равно 36,7 а бензола – 120,2 мм рт.ст. при 30 °С. Жидкость содержит эти компоненты в эквимолярных количествах. Какой состав (масс. %) имеет парообразная фаза. 56. При 250,9 мм рт.ст. и 70°С жидкость, несмешивающаяся с водой, перегоняется с водяным паром. Вода при этой температуре имеет давление паров 233,7 мм рт.ст. Полученный дистиллят содержит 18,82 масс. % жидкости. Вычислить молекулярный вес этой жидкости. 57. Температура кипения азотной кислоты 86 °С. Температура кипения чистой воды 100°С. Азотная кислота и вода образуют азеотропную смесь, содержащую 68 % кислоты и 32% воды. Температура кипения азеотропной смеси 120,5°С. Определите, что останется в остатке, и какой компонент будет преимущественно отгоняться при перегонке смесей содержащих: а) 82% кислоты и 18% воды; б) 55% кислоты и 45% воды? 58. Температура кипения хлористого водорода 85°С. Температура кипения чистой воды 100°С. Хлористый водород и вода образуют азеотропную смесь, состоящую из 20,24% хлористого водорода и 79,76% воды. Температура кипения азеотропной смеси 108,5°С. Определите, что станется в остатке, и какой компонент будет отгоняться, если подвергнуть перегонке смеси, содержащие: а) 12% хлористого водорода и 88% воды; б) 55% хлористого водорода и 45% воды? 59. Температура кипения этилового спирта 78,3°С, а воды – 100°С. Этиловый спирт и вода образуют азеотропную смесь состоящую из 4,43 % воды и 95,57% спирта. Температура кипения азеотропной смеси 78,13°С. Определите, что останется в остатке, и что будет отгоняться при дистилляции смесей, содержащих: а) 72% воды и 38% спирта; б) 3% воды и 97% спирта? 60. Температура кипения пиридина равна 115°С. Температура кипения воды равна 100°С. Вода и пиридин образуют азеотропную смесь, содержащую 41% воды и 59% пиридина. Температура кипения азеотропной 92°С. Определите, что будет перегоняться и что останется в остатке при дистилляции смесей, содержащих: а) 75% воды и 25% пиридина; б) воды 75% и пиридина 25%? 61. Температура кипения метилового спирта 65°С, а ацетона – 56°С. Эти вещества образуют азеотропную смесь, содержащую 86,5 % ацетона. Температура кипения азеотропной смеси 55,95°С. Определите, что будет перегоняться и что останется в остатках при дистилляции смесей, содержащих: а) 78% спирта и 22% ацетона; б) 6% спирта и 94% ацетона?
|
|||||||||||
|
Последнее изменение этой страницы: 2019-05-20; просмотров: 1408; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.142.171.180 (0.087 с.) |
 Рис. 1.1. Диаграмма
Рис. 1.1. Диаграмма

 Рис.1.5
Рис.1.5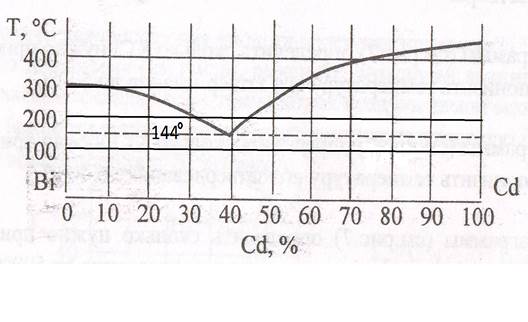 Рис. 1.6
Рис. 1.6



 1 – Ха = 1 – 0,87 = 0,13
1 – Ха = 1 – 0,87 = 0,13


