
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Температура замерзания и кипения растворов
Неэлектролитов. Второй закон Рауля. Пример 1. Определение температуры кипения и замерзания раствора неэлектролита. Определите температуру кипения и замерзания раствора, содержащего 1 г нитробензола C6H5NO2 в 10 г бензола. Эбулиоскопическая и криоскопическая константы бензола соответственно равны 2,57 и 5,1ºС. Температура кипения чистого бензола 80,2ºС, температура замерзания – 5,4ºС. Решение. По закону Рауля следует, что Δtзам= где Δ t зам и Δ t кип – соответственно понижение температуры замерзания и повышение температуры раствора; K к и K э – соответственно криоскопическая и эбуллиоскопическая константы растворителя; g – масса растворённого вещества, г; G – масса растворителя, г; Mr – молекулярная масса растворённого вещества; Mr (C6H5NO2) = 123,11. Повышение температуры кипения раствора нитробензола в бензоле: Δ t кип= Температура кипения раствора: t кип = 80,2 + 2,09 = 82,29 ºС. Понижение температуры замерзания раствора нитробензола в бензоле: Δ t зам = Температура замерзания раствора: Δ t зам = 5,4 – 4,14 = 1,26 ºС.
Пример 2. Вычисление молекулярной массы неэлектролита по повышению температуры кипения раствора. Раствор камфоры массой 0,552 г в 17 г эфира кипит при температуре на 0,461 ºС выше, чем чистый эфир. Эбуллиоскопическая константа эфира 2,16ºС. Определите молекулярную массу камфоры. Решение. Молекулярную массу камфоры определяем, пользуясь соотношением M r = Молекулярная масса камфоры равна 155,14.
Задачи для самостоятельного решения 142. Массовая доля глюкозы C6H12O6 равна 10%. Определите температуру кипения водного раствора глюкозы. Кэ(Н2О) = 0,516 Ответ: 100,32 ºС 143. Рассчитайте молекулярную массу серы S в растворе, если раствор, содержащий 0,162 г серы в 20 г бензола С6Н6, кипит при температуре на 0,081ºС выше, чем чистый бензол. Кэ(С6Н6) = 2,57 Ответ: 256,0 144. Температура кипения эфира равна 35,60ºС и Kэ = 2,16ºС. Определите температуру кипения раствора 1 г нафталина C10H8 в 20 г эфира. Ответ: 35,44 ºС 145. Вычислите молекулярную массу неэлектролита, если раствор 1,05 г неэлектролита в 30 г воды замерзает при –0,7ºС. Кк(Н2О) = 1,85 Ответ: 92,5 146. Определите температуру замерзания раствора неэлектролита, содержащего 2,02×1023 молекул 1 л воды? Кк(Н2О) = 1,85 Ответ: –0,62 ºС
147. Рассчитайте молекулярную массу камфоры, если понижение температуры замерзания раствора 0,052 г камфоры в 26 г бензола С6Н6 равно 0,067ºС . Кк(С6Н6) = 5,1 Ответ: 152,2 148. Вычислите температуру замерзания раствора, который содержит 20 г сахара C12H22O11 в 400 г воды. Кк(Н2О) = 1,85 Ответ: –0,27ºС 149. Кк(Н2О) = 1,85. Вычислите количество этиленгликоля C2H4(OH)2, которое необходимо прибавить на каждый килограмм воды для приготовления антифриза с точки замерзания –15ºС. Ответ: 502,8 г 150. Чистый ацетон СН3СОСН3 кипит при 56,0ºС. Раствор, состоящий из 9,2 г глицерина C3H5(OH)3 и 400 г ацетона, кипит при 56,38ºС. Вычислите эбулиоскопическую константу ацетона. Ответ: 1,52ºС 151. Кк(Н2О) = 1,85. При какой температуре будет замерзать раствор, содержащий в 4 л H2O 500 г этиленгликоля C2H4(OH)2? Ответ: –3,73ºС 152. Раствор, содержащий 0,2 г некоторого вещество в 26 г бензола С6Н6, замерзает при температуре на 0,318 ºС ниже, чем чистый бензол. Массовые доли углерода, водорода и серы, входящих в состав вещества, соответственно равны 39,34, 8,20 и 52,46%. Определите формулу этого вещества. Ответ: C4H10S2 153. Чему равна температура замерзания приготовленного антифриза, если для приготовления антифриза на 30 л взято 9 л глицерина C3H5(OH)3? Плотность глицерина 1261 кг/м3. Ответ: −7,6°С 154. Массовая доля этилового спирта в водном растворе C2H5OH ω = 25%. При какой температуре будет замерзать этот раствор. Ответ: −13,4°С 155. Сколько атомов входит в состав молекулы иода In, находящегося в растворенном состоянии в растворе, состоящем из 9,2 г иода и 100 метилового спирта СН3ОН, который закипает при 65,0ºС? Температура кипения спирта 64,7ºС, а его эбуллиоскопическая константа K э = 0,84ºС. Ответ: I2
156. Температура замерзания чистого бензола С6Н6 5,40ºС. Какая масса нафталина C10H8 находится в 8 кг бензола, если этот раствор замерзает при 3,45ºС? Ответ: 392 г
|
||||||
|
Последнее изменение этой страницы: 2019-05-20; просмотров: 2288; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.131.13.37 (0.009 с.) |
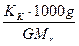 ; Δtкип=
; Δtкип= 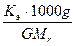 ,
,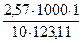 =2,09 ºС.
=2,09 ºС.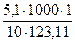 = 4,14 ºС.
= 4,14 ºС.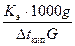 =
= 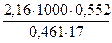 = 155,14.
= 155,14.


