
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Ое начало термодинамики и его различные формулировки . Статистически смысл 2-го начала термодинамикиСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте Второе начало термодинамики можно сформулировать как закон возрастания энтропии замкнутой системы при необратимых процессах: любой необратимый процесс в замкнутой системе происходит так, что энтропия системы при этом возрастает.
Можно дать более короткую формулировку второго начала термодинамики: в процессах, происходящих в замкнутой системе, энтропия не убывает. Существенен момент, что речь идет о замкнутых системах, так как в незамкнутых системах энтропия может вести себя произвольным образом (возрастать, убывать, оставаться постоянной). Кроме того, повторим еще раз, что энтропия остается постоянной в замкнутой системе только при обратимых процессах. При необратимых процессах и в замкнутой системе энтропия всегда возрастает. Формула Больцмана S=k•lnW дает объяснение постулируемое вторым началом термодинамики возрастанию энтропии в замкнутой системе при необратимых процессах: возрастание энтропии означает переход системы из менее вероятных в более вероятные состояния. Значит, формула Больцмана дает статистическое толкование второго начала термодинамики. Являясь статистическим законом, оно описывает закономерности хаотического движения огромного числа частиц, которые составляющих замкнутую систему. Дадим еще две формулировки второго начала термодинамики: 1) по Кельвину: невозможен круговой процесс, единственным результатом которого является превращение теплоты, полученной от нагревателя, в эквивалентную ей работу; 2) по Клаузиусу: невозможен круговой процесс, единственным результатом которого является передача теплоты от менее нагретого тела к более нагретому
52. Энтропия. Её физический смысл. Вычисление изменения энтропии в различных процессах ЭНТРОПИЯ - (от греч. entropia - поворот - превращение) (обычно обозначаетсяS), функция состояния термодинамической системы, изменение которой dS в равновесном процессе равно отношению количества теплоты dQ, сообщенного системе или отведенного от нее, к термодинамической температуре Т системы. Неравновесные процессы в изолированной системе сопровождаются ростом энтропии, они приближают систему к состоянию равновесия, в котором S максимальна. Понятие "энтропия" введено в 1865 Р. Клаузиусом. Энтропия системы является функцией ее состояния, определенная с точностью до произвольной постоянной.
Таким образом, по формуле (6.2.1) можно определить энтропию лишь с точностью до аддитивной постоянной, т.е. начало энтропии произвольно. Физический смысл имеет лишь разность энтропий.
Таким образом, изменение энтропии ΔS1-2 идеального газа при переходе его из состояния 1 в состояние 2 не зависит от вида перехода 1 - 2.
53. Холодильная машина и нагреватель. Её эффективность. Холодильная машина – это машина, работающая по обратному циклу Карно (рис. 5.4). То есть если проводить цикл в обратном направлении, тепло будет забираться у холодильника и передаваться нагревателю (за счет работы внешних сил). Обратный цикл Карно можно рассмотреть на примере рис. 5.5. При изотермическом сжатии В–А, от газа отводится количество теплоты Q1 при Т1. В процессе изотермического расширения D–С к газу подводится количество теплоты Q2. В этом цикле
Если рабочее тело совершает обратный цикл, то при этом можно переносить энергию в форме тепла от холодного тела к горячему за счет совершения внешними силами работы. Для холодильных машин, работающих по циклу Карно
54. Теоремы Карно. Неравенство Клаузиуса. Теоремы Карно. Французским инженером С. Карно были исследованы различные циклы, по которым работают тепловые машины, и сформулированы некоторые общие принципы, касающиеся теоретически возможных КПД таких машин. Теперь эти принципы известны как теоремы Карно, которые гласят: 1. КПД обратимого цикла Карно, осуществляемого между двумя источниками теплоты, не зависит от свойств рабочего вещества, с помощью которого этот цикл осуществляется. (КПД тепловой машины, работающей по циклу Карно не зависит от рода в-ва и конструктивных особенностей машины, а зависит только от температуры нагревателя Т1 и температуры холодильника Т2.)
2. КПД тепловой машины, работающей по обратному циклу Карно максимально.
КЛАУЗИУСА НЕРАВЕНСТВО -неравенство, выражающее теорему термодинамики: для кругового процесса.
|
||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-04-06; просмотров: 2101; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.102 (0.009 с.) |



 .
.
 ,
,
 ,
,
 , или
, или
 .
.
 , т.к.
, т.к. 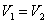 ;
;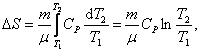 т.к. Р1 = Р2;
т.к. Р1 = Р2;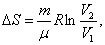 т.к.
т.к. 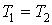 ;
;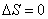 , т.к.
, т.к. 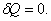
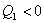 ,
,  и работа, совершаемая над газом, отрицательна, т.е.
и работа, совершаемая над газом, отрицательна, т.е.
 .
.




