
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Предмет и задачи термодинамикиСодержание книги
Поиск на нашем сайте
Термодинамика возникла в конце первой половины 19 века. В тот период цель термодинамики сводилась к установлению взаимосвязи между теплотой и работой и разработке теории паровой машины. В дальнейшем цели термодинамики расширяются и основные ее положения используются в различных областях, в том числе и химии. Термодинамика базируется на трех законах, из которых все остальные положения данной науки можно получить путем логических рассуждений. Первый закон термодинамики связан с законом сохранения энергии и позволяет рассчитывать тепловые балансы процессов. Второй закон термодинамики - закон о возможности протекания самопроизвольных процессов. Третий закон термодинамики - закон об абсолютном значении энтропии. Та часть термодинамики, которая имеет дело с применением этих законов к химическим процессам и фазовым переходам называется химической термодинамикой. Химическая термодинамика разрабатывает наиболее рациональные методы расчета тепловых эффектов химических процессов, раскрывает закономерности при равновесии, определяет благоприятные условия для осуществления химического процесса.
ОСНОВНЫЕ ПОНЯТИЯ И ОПРЕДЕЛЕНИЯ ХИМИЧЕСКОЙ ТЕРМОДИНАМИКИ
СИСТЕМА - тело или группа тел, мысленно выделенная из окружающей среды. ОТКРЫТАЯ СИСТЕМА - система, которая может обмениваться с окружающей средой энергией и веществом. ЗАКРЫТАЯ СИСТЕМА - отсутствует обмен веществом с окружающей средой, но она может обмениваться энергией с ней. ИЗОЛИРОВАННАЯ СИСТЕМА - система, объем которой остается постоянным и которая не обменивается энергией и веществом с окружающей средой. Система может быть гомогенной или гетерогенной. Совокупность всех физических и химических свойств системы называется состоянием системы. Свойства, которые могут быть выражены через функции температуры, давления и концентрации веществ называются термодинамическими. Для полного описания системы достаточно знать некоторое наименьшее число термодинамических свойств, которые рассматривают как внутренние параметры системы (параметры состояния системы). Обычно в качестве параметров состояния системы выбирают такие ее свойства, которые наиболее легко определить экспериментальным путем, например давление (Р),объем (V),температура (Т) и концентрация (Сi)компонентов.
Параметры состояния системы связаны между собой соотношением, которое называется уравнением состояния. В общем виде f(P,V,T) = 0 PV = n RT ТЕРМОДИНАМИЧЕСКИЙ ПРОЦЕСС - изменение во времени хотя бы одного из термодинамических свойств. САМОПРОИЗВОЛЬНЫЕ ПРОЦЕССЫ - процессы, не требующие затраты энергии извне. НЕСАМОПРОИЗВОЛЬНЫЕ ПРОЦЕССЫ -процессы, требующие затраты энергии. РАВНОВЕСНОЕ СОСТОЯНИЕ - состояние системы, которое сохраняется неизменным во времени. ПОСТУЛАТ - Протекание самопроизвольного процесса в конечном счете приводит систему в равновесное состояние. ВНУТРЕННЯЯ ЭНЕРГИЯ - совокупность всех видов энергии частиц в системе. Обозначается U. Является функцией состояния, т.е. ее изменение не зависит от того как идет процесс, а будет определяться только исходным и конечным состояниями системы. РАБОТА ПРОЦЕССА - форма передачи энергии от изучаемой системы к окружаюшей среде или от окружающей среды к системе путем преодоления сил, действующих на систему со стороны окружающих тел или в противоположном направлении. Обозначается W(A). Работа, совершаемая системой, принимается положительной, а работа окружающей среды отрицательной. Полная работа (W) рассматривается как сумма работ изменения объема системы и всех других видов работ, связанных с преодолением сил, действующих на систему, называемых полезной работой (Wп). Работа определяется соотношением W = Если действующая сила вызвана внешним давлением (F = PS), где S - площадь, к которой приложено давление, то работа преодоления внешнего давления W = Полная работа W = ТЕПЛОТА ПРОЦЕССА (Q) - форма передачи энергии от изучаемой системы к окружающей среде путем микрофизических процессов (столкновений молекул).Теплота считается положительной, когда она подводится к системе.
ПЕРВЫЙ ЗАКОН ТЕРМОДИНАМИКИ
Он является по существу законом сохранения энергии, представленным в форме, удобной для термодинамического анализа. Закон сохранения энергии - энергия не возникает из ничего и не исчезает бесследно, она может лишь в различных формах переходить от одних тел к другим, но общее ее количество в изолированной системе не изменится ни при каких условиях.
В термодинамике изменение внутренней энергии системы выражается через количество теплоты и работ, которыми система обменивается с окружающей средой. С учетом правила знаков первый закон термодинамики математически выражается DU = Q - W = Q - Для бесконечно малого изменения
dU =δQ - δW =δQ - PdV - δWn
Формулировки первого закона 1.Изменение внутренней энергии термодинамической системы равно разности между количеством теплоты, подведенной к системе и количеством работы, совершенной системой. 2.Вечный двигатель первого рода невозможен или нельзя совершать работу без затраты энергии. 3.Внутренняя энергия изолированной системы постоянна (dU = 0, U = const)
|
||||||
|
Последнее изменение этой страницы: 2016-08-15; просмотров: 284; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.144.206.120 (0.007 с.) |

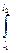 F dl
F dl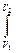 P dV
P dV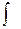 PdV – Wп
PdV – Wп


