
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
II. Реакции отщепления галогенаСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте 1. Отщепление галогена атомарным водородом по методу Степанова СН3-Сl + 2H 2C2H5OH+2Na Метод используется для количественного определения галогенов в органических соединениях. 2.Отщепление галогенов под действием металлов: а) реакция Вюрца СH3Br + 2Na + Br-CH3 б) получение этиленовых углеводородов СH2-CH2 + Zn Cl Cl в) получение циклических углеводородов СH2-CH2-CH2 + Zn Br Br CH2 г) под действием магния С2H5Br + Mg -MgBr(OH)
III. Реакции отщепления галогеноводорода 1. При нагревании СH3-CH2Cl 2. Под действием спиртового раствора щелочи СH3-CH3-Cl + KOHспиртовый A B
H H H HO- H H K+ R=k[A][B] Реакция нуклеофильного отщепления протекает по механизму ЕN2. У третичных галоидных алкилов идет, в основном, по механизму ЕN1. H CH3 H CH3 CH3 H-C-C-Cl H CH3 H CH3 CH3 А изобутилен r=k[A] Такие реакции обычно сопутствуют реакциям нуклеофильного замещения. ЛЕКЦИЯ 7 ГАЛОГЕНОПРОИЗВОДНЫЕ НЕПРЕДЕЛЬНЫХ УГЛЕВОДОРОДОВ
Подразделяются на три типа. I. Галогенопроизводные винилового типа: атом галогена находится у непредельного атома углерода. СН2=СНCl хлористый винил СН2=ССl2 хлористый винилиден СН2=С-СН=СН2 хлорпрен Cl II. Галогенпроизводные аллильного типа (галоген в СН2=СН-СН2-Сl хлористый аллил СН3-СН=СН-СН2Cl хлористый кротил III. Галогенпроизводные с изолированным расположением двойной связи и Hal. СН2=СН-СН2-СН2-Cl 4-хлор-1-бутен В этом случае галоген не подвергается влиянию
I. Галогенопроизводные винильного типа. Получение 1) Присоединение одной молекулы ННal к ацетиленовым углеводородам. СН хлористый винил СН2=СН-С Cl 1,3-бутадиенин хлорпрен 2) Пиролиз полигалогенопроизводных СН2-СН2 Cl Cl хлористый хлористый этилен винил 3) Действие недостатка спиртового раствора КОН на полигалогенопроизводные Cl Cl СН-СН Cl Cl -HCl тетрахлорэтан трихлорэтилен Особенности свойств 1. Соединения винильного типа проявляют инертность в реакциях нуклеофильного замещения. Причина заключается в особенности электронного строения. Графически это можно показать следующим образом: .. СН2=СН-Cl: .. или
Н Сl C - C p- H H Хлор расположен через одну простую связь от двойной и имеет 3 неподеленных пары электронов. Наблюдается эффект p- 2. Реакции присоединения по двойной связи идут в соответствии с правилом Марковникова, т.к.
СН2=СН этилиденхлорид /+М/</-I/, по p- + + СН3 Более устойчив катион (1), т.к. электродонорная метильная группа частично компенсирует положительный заряд. 3. Очень легко полимеризуются. n СН2=СНCl винилхлорид ПВХ-самые массовые пластмассы Полимеры на основе винилхлорида находят широчайшее применение для изготовления пленок, пластмассовых изделий. Они устойчивы к действию влаги, кислот, щелочей, нефтепродуктов, обладают хорошими электроизоляционными свойствами.
|
||
|
Последнее изменение этой страницы: 2017-01-24; просмотров: 516; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.224.51.27 (0.007 с.) |

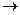 CH4 + HCl
CH4 + HCl C2H6
C2H6 HCl + CH2=CH2
HCl + CH2=CH2
 +///
+/// 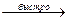 CH2=CH2 + H2o + KCl
CH2=CH2 + H2o + KCl -положении к двойной связи).
-положении к двойной связи). -связи и ведет себя так же, как в предельных галогеноводородах.
-связи и ведет себя так же, как в предельных галогеноводородах. СН + HCl
СН + HCl  HCl + СН2=СН-Cl
HCl + СН2=СН-Cl СНCl=CCl2
СНCl=CCl2 -
-  +..
+..


