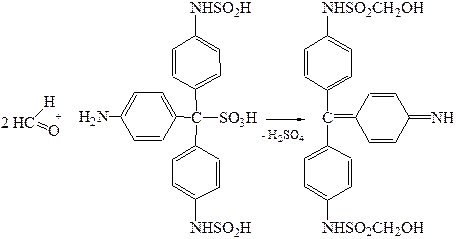Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Количественное определение алкилгалогенидов.Содержание книги
Поиск на нашем сайте
Для количественного определения алкилгалогенидов перегонке с водяным паром подвергается новая порция биологического материала. Существуют несколько методов количественного определения. 1. Метод газожидкостной хроматографии с внутренним стандартом. В качестве внутреннего стандарта используют н-пропанол. 2. Метод обратной йодометрии (хлоралгидрат). 3. Объемный метод. Навеску биологического материала подкисляют винной или щавелевой кислотами и подвергают перегонке с водяным паром. Перегонка считается законченной при отрицательной реакции образования изонитрила. С дистиллятом проводят реакцию отщепления органически связанного хлора. После проведения реакции отгоняют на водяной бане из реакционной смеси этиловый спирт. Охлажденную жидкость подкисляют азотной кислоты до кислой реакции среды (по лакмусу) и проводят аргентометрическое определение галогенидов по Фольгарду. Количественное определение 1,2-дихлорэтана возможно по отщепленному с помощью металлического натрия в присутствии этилового спирта хлору (метод Фольгарда). Определяется около 50% хлора от теоретически вычисленного.
Кислородсодержащие органические соединения. Формальдегид. Формальдегид — газообразное вещество, хорошо растворимо в воде. Формалин — 40% раствор формальдегида в воде, бесцветная прозрачная жидкость с резким удушливым запахом. Смешивается с водой и спиртом во всех отношениях. Формальдегид способен к полимеризации, особенно при хранении в помещениях с температурой ниже 10 0С. При этом образуется полимер формальдегида — параформальдегид или параформ, представляющий собой белый осадок. Параформ - это белый, рыхлый порошок с запахом формальдегида, содержит его не менее 95 %. При нагревании легко переходит в газообразное состояние. Формальдегид используется при изготовлении искусственных смол и пластических масс, при различных синтезах, в красочной и текстильной промышленности, в производстве мыла, для протравливания семян и обработки помещений, тары, инвентаря, транспортных средств, в лабораториях и музеях для сохранения препаратов. В медицинской практике используют 36,5 – 37,5% раствор формальдегида как дезинфицирующее и дезодорирующее средство. Параформ - одно из лучших дезинфицирующих средств, пригодных для дезинфекции как при неспорообразующей, так и при споровой микрофлоре, вирусах и грибах. Для дезинфекции животноводческих помещений применяют 1-4 % растворы по формальдегиду. Токсикологическое значение и метаболизм. Токсикологическое значение формальдегида обусловлено довольно широким его применением. При попадании фрмальдегида с вдыхаемым воздухом (ингаляционные отравления) формальдегид, способен вызывать слезотечениее, раздражение дыхательных путей, характеризующееся резким кашлем, чувство стеснения в груди, одышкой. При вдыхании больших количеств может наступить внезапная смерть в результате отёка и спазма гортани. Кроме того, симптомами отравления формальдегидом являются цианоз, боли, рвота, некроз слизистой. Прием формальдегида внутрь носит, случайный характер (в большинстве случаев ошибочный). В результате всасывания формальдегида наблюдаются потеря сознания, судороги, угнетение нервных центров, раздражение почек. Общетоксическое действие связано с поражением ЦНС: потерей сознания и судорогами. За счет образования в результате метаболизма муравьиной кислоты, наблюдается раздражение печени и почек. Паталогоанатомическая картина при вскрытии - гиперемия слизистой оболочки желудка, острый гастрит, энтерит, при приеме больших количеств формальдегида — ожог, струпья и язвы на слизистой оболочке желудка. Формальдегид выводиться частично из организма в неизменном виде. Основная часть биотрансформируется до метанола и муравьиной кислоты, которая затем превращается в оксида углерода (II) и воду. Смертельной дозой принято считать 10 – 30 г формальдегида. При пероральном поступлении формальдегида, в первые 15 мин пострадавшему необходимо провести промывание желудка 0,1% раствором аммиака или раствором, содержащим 1% карбоната и 2% гидрокарбоната натрия. Кроме того, обеспечить лечение острого разъедающего воспаления пищевода и желудка, острой сердечно-сосудистой и почечной недостаточности. Объектами химико-токсикологического исследования могут являться формалин, жидкости, содержащие его (чай, молоко), и биологический материал: протравленное зерно, внутренние органы трупов (желудок, двенадцатиперстная кишка, и часть тощей кишки с содержимым, головной мозг, печень, почки, моча) и т. д. При значительных количествах формальдегида при перегонке с водяным паром дистиллят обладает характерным удушливым запахом. Границей отгонки при исследовании 100 г трупного материала является 60—65 мг формальдегида (А.А. Васильева). При наличии значительных количеств формальдегида (может иметь место при недопустимом консервировании объектов исследования), необходимо тщательно пересмотреть все материалы дела, и запросить материалы по способу консервирования объектов, а по окончании анализа отметить возможные последствия неправильного консервирования. Для качественного обнаружения формальдегида используют как основной метод газожидкостную хроматографию (ГЖХ), а в качестве подтверждающих - химические методы анализа. 1. Реакция с фуксинсернистой кислотой (реактив Шиффа). Фуксинсернистая кислота известна как реактив Шиффа на альдегиды. Растворимые альдегиды при взаимодействии с реактивом Шиффа окрашивают раствор в синий, сине-фиолетовый или фиолетовый цвет.
Эффект реакции проявляется в течение 15 минут. Появление окраски по истечении 30 минут и более не должно рассматриваться как положительный результат на наличие формальдегида в дистилляте, поскольку появление окраски может быть вызвано влиянием окислителей, содержащихся в воздухе (хлор, окислы азота, кислород и другие окислители), наличием в нем формальдегида или повышением температуры. В сильнокислой среде (концентрированной серной или хлористоводородной кислоте, рН 0,7) в реакцию вступает только формальдегид. В остальных случаях при рН > 2,7 с фуксинсернистой кислотой будут реагировать уксусный альдегид, нитробензальдегид, фурфурол, ацетон. Не дает указанной окраски хлоралгидрат. Реакция позволяет обнаружить 0,03 мкг формальдегида в пробе. 2. Реакции формальдегида с соединениями, имеющими в структуре фенольный гидроксил. Альдегиды способны реагировать с фенолами при нагревании в сернокислой среде с образованием бесцветных продуктов конденсации, при окислении которых получаются интенсивно окрашенные соединения. 2.1. Реакция с резорцином в щелочной среде. Альдегиды реагируют с резорцином в его таутомерной форме (кето-форме) с образованием окрашенного соединения:
При наличии формальдегида появляется малиново-красное или розовое окрашивание. Реакцию проводят с применением контрольного опыта. За счет продуктов окисления резорцина, раствор в контрольном опыте может приобретать желто-зеленый или зеленый цвет. Белковые вещества и продукты их разложения мешают реакции, поэтому ее нельзя проводить (например, для установления факта консервирования формалином) непосредственно с жидкостью, которой залиты внутренние органы трупа, не подвергнув объект предварительной дистилляции с водяным паром. Предел обнаружения - 0,03 мкг в пробе. Реакция не является специфичной, ее могут давать уксусный альдегид, алкилгалогениды, акролеин, фурфурол. Реакция имеет отрицательное значение при СХА.
2.2. Реакция с кодеином (морфином). При взаимодействии формальфегида с кодеином (морфином) в присутствии концентрированной серной кислоты наблюдается синее или сине-фиолетовое окрашивание.
Реакцией обнаруживается до 0,02 мкг вещества в 1 мл раствора. Реакция используется в качестве подтверждающей. 2.3. Реакция с хромотроповой кислотой (1,8-диоксинафталин-3,6—дисульфокислота. Формальдегид реагирует с хромотроповой кислотой в присутствии концентрированной серной кислоты при нагревании до 600С с появлением фиолетовой или красно-фиолетовой окраски.
Предел обнаружения формальдегида 1 мкг в пробе. Не дают этой реакции альдегиды уксусной, пропионовой, масляной кислот, хлоралгидрат и др. Вещества, способные к образованию формальдегида в процессе деструкции или химического взаимодействия способны давать эту реакцию. 2.4. Реакция с салициловой кислотой. В присутствии концентрированной серной кислоты происходит конденсация салициловой кислоты с формальдегидом с образованием метилен-бис-салициловой кислоты, которая окисляется до хиноидной структуры и вступает во взаимодействие с непрореагировавшей салициловой кислотой с образованием ауринового красителя красного цвета.
3. Реакция с реактивом Фелинга При нагревании реактива Фелинга с формальдегидом выпадает красный осадок оксида меди (I) Cu2O.
Реакция неспецифична, ее дают другие альдегиды алифатического ряда, некоторые алкилгалогениды, сахара и др.
4. Реакция восстановления серебра. Формальдегид обладая восстановительными свойствами способен восстанавливать металлическое серебро из аммиачных растворов. При наличии формальдегида аммиачный раствор серебра нитрата образует серебряное «зеркало» или черный осадок: AgNO3 + 2 NH4OH → [Ag(NH3)2]NO3 + 2 H2O
Реакция очень чувствительна. Предел обнаружения формальдегида 0,02 - 0,04 мкг/мл, однако, серебряное «зеркало» может образовываться за счет термического разложения серебра оксида, поэтому реакция не является специфичной.
При обнаружении формальдегида в дистилляте его удаляют из всего объема дистиллята во избежание переоткрытия других «летучих ядов». Дистиллят нагревают с обратным холодильником в присутствии раствора нитрата серебра и гидроксида натрия и перегоняют. При отрицательной реакции части дистиллята после перегонки с фуксинсернистой кислотой, продолжают анализ на «летучие яды».
|
||||
|
Последнее изменение этой страницы: 2016-04-26; просмотров: 1263; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.118.10.75 (0.006 с.) |