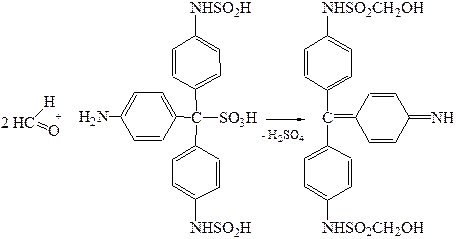Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Изолирование этиленгликоля из внутренних органов (метод Гуляевой)Содержание книги
Поиск на нашем сайте
К 20 г мелко измельченной ткани печени, почки или стенки мочевого пузыря, смесь тщательно перемешивают, прибавляют 20 мл ацетона и настаивают в течение 30 мин. Затем ацетоновое извлечение сливают с объекта исследования, а последний вновь настаивают 30 мин. с новой порцией ацетона (20 мл). Водно-ацетоновые извлечения фильтруют в стаканчик, куда прибавляют 0,5 г активированного угля. Взвесь фильтруют в выпарительную чашку, при этом фильтр промывают несколькими порциями ацетона, которые присоединяют к основному фильтрату, затем фильтрат выпаривают приблизительно до объема 1,0 - 1,5 мл. К остатку прибавляют 15 мл ацетона и, после перемешивания, 10 - 15 г безводного натрия сульфата. Далее поступают как при изолировании этиленгликоля из биологических жидкостей.
Качественный анализ дистиллята на содержание этиленгликоля.
1. Реакция окисления этиленгликоля до формальдегида. К 3 - 5 мл дистиллята прибавляют 5 капель 12 % раствора кислоты серной, 5 капель 5 % раствора калия перйодата в 5 % растворе кислоты серной и взбалтывают. Через 5 мин. прибавляют 3 - 5 капель раствора кислоты серной, а затем 4 капли раствора кислоты фуксинсернистой. При наличии этиленгликоля через 3 - 20 мин появляется красно-фиолетовое или розовое окрашивание.
2. Реакция окисления этиленгликоля до щавелевой кислоты. Часть дистиллята смешивают с концентрированной азотной кислотой и выпаривают досуха. В остатке образуется щавелевая кислота, образующая оксалат кальция при добавлении его солей.
При рассмотрении под микроскопом кристаллы оксалата кальция имеют характерную форму, напоминающую почтовые конверты. 3. Реакция образования гликолята меди. К части анализируемого дистиллята добавляют избыток раствора гидроксида натрия и по каплям раствор сульфата меди – образуется гидроксид меди, который растворяется в присутствии этиленгликоля с образованием раствора, окрашенного в синий цвет.
Реакция образования гликолята меди может быть использована для определения этиленгликоля в технических жидкостях (антифризах, тормозных жидкостях). Еще одним испытанием для определения этиленгликоля в технических жидкостях является его окисление до щавелевой кислоты и дальнейшее определение по реакциям: - образования оксалата кальция; - часть остатка смешивается с концентрированной серной кислотой и нагревается – выделяется оксид углероды (II), горящий голубым пламенем. Реакция возможна при получении достаточного количества щавелевой кислоты; - часть остатка растворяется в воде, подкисляется серной кислотой и добавляется раствор перманганата калия. При нагревании раствор должен обесцвечиваться.
Количественное определение этиленгликоля в диализате проводят методом газожидкостной хроматографии или фотоколориметрическим методом (основа на реакции окисления этиленгликоля до формальдегида, с последующим взаимодействием с фуксинсернистой кислотой).
Тетраэтилсвинец. Прозрачная бесцветная жидкость (Т.кип 195 – 200 0С с разл), с раздражающим запахом. Разбавленные растворы ТЭС имеют приятный фруктовый запах. ТЭС практически нерастворим в воде, легко растворим в бензине, хлороформе, этаноле, диэтиловом эфире и др. органических растворителях. Хорошо растворим в жирах и маслах. ТЭС горит на воздухе с образованием желтовато-белого дыма. Разлагается под влияние температуры, солнечных и УФ- и рентгеновских лучей. Бензин и керосин содержат антидетонатор - этиловую жидкость, которая на 50% состоит из ТЭС. Топливо с добавлением ТЭС называют этилированным и, как правило, оно подкрашено в красный, оранжевый или синий цвет. ТЭС и жидкости его содержащие являются токсичными и вызывают отравление после попадания их с вдыхаемым воздухом или через кожу. В результате отравления происходит расстройство ЦНС (головная боль, возбуждение, бессонница, расстройство зрения, судороги). Летальный исход наступает в течение первых 2 – 5 суток. При отсутствии смертельного исхода, развивается хроническое отравление свинцом. Выделение ТЭС из биологического материала проводят путем перегонки с водяным паром биологических объектов. Дистиллят собирают в приемник и уловитель, в которые вносят по 30 мл насыщенного спиртового раствора йода. Затем проводят повторную перегонку с водяным паром, собирая 50 – 100 мл дистиллята. После окончания перегонки содержимое приемника и уловителя объединяют и оставляют при комнатной температуре на 30 мин. Происходит разложение ТЭС раствором йода.
После отстаивания жидкости, ее переносят в фарфоровую чашку и выпаривают досуха на водяной бане. Остаток растворяют в 50% растворе азотной кислоты, и полученный раствор снова выпаривают досуха.
Сухой остаток, содержащий нитрат свинца, растворяют в воде и исследуют на наличие ионов свинца. Метод позволяет выделить 0,3 мг ТЭС из 100 г биологического материала. Исследование на наличие ТЭС в биологическом объекте проводят сразу же после его поступления. При необнаружении ТЭС в биологическом материале, его подвергают исследованию на наличие продуктов его разложения. С этой целью содержимое колбы, из которой производилась перегонка, вносят в фарфоровую чашку и выпаривают досуха. Оставшийся при этом биологический материал разрушают смесью серной и азотной кислот, а затем минерализат исследуют на наличие ионов свинца. При исследовании пищевых продуктов растительного происхождения и одежды на наличие ТЭС из объектов его изолируют путем настаивания с органическими растворителями.
САМОСТОЯТЕЛЬНАЯ РАБОТА.
|
||||
|
Последнее изменение этой страницы: 2016-04-26; просмотров: 1408; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.119 (0.006 с.) |