
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Rp. : papaverini hydrochloridi 0,3 Natrii nitritis 1,2 Aquae destillatae 180 ml M. D. S. По 1 столовой ложке 2 раза в деньСодержание книги
Поиск на нашем сайте
Выпадает осадок основания папаверина. Раствор окрашивается в желтый цвет, выделяются оксиды азота.
Папаверина основание При сочетании натрия тиосульфата с кислотами выделяется серы диоксид и свободная сера. Na2S2O3 + 2HCl~2NaCI + SO2f + SJ На этой реакции основано лечение чесотки (метод М. П. Демьяновича). Поэтому комбинацию 60% раствора натрия тиосульфата и 6 % раствора кислоты хлороводородной относят к условной несовместимости. Кальция и натрия карбонаты несовместимы с кислотами более сильными, чем угольная. Например: СаСОз + 2НС1-.СаС12 + Н2О + C02f Водорода пероксид неустойчив в щелочной среде, разлагается с выделением кислорода: 2Н2О2-,2Н2О + O2f Поэтому он несовместим со щелочами, карбонатами, боратами и другими веществами, имеющими щелочную реакцию среды. Слабыми основаниями, из солей которых могут выделяться под воздействием щелочей газообразные вещества, являются аммиак и его соединения с формальдегидом — гексаметилентетрамин. Rp.: Acidi ascorbinici 1,2 Solutionis He.xamethylentetramini 3% 180 ml M. D. S. По 1 столовой ложке 3 раза в день Гексаметилентетрамин разлагается с выделением формальдегида. 25.2.4. Окислительно-восстановительные реакции На возможность нежелательных окислительно-восстановительных реакций указывалось при описании технологии водных растворов, пилюль, инъекционных растворов и глазных капель. Водные растворы калия перманганата и серебра нитрата рекомендуется процеживать или фильтровать не через вату или бумагу, а через стеклянные фильтры. При изготовлении пилюль с этими веществами используют в качестве вспомогательных веществ вместо растительных порошков и экстрактов глину белую, бентонит или смесь глины белой и бентонита. Растворы для инъекций и глазные капли с кислотой аскорбиновой, сульфацил-натрием и другими восстановителями стабилизируют антиоксидантами: натрия сульфитом, натрия метабисульфитом и др. Окислительно-восстановительное разложение кислоты аскорбиновой при взаимодействии с эуфилли-ном в порошках рассматривалось выше. Калия перманганат несовместим с большинством органических лекарственных веществ. В кислой среде его окисляющее действие основано на переходе марганца: Мп7+—►Мп2+ (окислительный потенциал+ + 1,52 в). В нейтральном и щелочной средах Мп7+ восстанавливается до Мп4+ с выделением бурого осадка МпОг. .Калия перманганат несовместим с натрия нитритом (окисление в нитрат), кислотой хлороводородной и ее солями (образование свободного хлора), бромидами (окисление до свободного брома), йоди-дами (выделение свободного йода), водорода перок-сидом (выделение кислорода в кислой среде). Он окисляет этанол в альдегид уксусный и кислоту уксусную, глицерин — в смесь муравьиной, пропионовой, тартро-новой и угольной кислот. При растирании калия пер-манганата с серой, глицерином, этанолом, танином, маслами, сахаром, активированным углем и другими органическими веществами может произойти даже взрыв. Водорода пероксид является также сильным окислителем (окислительный потенциал + 1,66 в). Подобно калия перманганату, он несовместим со многими органическими веществами — танином (выделение кислорода), этанолом (медленное окисление в альдегид уксусный и кислоту), веществами щелочного характера. По сравнению с калия перманганатом и водорода пероксидом йод является более слабым окислителем (окислительный потенциал +0,58 в). Йод несовместим с кислотой аскорбиновой (окисление), натрия тиосульфатом (образование натрия тетратионата), аммиаком (образование нерастворимого и взрывчатого йодистого азота), эфирными маслами (возможность вспышки); формальдегидом (окисление до кис-ловд муравьиной). G солями-ртути, серебра и свинца образует труднораетворимые осадки йодидов. С- солями-алкалоидов и-других азотсодержащих органических «веществ' взаимодействует е образованием малорастворимых соединений. Ртути ямидохлорид восстанавливается резорцином/ 'фенолом и*другими восстановителями. Ртути оксид желтый разлагается *д* ртути» металлической на свету или яри растирании с восстановителями. Rp.: Hydrargyri amidochloridi Zinci oxydi aa 2,0 Resorcini Lanolini Vaselini aa 10,0 M. D. S. Для смазывания кожи При растирании ртути амидохлорида, цинка оксида и резорцина с частью расплавленной основы с последующим добавлением остального количества основы мазь вскоре темнеет (образуется ртуть металлическая и продукты окисления резорцина). Окислительно-восстановительную реакцию можно замедлить, если ртути амидохлорид и цинка оксид смешать с частью основы, резорцин — с другой частью основы и обе части осторожно перемешать. Натрия нитрит несовместим с кислотами и веществами, создающими кислую реакцию среды, в том числе солями некоторых алкалоидов, аммония хлоридом и др. (разложение с выделением окислов азота), йоди-дами (выделение йода). Легко окисляются фенолы (фенол, резорцин) и вещества, имеющие фенольные группы (адреналин, натрия салицилат, физостигмина салицилат, танин, морфин, апоморфин и др.). В присутствии веществ с щелочной реакцией среды (натрия тетраборат, сульфацил-натрий, натрия гидрокарбонат и др.) адреналин легко окисляется с изменением окраски раствора от желтой до бурой. Несовместимость кислоты аскорбиновой обусловлена ее свойствами сильного восстановителя и сильной кислоты (рН 1 % раствора 2,6). Она окисляется йодом, цианкобаламином, кислотой фолиевой и др. Кислота аскорбиновая несовместима с гексаметилен-теграмином (разложение гексаметилентетрамина на формальдегид и аммиак), карбонатами (разложение с выделением углерода диоксида), бензоатами и салици-латами (осаждение труднорастворимых бензойной и салициловой кислот), солями барбитуратов и сульфо-намидов (осаждение нерастворимых барбитуратов и сульфонамидов), натрия тиосульфатом и нитритом (разложение этих веществ). Тиамин (витамин Bi) в нейтральных и щелочных растворах несовместим с окислителями. Может раз- лагаться в растворах никотинамидом и кислотой никотиновой; окисление тиамина кислородом воздуха значительно ускоряется в присутствии рибофлавина. Разлагается восстановителями — глюкозой, натрия сульфитом и др. Цианкобаламин (витамин В12) несовместим с окислителями (водорода пероксид, калия перманганат и др.), восстановителями (натрия биосульфит, хлоралгидрат, цистеин и др.), тяжелыми металлами. Легко окисляются также ретинол (витамин А), рибофлавин (витамин Вг), эргокальциферол (витамин D2), токоферола ацетат (витамин Е ацетат). Легко окисляются амидопирин, анальгин. При окислении амидопирина образуются неактивные окрашенные в сине-фиолетовый цвет соединения. Антипирин с натрия нитритом образует в кислой среде нитро-зоантипирин, окрашенный в зеленый цвет. Rp.: Analgini Kalii iodidi aa 1,0 Iodi 0,5 Lanolini Vaselini aa 10,0 M. D. S. Для смазывания руки Мазь быстро обесцвечивается за счет окислительно-восстановительной реакции йода с бисульфитной группой в молекуле анальгина. При этом сера (IV) переходит в серу (VI). Rp.: Kalii permanganatis 3,0 Spiritus aethylici Aquae destillatae aa 30 ml M. D. S. Для смазывания кожи Данная пропись является примером рациональной комбинации, в которой специально предусмотрено взаимодействие компонентов лекарственного препарата. Препарат предложен для лечения эритематозной волчанки. Калия перманганат окисляет этанол: ЗСН3СН2ОН + 2КМпО4------ ► ЗСНзСНО + 2К.ОН + 2МпО2 + 2Н2О ЗСНзСНО + 2КМпО4------ ►гСНзСООК + СНзСООН + 2МпО2 + + н2о с выделением бурого осадка марганца диоксида. Представляет интерес американская компьютерная система по выявлению и предупреждению взаимодействия лекарственных средств на базе аптеки. В памяти компьютера находятся данные о 2000, зафиксировано 1004 комбинации лекарственных средств (потенциально опасных). Если комбинация относится к взаимодействиям первого класса (немедленное проявление, сильная реакция), то фармацевт должен связаться по телефону с врачом. Если взаимодействие относится ко второму классу (отдаленная реакция), то фармацевту следует сделать предупредительную запись и внести предложения по изменению назначения. Эти документы оставляют в рецептурной коробке врача. Примером современного подхода к предупреждению несовместимости является стабилизация порошков, содержащих кислоту ацетилсалициловую, димедрол, кислоту аскорбиновую и кальция лактат («Антигриппин»). В результате взаимодействия кислоты аскорбиновой с димедролом и кальция лактатом порошки при хранении отсыревают и изменяют окраску. При добавлении аэросила порошки пригодны для применения в течение 2 мес. Путем раздельного гранулирования кислоты аскорбиновой и остальных компонентов удалось продлить срок годности «Антигриппина» в форме таблеток до 1 года. Кроме того, целесообразно распространить на все лекарственные формы запрещение изготовления инъекционных растворов при отсутствии данных о химической, совместимости входящих ингредиентов (приказ Минздрава СССР № 582 от 30.04.85 г.). Развитие исследований в области фармацевтиче-t сиен несовместимости связано с углубленным изучением сущности, количественной характеристики и биофармацевтической оценки процессов взаимодействия лекарственных и вспомогательных, веществ. В этих исследованиях должны использоваться современные физико-химические методы анализа (спектрофотомет-рия, различные виды хроматографии и т. д.). Особое внимание следует уделять изучению совместимости многокомпонентных смесей инъекционных растворов, применяемых при интенсивной терапии различных заболеваний. Для преодоления фармацевтической несовместимости необходимо разрабатывать новые способы их преодоления, использовать более эффективные ■стабилизаторы, эмульгаторы, растворители, специальные упаковки и т. д.: Контрольные вопросы 1. Какова сущность понятий: фармацевтическая несовместимость; фармакологическая несовместимость; нерациональные прописи; потенциальная несовместимость?. 2. Какие причины обусловливают возникновение несовместим.ости? 3. Каковы обязанности провизора-технолога при поступлении ре 4. Как классифицируют несовместимость? Приведите примеры 5. В каких случаях нерастворимость лекарственных веществ рас 6. Каким образом можно предотвратить несовместимость, обус 7. Каковы причины отсыревания и расплавления сложных по 8. Каким образом классифицируют химическую несовместимость? 9. Каковы причины образования осадков в жидких лекарствен
10. В каких случаях несовместимость обусловливается выделением 11. Какие факторы влияют на совместимость или несовместимость 12. Какими способами можно предотвратить несовместимость? 13. Каковы основные направления развития исследований в об Глава 26
|
|||||||||||
|
Последнее изменение этой страницы: 2016-12-16; просмотров: 395; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.223.195.30 (0.009 с.) |

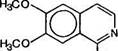
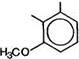
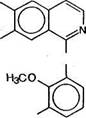 Н3СО
Н3СО


