
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
К полученным осадкам галогенидов свинца(II) добавьте концентрированный раствор гидроксида натрияСодержание книги
Поиск на нашем сайте
- отметить, какие изменения происходят в пробирках ………….
- составить уравнения реакций в молекулярной и ионной форме, учитывая, что растворение галогенидов свинца () происходит в результате образования гидроксокомплексов PbI2 + NaOH →
PbCl2 + NaOH →
- вывод
Опыт 6. Сульфид свинца (II) В две пробирки внести по 2-3 капли раствора соли свинца(II). Прилить в первую пробирку 2-3 капли раствора Na2S, во вторую - 2-3 капли раствора H2S. К образовавшимся осадкам добавить в каждую пробирку раствор соляной кислоты - отметить, какие изменения происходят в пробирках ………….
- составить уравнения реакций в молекулярной и ионной форме Pb(NO3)2 + Na2S →
Pb(NO3)2 + H2S →
- укажите реакцию, которая протекает на «свинцовой индикаторной бумаге», она используется для …………………………. - вывод
Опыт 7. Окислительные свойства соединений свинца (IV) В пробирку поместить одну ложечку порошка PbO2 и 10 капель концентрированного раствора NaOH. Пробирку нагреть на спиртовке. В горячий раствор внести 2 капли раствора Cr2(SO4)3 и снова нагреть пробирку. Отметить появление желтой окраски раствора, характерной для иона CrО42-. Написать уравнение реакции. - отметить, какие изменения происходят в пробирке при нагревании………….
- составить уравнение реакции, учитывая, что образуется хромат натрия и тетрагидросоплюмбат(II) натрия PbO2 + NaOH + Cr2(SO4)3 → Na2CrО4 + Na2[Pb(OH)4]
- как изменилась степень окисления свинца………………хрома………………… - какие свойства проявляет оксид свинца (IV)
- Вывод Опыт 8. Восстановительные свойства соединений олова (II) К 1-2 каплям раствора хлорида олова SnCl2 прилить по каплям раствор щелочи до растворения первоначально образовавшегося осадка. К полученному раствору тетрагидроксостанната(II) натрия прилить 2-3 капли раствора соли висмута (Bi(NO3)3), перемешать. - отметить, какие изменения происходят в пробирке ………….
- составить уравнение реакции, учитывая, что сначала образуется белый осадок Bi(OH)3, затем он чернеет, восстанавливаясь до металлического висмута; олово(II) при этом превращается в гексагидроксостаннат(IV) натрия
SnCl2 + NaOH + Bi(NO3)3 → Bi + Na2[Sn(OH)6] +…
- как изменилась степень окисления олова…………………висмута………………… - какие свойства проявляет олово(II) - вывод
Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования
Уфимский государственный нефтяной технический университет
Кафедра «Общая и аналитическая химия»
Дисциплина «Общая и неорганическая химия»
ОТЧЕТ По лабораторной работе № 8 На тему: «Химические свойства металлов IБ и IIБ- подгрупп Цинк, Медь»
Выполнил студент группы__________ ______________ Фамилия И.О. (Подпись, дата)
Принял доцент кафедры ОАХ ______________ (Подпись, дата) Цель работы: - Изучить свойства металлов IБ и IIБA- подгрупп; - Изучить свойства характеристичных соединений металлов IБ и IIБ- подгрупп; Краткая теория. 1. Положение элементов в периодической системе, свойства атомов Электронные конфигурации атомов, валентные электроны IБ- подгруппа: IIБ- подгруппа: Степени окисления: IБ- подгруппа …………..……..IIБ- подгруппа ……. 2. Свойства простых веществ – металлов: - положение в «ряду стандартных окислительно-восстановительных (электродных) потенциалов металлов» φ(Men+/Me) = - активность металлов: - пассивирование металлов…….. Составьте уравнения реакций: - взаимодействие с кислородом: а) Zn б) Cu - взаимодействие с галогенами (хлором): а) Zn б) Cu - взаимодействие с серой: а) Zn б) Cu
- взаимодействие с водой термодинамически невозможно для металла………….. - взаимодействие с водой для металла………….. термодинамически возможно, однако он устойчив в воде так как…………………….
- взаимодействие с водными растворами кислот, окисляющими H+ (HF, HCl, HBr, HI, разбавленной H2SO4, H3PO4, RCOOH и другими): а) Zn + HBr → б) Ag + HF → а) Zn + H2SO4(разб) → б) Cu + H2SO4(разб) →
- Металл IIБ – подгруппы …………….., который не взаимодействует с водой, так как …………………………………, но вытесняет водород из водного раствора щелочи ……… + NaOH + H2O →
- взаимодействие с концентрированной H2SO4: а) Zn + H2SO4(конц) → ………….+ S + H2O
б) Cu + H2SO4(конц) → ………….+ H2S + H2O
- взаимодействие с разбавленной и концентрированной HNO3: а) Zn + HNO3(разб) → ………….+ N2O + H2O
б) Cu + HNO3(конц) → ………….+ NO2 + H2O
3. Свойства оксидов и гидроксидов металлов IБ и IIБ- подгрупп: - формулы оксидов металлов IБ ………………………и IIБ- подгрупп………………. - формулы гидроксидов металлов IБ ………………………..и IIБ- подгрупп…………… - растворимость, взаимодействие с водой оксидов и гидроксидов металлов IБ и IIБ- подгрупп - диссоциация в водном растворе гидроксида меди (II): - диссоциация в водном растворе гидроксида цинка: [Zn(OH)4]2- + 2H+
Оксиды и гидроксиды меди проявляют ………………………… свойства Оксиды и гидроксиды цинка проявляют ………………………… свойства
Сравните основные свойства оксидов меди и цинка:
- взаимодействие оксидов и гидроксидов металлов IБ и IIБ - подгрупп с кислотами и кислотными оксидами. а) CuО + H2SO4 →
б) Zn(OH)2 + H2SO4 →
- взаимодействие оксидов и гидроксидов металлов IБ и IIБ - подгрупп с основаниями при сплавлении происходит с образованием простых солей (назовите их) и воды ZnO + NaOH → Na2ZnO2 + H2O
Cu(OH)2 + NaOH → Na2CuO2 + H2O
- взаимодействие оксида и гидроксида цинка с водными растворами щелочей происходит с образованием комплексных солей (назовите их): ZnО + NaOH + H2O → Na2[Zn(OH)4]
Zn(OH)2 + NaOH → Na2[Zn(OH)4] 4. Растворимость солей, гидролиз солей Плохо растворимы соли цинка………….
Плохо растворимы соли меди(II)………….
Растворимые сульфат цинка и сульфат меди(II) подвергаются гидролизу по …………….., среда в растворах ……………………. 5. Окислительно-восстановительные свойства соединений металлов IБ и IIБ - подгрупп Соединения цинка окислительно-восстановительных свойств……………………, так как ………… - Используя значения ОВП, приведенных на диаграмме Латимера, охарактеризовать окислительно-восстановительные свойства соединений меди. Диаграмма Латимера для меди:
0,153 +0,521
X = Cl, + 0,538 +0,137
X = Br, + 0,640 + 0,033 X = I, + 0,860 – 0,1852 X = CN,» + 1,2» - 0,43
5. Комплексные соединения металлов IБ и IIБ - подгрупп Катионы металлов IБ и IIБ – подгрупп образуют устойчивые комплексные соединения с аммиаком, цианид-, тиосульфат-, галогенид – ионами. Поэтому оксиды, гидроксиды меди(II) и цинка растворяются в избытке аммиака, в растворе тиосульфата натрия. CuO + 4 NH4OH → [Cu(NH3)4](OH)2 + 3H2O гидроксид тетра аминмеди(II)
6. Термическая устойчивость Гидроксиды меди(I) и меди (II) термически неустойчивы. По этой причине гидроксид меди(I) при комнатной температуре не образуется, а гидроксид меди(II) разлагается при незначительном нагревании на пламени спиртовки на оксид меди(II) и воду. Cu(OH)2 → CuO + H2O
При нагревании разлагаются некоторые соли: карбонаты, нитраты цинка и меди
Взаимодействие металлических цинка и меди с раствором щелочи, соляной кислотой, с концентрированной серной кислотой, азотной кислотой, с раствором аммиака изучено в лабораторной работе «Общие свойства металлов»
|
||||
|
Последнее изменение этой страницы: 2016-07-16; просмотров: 169; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.137.159.163 (0.006 с.) |

 2 H2O + Zn(OH)2
2 H2O + Zn(OH)2 
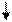
 +0,337
+0,337

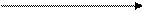
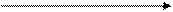 Cu 2+ Cu+ Cu
Cu 2+ Cu+ Cu
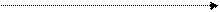 Cu X
Cu X


