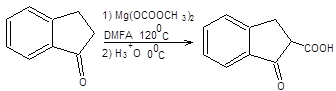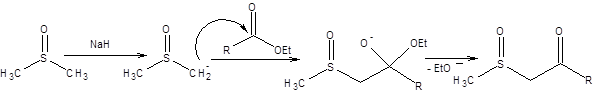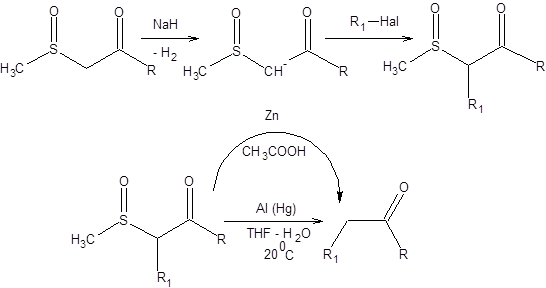Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Синтезы кетонов из ацетоуксусного эфираСодержание книги
Поиск на нашем сайте
Ацетоуксусный эфир является достаточно сильной С–Н-кислотой и нацело депротонируется уже под действием этилата натрия. Повышенная С–Н-кислотность ацетоуксусного эфира связана с делокализацией отрицательного заряда между двумя электроноакцепторными заместителями. Для депротонирования ацетоуксусного эфира используются следующие основания: EtONa, t-BuOK, NaH, KH, LDA:
Схема 7.23
Алкилирование по атому углерода ацетоуксусного эфира с последующим кислотным гидролизом и декарбоксилированием приводят к образованию кетона. Моноалкилированный ацетоуксусный эфир может вторично подвергаться депротонированию с последующим алкилированием и кислотным гидролизом (схема 7.24).
Схема 7.24
Другие возможности использования ацетоуксусного эфира в синтезе кетонов связаны с его способностью образовывать дианион при последовательном депротонировании сильными основаниями.
Схема 7.25
Дианион ацетоуксусного эфира в первую очередь алкилируется по первичному атому углерода как наиболее нуклеофильному, а затем по вторичному. Возможность селективного алкилирования дианиона ацетоуксусного эфира позволяет использовать его как общий предшественник кетонов в органическом синтезе (схема 7.26).
Схема 7.26
Дианион ацетоуксусного эфира можно с успехом применять и для построения циклов (схема 7.27).
Схема 7.27
Применение ацетоуксусного эфира в качестве синтетического предшественника кетонов произвольного строения встречает трудности, связанные с невозможностью эффективно использовать вторичные и особенно третичные алкилирующие реагенты ввиду преобладания продуктов элиминирования. Указанные затруднения могут быть устранены, если алкилированию подвергать не енолят ацетоуксусного эфира, а его енол в условиях катализа кислотами Льюиса (схема 7.28).
Схема 7.28 Ацетоуксусный эфир коммерчески доступен и образуется при самоконденсации этилацетата в присутствии этилата натрия.
Схема 7.28
b-Кетоэфиры, являющиеся производными ацетоуксусного эфира, обладают комплексом схожих свойств. Общим методом синтеза b-кетоэфиров является С-карбоксилирование кетонов, действием диметилкарбоната магния (схема 7.29).
Схема 7.29
Аналогами β-кетоэфиров являются 1,3-кетосульфоксиды, обладающие значительной С–Н-кислотностью и получаемые перекрестной конденсацией сульфоксидов со сложными эфирами (схема 7.30).
Схема 7.30
Высокая С-Н-кислотность 1,3-кетосульфоксидов позволяет депротонировать их сильными основаниями с образованием резонансно стабилизированного карбаниона, который далее подвергается алкилированию по традиционной схеме. 1,3-кетосульфоксиды восстанавливаются до кетонов амальгамой алюминия в воде или цинком в уксусной кислоте, что позволяет получать кетоны различного строения (схема 7.31).
Схема 7.31
|
|||||
|
Последнее изменение этой страницы: 2021-05-27; просмотров: 273; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.222.215.20 (0.007 с.) |

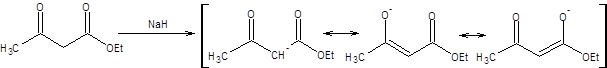
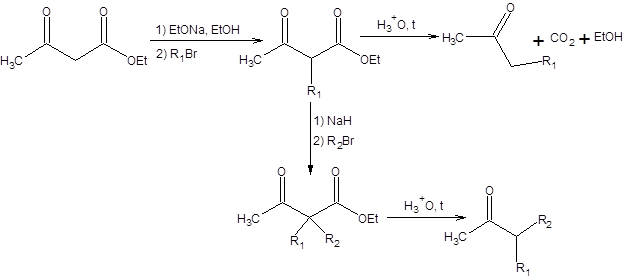
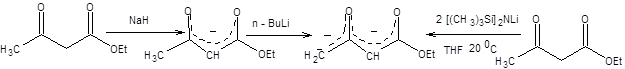
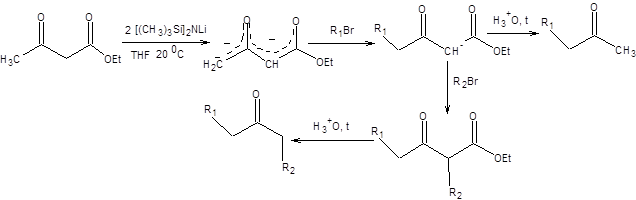
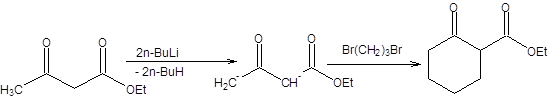
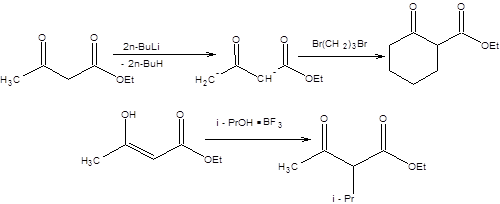
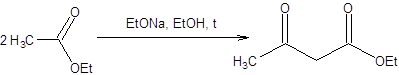
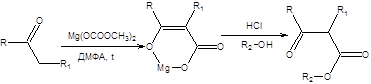 .
.