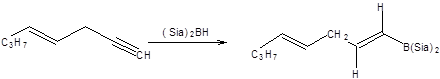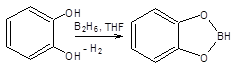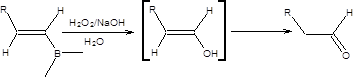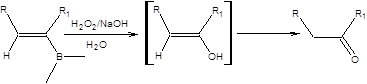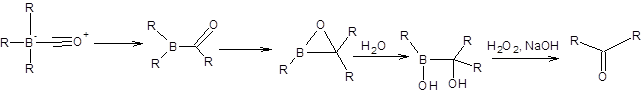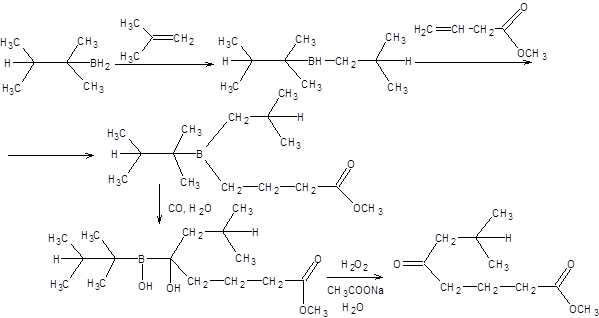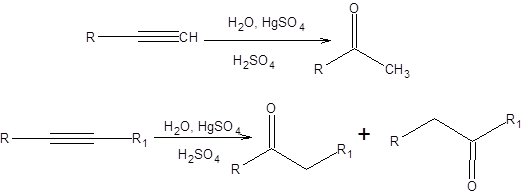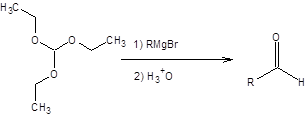Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Синтез карбонильных соединений из боранов
Гидроборирование алкинов диалкилборанами представляет удобный метод синтеза карбонильных соединений [14]. Из диалкилборанов, применяющихся для гидроборирования тройной связи, наибольшее значение имеют коммерчески доступные дисиамилборан и пирокатехинборан. Дисиамилборан присоединяется к алкинам против правила Марковникова и является типичным син-реагентом. Важная особенность дисиамилборана состоит в его способности высокоселективно присоединяться к тройной связи в присутствии двойной связи. Высокой селективностью по отношению к тройной связи также обладает пирокатехинборан, получаемый из пирокатехина и диборана. Пирокатехинборан устойчив на воздухе, удобен в работе и присоединяется к алкинам при небольшом нагревании до 65 – 700С. Примеры синтетического применения дисиамилборана и пирокатехинборана приведены на схеме 6.17.
Схема 6.17
Винилбораны, образующие при гидриоборировании алкинов, расщепляются под действием щелочного раствора пероксида водорода с образованием виниловых спиртов, которые претерпевают перегруппировку Эльтекова, превращаясь в соответствующие карбонильные соединения, как показано на схеме 6.18.
Схема 6.18
Симметричные кетоны также могут быть получены взаимодействием триалкилборанов с монооксидом углерода при нагревании в присутствии воды с последующим окислительным расщеплением, как показано на схеме 6.19.
Схема 6.19
Данный метод пригоден также для получения несимметричных кетонов, если один из трех радикалов триалкилборана предъявляет высокие пространственные требования и неспособен к миграции. В качестве исходного борана в синтезе несимметричных кетонов удобно использовать тексилборан, так как он контролируемо реагирует с алкенами, а тексильный радикал не способен к миграции. Пример синтеза несимметричных кетонов, исходя из тексилборана, представлен на схеме 6.20.
Схема 6.20 Реакция Кучерова
Реакция Кучерова позволяет осуществить превращение алкинов в карбонильные соединения при их взаимодействии с водой в кислой среде в присутствии каталитических количеств солей ртути. При гидратации алкинов более сложного строения, чем ацетилен, образуются кетоны, причем, если возможно образование смеси кетонов, то она образуется. Реакция катализируется ионами ртути и протекает в соответствии с правилом Марковникова (схема 6.21). Роль ионов ртути окончательно не установлена.
Схема 6.21
Осуществление реакции Кучерова требует относительно жестких условий, поэтому она имеет ограниченное значение в современной синтетической практике, несмотря на ее общность для алкинов.
Реакция Бодру – Чичибабина
Реакция Бодру – Чичибабина представляет удобный метод удлинения углеродной цепи на один атом углерода с образованием концевой карбонильной группы. Реакция протекает при взаимодействии реактивов Гриньяра с ортомуравьиным эфиром с образованием ацеталей. Гидролиз ацеталей приводит к образованию альдегидов (схема 6.22).
Схема 6.22
В реакцию Бодру – Чичибабина не вступают литийалкилы, которые депротонируют ортомуравьиный эфир ввиду их чрезмерной основности.
|
|||||
|
Последнее изменение этой страницы: 2021-05-27; просмотров: 110; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.129.22.135 (0.005 с.) |