
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Жидкости. Свойства и особенности молекулярного строения жидкостей.Содержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
Жидкости в этом смысле занимают промежуточное положение между газами и твердыми телами. В частности, для жидкости, как и для кристаллических тел, характерно наличие определённого объёма, и вместе с тем жидкость, подобно газу, принимает форму сосуда, в котором находится. Тем не менее жидкость нельзя рассматривать просто как сильно сжатый газ: количественное различие в плотностях настолько велико, что свойства жидкостей во многом значительно отличаются от свойств газов. В первую очередь это относится к различию в характере теплового движения молекул жидкости и газа. Свойства жидкостей их структура, особенности движения молекул представляют особый интерес для биофизиков и медиков, т.к. биоорганизмы больше, чем на половину состоят из жидкостей. Обмен веществ, снабжение клеток кислородом, выведение из организмов продуктов жизнедеятельности обеспечивается именно перемещением жидкостей. Молекулы в жидкостях находятся значительно ближе друг к другу, чем в газах. По этой причине силы межмолекулярного взаимодействия в жидкости значительно больше, чем в газе. Соответственно поправка р´= а/V2 на добавочное давление в уравнении состояния Ван-дер-Ваальса, как показывает расчёт, очень велика: примерно в 106 раз больше, чем в газах. Например, для воды ван-дер-ваальсово давление равно примерно 11 000 атмосфер. Именно этой огромной величиной молекулярного давления объясняется ничтожно малая сжимаемость жидкостей даже при значительном изменении внешнего давления. Структура жидкостей (их молекулярное строение) характерна тем, что расстояние между частицами является неодинаковым и непостоянным. В расположении молекул и атомов наблюдается ближний порядок. Это означает, что ближайшие соседи каждой молекулы по отношению друг к другу имеют определенную ориентацию и расположение. Однако, по мере удаления от «центра наблюдения» расположение частиц становится все менее упорядоченным и уже на расстояниях 3–4-ёх молекулярных диаметров совершенно исчезает Исключение в этом плане составляют жидкости с удлиненной или дискообразной формой молекул, для которых, при определенных условиях, упорядоченная ориентация частиц наблюдается в пределах значительных объёмов. Такие жидкости получили название жидких кристаллов, т.к. для них, в силу указанной особенности структуры, наблюдается анизотропия механических, оптических, электрических и др. свойств, подобно тому, как это имеет место в кристаллах. Тепловое движение частиц жидкости, по теории Я. И. Френкеля, представляет собой периодические колебания, со средней частотой ν0 ~1012 с-1, которые чередуются с нерегулярными переходами, «скачками», частиц с места на место. При этом частица перемещается на расстояние δ ~ 10-8 – 10-10 м, равное среднему расстоянию между молекулами. Т.к. среднее расстояние между молекулами того же порядка, что и их размеры, то перемещение частиц по объёму жидкости крайне затруднено. Среднее время τ пребывания молекул на одном месте, время «оседлой жизни» (время релаксации), связано со средним периодом τ0 их колебаний быстро убывает с ростом температуры:
где Еа – энергия активации: энергия, которую должна приобрести молекула для разрыва молекулярных связей со своими соседями при смене места; k – постоянная Больцмана. Среднее значение скорости поступательного движения молекул жидкости при «скачках»: В случае несферической формы молекулы жидкости могут совершать кроме колебаний также вращательное и вращательно-колебательное движения. Такая структура жидкостей и характер поведения её молекул обеспечивает сильно выраженную самодиффузию частиц жидкости и её основное свойство – текучесть. Вместе с тем, жидкости практически несжимаемы и сохраняют свой объем подобно твердым телам. Сближает жидкости способны сопротивляться растяжению. По сравнению с газами жидкости обладают значительным коэффициентом теплового расширения. Значения коэффициентов объёмного расширения при постоянном давлении (p = const):
приведены в таблице (Яковлев стр. 213). Молярные теплоёмкости Ср и СV для жидкостей тоже существенно отличаются от соответствующих значений для их паров. Интересно отметить, что для жидкостей не выполняется уравнение Майера: Ср – СV = R. В тоже время из теории известно, что значения γ = Ср /СV для жидкостей примерно такие же, как и у газов.
Реальные жидкости. Вязкость. Сила внутреннего трения (закон Ньютона). Ньютоновские и неньютоновские жидкости Законы, описывающие диффузию, теплопередачу и внутреннее трение в жидкостях по своей математической форме аналогичны соответствующим законом для газов. Однако коэффициенты переноса отличаются от газовых, как по значениям, так и по своему содержанию. Так в уравнении Фика, которое описывает перенос массы: коэффициент диффузии для химически однородных жидкостей:
где δ – среднее перемещение молекул, τ0 – средний период колебаний молекул. Коэффициент диффузии быстро возрастает с ростом температуры, главным образом за счёт уменьшения времени релаксации τ. В целом, при температурах Т << Тк значения коэффициентов диффузии для жидкостей на 4÷5 порядков меньше, чем для газов при тех же условиях. Процесс теплопереноса в жидкостях описывается уравнением Фурье:
В отличие от газов перенос энергии в жидкостях определяется передачей от молекулы к молекуле энергии колебательного, а не поступательного движения. В области повышенной температуры амплитуда колебаний более высокая, чем в соседних областях. Взаимодействие частиц приводит к постепенному возрастанию амплитуд колебаний в областях с более низкой температурой и распространению этого явления по всему объёму жидкости. Коэффициент теплопередачи χ для жидкостей примерно в 100 раз больше, чем для газов. В реальной жидкости между молекулами действуют силы взаимного притяжения, обуславливающие внутреннее трение или вязкость. Это свойство проявляется в том, что при перемещении одних слоев жидкости относительно других, появляются силы, которые препятствуют этому перемещению. В результате, скорость медленно движущихся слоёв возрастает, а быстрых уменьшается. Вязкость вызывает силу сопротивления при перемешивании жидкостей, замедляет скорость движения твёрдых тел в жидкости и т.д. Сила внутреннего трения между двумя слоями жидкости в случае ламинарного течения определяется законом Ньютона: Здесь: du/d х – поперечный градиент скорости; S – площадь соприкосновения трущихся слоев; η – динамический коэффициент вязкости или просто вязкость. [η] = Па·с (паскаль∙секунда). Коэффициент вязкости η для жидкостей сильно зависит от температуры и давления. В целом вязкость жидкости, как установил Я. И. Френкель, пропорциональна времени релаксации (η ~ А. И. Бачинский экспериментально установил закон зависимости вязкости жидкости от её молярного объёма:
где Vμ – молярный объём жидкости; b – константа в уравнении Ван-дер-Ваальса, С – постоянная, зависящая от природы жидкости. Для большинства жидкостей (вода, низкомолекулярные органи-ческие соединения, истинные растворы, расплавы металлов и их солей) вязкость зависит только от природы жидкости и ее температуры. Такие жидкости называются ньютоновскими. Коэффициент вязкости для них можно рассчитать из формулы (6) или (7). У некоторых жидкостей (кровь, растворы полимеров, суспензии, эмульсии) коэффициент вязкости зависит от режима течения: давления р и значения градиента скорости du/d x. При их увеличении вязкость уменьшается вследствие нарушения внутренней структуры потока. Такие жидкости называется структурно вязкими или неньютоновскими. Для них коэффициент вязкости является функцией градиента скорости и давления.
|
||||
|
Последнее изменение этой страницы: 2016-12-12; просмотров: 1690; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.17.174.204 (0.009 с.) |

 , (1)
, (1) ~ 40 м/с, что примерно в 20 раз меньшие, чем для газа при той же температуре.
~ 40 м/с, что примерно в 20 раз меньшие, чем для газа при той же температуре. (2)
(2)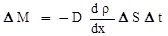 , (3)
, (3) , (4)
, (4) . (5)
. (5) . (6)
. (6) ), которое уменьшается с ростом температуры. Т.е. при нагревании жидкостей их текучесть должна возрастать, что подтверждается опытом. Это связано с возрастанием среднего расстояния между молекулами и, следовательно, ослаблением взаимодействия между ними.
), которое уменьшается с ростом температуры. Т.е. при нагревании жидкостей их текучесть должна возрастать, что подтверждается опытом. Это связано с возрастанием среднего расстояния между молекулами и, следовательно, ослаблением взаимодействия между ними.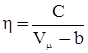 , (7)
, (7)


