Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Методика приготовления гидрозоля гндрокснда железаСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
Гидрозоль гидроксида железа готовят методом химической конденсации, происходящей в результате гидролиза хлорида железа согласно реакции: FeCl3 + З Н2O Равновесие реакции сдвигается вправо при повышении температуры и разведении реакционной смеси. Для получения золя в колбу с 250 мл кипящей дистиллированной воды доливают 10 мл 2% раствора хлорида железа и кипятят несколько минут. При этом получается гидрозоль красно-коричневого цвета. Приготовленный гидрозоль охлаждают до комнатной температуры.
Ход работы:
За процессом коагуляции следят по изменению оптической плотности D, которую измеряют на приборе ФЭК-56. Для изучения коагуляции золя гидроксида железа предварительно проводят следующие операции: берут 11 пробирок, нумеруют их и наливают воду в количестве, указанном в таблице 6.2. Затем в каждую пробирку добавляют по 10 мл золя.
Таблица 6.2 – Результаты изучения процесса коагуляции гидрозоля железа Электролит................................ (название, концентрация)
Далее в каждую пробирку вносят растворы хлорида или ацетата натрия в таком количестве, чтобы общий объем смеси в каждой пробирке составлял 15 мл (см. таблицу 6.2). По часам отмечают время внесения электролита в золь. Измерения на ФЭК-56 проводят с раствором хлорида натрия не ранее, чем через 30 минут, а с раствором ацетата натрия – через 15 минут. Сульфат натрия вносят в золь гидроксида железа за 2 минуты до проведения измерений. Результаты проведенных измерений заносят в таблицу 6.2. Такую таблицу составляют для каждого электролита отдельно, т.е., в результате работы всего должны быть составлены и заполнены 3 таблицы. С целью экономии времени первыми следует приготовить пробирки с раствором хлорида натрия, затем – с раствором ацетата натрия. При проведении опыта необходимо следить за временем. Прежде, чем залить в кювету исследуемый раствор для измерения оптической плотности, кювету следует предварительно ополоснуть этим раствором. Вычисление концентрации раствора электролита в системе, содержащей электролит, проводят по соотношению объема и молярности исходной и конечной системы по формуле:
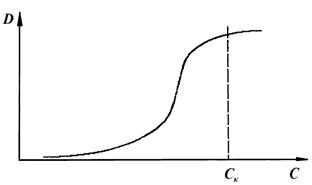
Например, для 5-ой пробирки с ацетатом натрия; 3×2 = С к×15, т.е. C к = 0,4 моль / л. На основании результатов строят зависимость D = f (C), которая должна иметь примерно такой вид, как показано на рисунке 6.6. По этой зависимости устанавливают порог коагуляции С к. На основании полученных результатов записывают формулу мицеллы золя гидроксида железа и объясняют влияние природы иона на коагуляцию.
Рисунок 6.6 – Зависимость оптической плотности золя от концентрации электролита
Лабораторная работа 6.3
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-12-10; просмотров: 586; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.118.226.167 (0.008 с.) |

 Fe(OH)3 + 3 HCl.
Fe(OH)3 + 3 HCl. .
.