Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Противоатеросклеротические средства, классификация. Статины, механизм действия, показания, побоичные эффекты.Содержание книги
Поиск на нашем сайте Для снижения риска прогрессирования атеросклероза необходимо использовать лекарственные средства, снижающие в плазме крови уровень атерогенных и повышающих уровень антиатерогенных липопротеинов. Антигиперлипопротеинемические (гиполипидемические) средства, с помощью которых возможна коррекция липидного обмена при атеросклерозе, классифицируются следующим образом: - ингибиторы З-гидрокси-3-метилглутарил-коэнзим А-редуктазы (статины); - секвестранты желчных кислот; - препараты никотиновой кислоты; - производные фиброевой кислоты (фибраты). ИНГИБИТОРЫ 3-ГИДРОКСИ-З-МЕТИЛГЛУТАРИЛ-КОЭНЗИМ А-РЕДУКТАЗЫ (СТАТИНЫ) Ловастатин (Мевакор), симвастатин (Зокор), правастатин (Ли-постат), флувастатин (Лескол), аторвастатин (Липримар) Статины обладают высокой гиполипидемической активностью и представляют одну из наиболее перспективных групп лекарственных средств в профилактике и лечении атеросклероза. Препараты обратимо ингибируют З-гидрокси-3-ме-тилглутарил-коэнзим А-редуктазу (ГМГ-КоА-редуктаза), ключевой фермент синтеза ХС на этапе образования мевалоновой кислоты. В результате содержание ХС в печени уменьшается, а количество рецепторов ЛПНП на гепатоцитахкомпенсаторно увеличивается, что приводит к снижению содержания ЛПНП плазмы крови за счет увеличения рецептор-зависимогоэндоцитоза ЛПНП. Кроме того, статины способны незначительно уменьшать уровни ЛППП и ЛПОНП и несколько повышать уровень ЛПВП в плазме крови. Ловастатин получают из грибка Aspergillusterreus, а симвастатин и правастатин являются химическими производными ловастатина. Эти статины в своей химической структуре имеют гидронафталеновое кольцо, которое вступает во взаимодействие с ферментом ГМГ-КоА-редуктазой, а также эти соединения имеют оксикислоту в боковой цепи, которая придает сходство с мевалонатом. Ловастатин и симвастатин являются пролекарствами, так как они представляют собой неактивные лактоны, которые предварительно должны гидролизоваться в р-оксикислоты, чтобы стать фармакологически активными соединениями. Флувастатин является синтезированным ингибитором ГМГ-Ко А-редуктазы и по химической структуре отличается от первых трех, так как является производным мевалонолактона, имеет в своей структуре фторфенилиндольную часть, что делает его похожим на коэнзим А, а также имеет боковую цепь, схожую с мевалонатом. Правастатин и флувастатин содержат в своей химической структуре оксикислоты и поэтому они фармакологически активны в исходном состоянии. Основным показанием для статинов является гиперлипопротеинемияИа типа (повышенный уровень ЛПНП). Препараты назначают внутрь 1 раз в сутки. Биодоступностьстатинов при введении внутрь невелика, наиболее низкая у ловаста-тина и симвастатина - меньше 5%, у правастатина - 18% и флувастатина около 24%. Низкая биодоступностьстатинов связана с тем, что они метаболизируются при первом прохождении через печень. Взаимодействие статинов с пищей происходит по-разному. Так, биодоступностьловастатина возрастает, если препарат принимается после еды; биодоступностьсимвастатина не изменяется от приема пищи; а биодоступностьправастатина и флувастатина уменьшается, если препараты приняты после еды. Максимальная концентрация в крови ловастатина и симвастатина достигается через 2-4 ч соответственно, а правастатина и флувастатина - через 0,71-1,5 ч и 0,5 ч соответственно. Через гематоэнцефалический барьер хорошо проникаю! липофильные соединения, такие как ловастатин, а флувастатин и правастатин практически не проходят через этот барьер. Препараты обычно применяются длительно (в течение нескольких месяцев).переносятся относительно хорошо. Побочные эффекты: диспептические расстройства, бессонница, головная боль, эритема кожи, сыпь. Зависимый от дозы побочный эффект — гепатотоксичность (с повышением уровня трансаминаз или без него) — могут вызывать все препараты группы статинов. Характерный и наиболее тяжелый побочный эффект для всех препаратов — миопатия. Противовирусные средства. Классификация. Противовирусные угнетающие абсорбцию вируса, процесс высвобождения вирусного генома. ЛИБО: Гамма-глобулин, Мидантан, Ремантадин. Противогриппозные средства. Классификация. Арбидол, Кагоцел, Рибавирин. Показания, побоичные действия. Процесс репликации вируса протекает в несколько этапов. Он начинается с фиксации (адсорбции) вируса к специфическим рецепторам клеточной стенки. Затем начинается проникновение (виропексис) вирионов внутрь клетки хозяина. Клетка путем эндоцитоза захватывает прикрепленные к ее оболочке вирусы внутрь. После растворения лизосомальными ферментами вирусной оболочки освобождается нуклеиновая кислота (депротеинизация вируса), которая проникает в ядро клетки и начинает управлять процессом размножения вируса. Сначала она заставляет клетку синтезировать так называемые «ранние» белки-ферменты, необходимые для синтеза нуклеиновых кислот дочерних вирусных частиц. Затем происходит синтез вирусной нуклеиновой кислоты. Следующим этапом является синтез «поздних» или структурных белков с последующей сборкой вирусной частицы. Последний этап взаимодействия вируса и клетки заключается в выходе зрелых вирионов во внешнюю среду. Классификацияпротивовирусныхсредств
Гамма-глобулин (иммуноглобулин G) содержит специфические антитела к поверхностным антигенам вируса. Препарат вводится внутримышечно 1 раз в 2-3 нед для профилактики гриппа, кори в период эпидемии. Другой препарат человеческого иммуноглобулина G — Сандоглобулин — вводится внутривенно 1 раз в месяц по тем же показаниям. При применении препаратов возможно развитие аллергических реакций. Римантадин (Ремантадин) иАмантадин (Мидантан) являются трицик-лическими симметричными адамантанаминами. Применяют препараты с целью раннего лечения и профилактики гриппа типа А2 (азиатский грипп). Назначают внутрь. К наиболее выраженным побочным эффектам препаратов относятся: бессонница, нарушения речи, атаксия и другие нарушения центральной нервной системы. Рибавирин (Виразол, Рибамидил) — синтетический аналог гуанозина. В организме препарат фосфорилируется, превращаясь в моно- и трифосфат. Моно- фосфат рибавирина является конкурентным ингибитором инозинмонофосфатдегидрогеназы, что приводит к угнетению синтеза гуаниновых нуклеотидов, а три-фосфат ингибирует вирусную РНК-полимеразу и нарушает образование мРНК. В результате подавляется репликация как РНК-, так и ДНК-содержащих вирусов. Рибавирин применяется при гриппе типа А и В, герпесе, гепатите А, гепатите В в острой форме, кори, а также инфекциях, вызванных респираторно-синтици-альным вирусом. Препарат применяется внутрь и ингаляционно. При применении препарата возможны бронхоспазм, брадикардия, остановка дыхания (при ингаляциях). Кроме того, отмечаются кожные сыпи, конъюнктивит, тошнота, боли в животе. Рибавирин оказывает тератогенное и мутагенное действие.
МИДАНТАН: Действующее вещество (МНН) Амантадин* (Amantadine*) Применение: Болезнь Паркинсона, паркинсонизм (ригидные и акинетические формы); невралгия при опоясывающем лишае; потеря сознания в результате черепно-мозговой травмы; замедленный выход из наркоза; химиопрофилактика и лечение гриппа (вируса гриппа А). Противопоказания: Гиперчувствительность, психоз, эпилепсия, тиреотоксикоз, глаукома, аденома предстательной железы, печеночная и/или почечная недостаточность, беременность (особенно I триместр), грудное вскармливание. Ограничения к применению: Застойная сердечная недостаточность, гипотензия, психомоторное возбуждение, спутанность сознания, галлюцинации, заболевания печени и почек. Побочные действия: Со стороны нервной системы и органов чувств: головокружение, инсомния, тревожность, раздражительность, снижение остроты зрения, возбуждение, тремор, судороги, зрительные галлюцинации. Со стороны сердечно-сосудистой системы и крови (кроветворение, гемостаз): сердечная недостаточность, тахикардия. Со стороны органов ЖКТ: анорексия, тошнота, сухость во рту, диспепсия. Римантадин: Противовирусное средство, производное адамантана; эффективно в отношении различных штаммов вируса гриппа А, вирусов Herpessimplex типа I и II, вирусов клещевого энцефалита (центрально-европейского и российского весенне-летнего из группы арбовирусов сем. Flaviviridae). Оказывает антитоксическое и иммуномодулирующее действие. Полимерная структура обеспечивает длительную циркуляцию римантадина в организме, что позволяет применять его не только с лечебной, но и с профилактической целью. Подавляет раннюю стадию специфической репродукции (после проникновения вируса в клетку и до начальной транскрипции РНК); индуцирует выработку интерферонов альфа и гамма, увеличивает функциональную активность лимфоцитов - естественных киллеров (NK-клеток), T- и B-лимфоцитов. Являясь слабым основанием, повышает pHэндосом, имеющих мембрану вакуолей и окружающих вирусные частицы после их проникновения в клетку. Предотвращение ацидификации в этих вакуолях блокирует слияние вирусной оболочки с мембраной эндосомы, предотвращая т.о. передачу вирусного генетического материала в цитоплазму клетки. Побочные действия: Со стороны ЦНС: снижение способности к концентрации внимания, бессонница, головокружение, головная боль, нервозность, чрезмерная утомляемость. Со стороны пищеварительной системы: сухость во рту, анорексия, тошнота, гастралгия, рвота. Кагоцел: Противовирусное средство. Индуцирует продукцию позднего интерферона (смесь альфа- и бета-интерферонов, обладающих высокой противовирусной активностью) во всех популяциях клеток, принимающих участие в противовирусном ответе организма: Т- и В-лимфоциты, макрофаги, гранулоциты, фибробласты, эндотелиальные клетки. При приеме внутрь одной дозы титр интерферона в сыворотке крови достигает максимума через 48 ч. Показания: Грипп, ОРВИ, герпес. Гиперчувствительность, беременность. Аллергические реакции. Арбидол: Противовирусное средство, оказывает иммуномодулирующее и противогриппозное действие, специфически подавляет вирусы гриппа А и В. Обладает интерферониндуцирующими свойствами, стимулирует гуморальные и клеточные реакции иммунитета, фагоцитарную функцию макрофагов, повышает устойчивость организма к вирусным инфекциям. Предупреждает развитие постгриппозных осложнений, снижает частоту обострений хронических заболеваний, нормализует иммунологические показатели. Противовирусное действие обусловлено подавлением слияния липидной оболочки вируса с клеточными мембранами при контакте вируса с клеткой. Терапевтическая эффективность при гриппе проявляется в снижении интоксикации и выраженности катаральных явлений, укорочении периодов лихорадки и общей продолжительности заболевания. Относится к мало токсичным ЛС (LD50>4 г/кг). Не оказывает какого-либо отрицательного воздействия на организм человека при пероральном применении в рекомендуемых дозах. Профилактика и лечение у взрослых и детей: грипп А и В, ОРВИ (в т.ч. осложненные бронхитом, пневмонией); вторичные иммунодефицитные состояния. Комплексная терапия хронического бронхита, пневмонии и рецидивирующей герпетической инфекции. Профилактика послеоперационых инфекционных осложнений и нормализация иммунного статуса у взрослых. Гиперчувствительность, детский возраст (до 2 лет). Аллергические реакции. Классификация противогриппозных средств:
Билет 14. 1. Фармакокинетика лекарственных препаратов, основные кинетические параметры и их значение для фармакотерапии. Период полувыведения (Т1/2), площадь под кинетической кривой (AUC), кажущийся объем распределения (Vd), константа скорости элиминации (Kel), клиренс (Сl). Фармакокине́тика (греч. pharmakon лекарство kinētikosотносящийся к движению) Раздел фармакологии, изучающий закономерности всасывания, распределения, метаболизма и выделения лекарственных средств. Исследование этих закономерностей основано на математическом моделировании указанных процессов. Определение фармакокинетических характеристик новых лекарственных веществ является важной частью их доклинического и клинического испытания. Период полувыведения (T1/2) — время, в течение которого концентрация препарата в организме снижается на 50 %. Некоторые лекарства имеют очень короткие периоды полувыведения. Для двух простых таблеток аспирина или ибупрофена период полувыведения — приблизительно 4 часа. Но некоторые нестероидные противовоспалительные препараты, такие как пироксикам имеют период полувыведения приблизительно 24 часа. Препарат золота (средство для базисной терапии ревматоидного артрита), введенный в мышцу, имеет период полувыведения 3-4 месяца. Для внесосудистых или энтеральных введений биодоступность ЛС оценивается сравнением площадей подкинетическими кривыми изменениями концентрации, а значения клиренса вычисляются по ранее приведенным уравнениям, поскольку все остальные величины - доза, интервал и другие известны или оцениваются непосредственно по площади под кинетической кривой (степени биодоступности), равновесной концентрации и др.), т. о. Площадь под кинетической кривой – зависимость концентрации от времени.
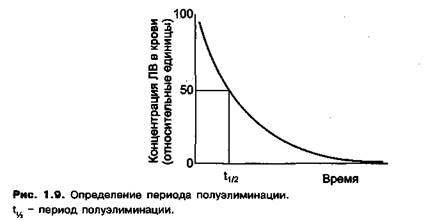
Кажущийся объем распределения - гипотетический объем жидкости организма, в котором лекарственное вещество распределено равномерно и при этом находится в концентрации, равной концентрации данного вещества в плазме крови (С). Соответственно, кажущийся объем распределения Vd = Q/C где Q — количество вещества в организме при концентрации в плазме крови С. Если допустить, что вещество после внутривенного введения в дозе D мгновенно и равномерно распределилось в организме, то кажущийся объем распределения Vd = D/C0, где С0 - начальная концентрация вещества в плазме крови. Кажущийся объем распределения позволяет судить о том, в каком соотношении распределяется вещество между жидкостями организма (плазмой крови, интерстициальной, внутриклеточной жидкостями). Константа скорости элиминации 1-го порядка показывает, какая часть вещества элиминируется из организма в единицу времени (размерность мин-1, ч-1). Например, если keI какого-либо вещества, которое ввели внутривенно в дозе 100 мг, составляет 0,1 ч~', то через 1 ч количество вещества в крови будет равно 90 мг, а через 2 ч - 81 мг и т.д. Немногие лекарственные вещества (этанол, фенитоин) элиминируются в соответствии с кинетикой нулевого порядка. Скорость такой элиминации не зависит от концентрации вещества и является постоянной величиной, т.е. в единицу времени элиминируется определенное количество вещества (например, за 1 ч элиминируется 10 г чистого этанола). Связано это с тем, что при терапевтических концентрациях названных веществ в крови происходит насыщение ферментов, метаболизирующих эти вещества. Поэтому при увеличении концентрации таких веществ в крови скорость их элиминации не повышается. Период полуэлиминации (tI/2, half-life) - время, за которое концентрация вещества в плазме крови снижается на 50%. Для большинства ЛВ (для тех, элиминация которых подчиняется кинетике 1-го порядка) период полуэлиминации - величина постоянная в определенных пределах и не зависит от дозы ЛВ. Поэтому, если за один период полуэлиминации из плазмы крови удаляется 50% внутривенно введенного ЛВ, то за 2 периода — 75%, а за 3,3 периода - 90% (этот параметр используют для подбора интервалов между введениями вещества, необходимых для поддержания его постоянной концентрации в крови).
Период полуэлиминации связан с константой скорости элиминации следующим соотношением: t1/2 = ln2/keI = 0,693/kel. Если сразу же после внутривенного введения вещества производить измерения его концентрации в плазме крови через короткие интервалы времени, то можно получить двухфазный характер изменения концентрации вещества в крови. Клиренс — фармакокинетический параметр, который характеризует скорость освобождения организма от лекарственного вещества. Поскольку освобождение организма от ЛВ происходит за счет процессов биотрансформации (метаболизма) и экскреции, различают метаболический и экскреторный клиренс. Метаболический клиренс (Clmet) и экскреторный клиренс (Сехсг) в сумме составляют системный (общий) клиренс (Clt, totalclearance): Clmet + С excr = Clt Системный клиренс численно равен объему распределения, который освобождается от вещества в единицу времени (размерность — объем в единицу времени, например, мл/мин, л/ч, иногда с учетом массы тела, например, мл/кг/мин): CLt= Vdkel 2. Средства для ингаляционного наркоза – галотан (фторотан), динитроген оксид (закись азота), энфлуран, севофлуран (севоран), эфир для наркоза. Стадии наркоза, сравнительная характеристика препаратов. Показания к использованию, возможные осложнения и их коррекция. Средства для ингаляционного наркоза: Летучие жидкости:
|
|||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-08-26; просмотров: 1037; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.62 (0.01 с.) |