
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Основные химические свойства алкановСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте Пример решения задачи 1 I. Приведите формулу соединения метилдиизопропилметан. Назовите данное соединение по систематической номенклатуре. Сколько одновалентных (первичных, вторичных, третичных) радикалов можно построить для этого соединения?
Решение Метилдиизопропилметан – название дано по рациональной номенклатуре/ 1. Строим основу соединения метан:
2. С основой связано три алкильных заместителя: метил и два изопропила. Присоединяем их к основе:
3. К свободной связи добавляем атом водорода:
4. Назовем полученное соединение по систематической номенклатуре: а) выбираем наиболее длинную углеродную цепь, которая включает пять атомов углерода. Называем алкан, соответствующий главной цепи - пентан; б) нумеруем углеродную цепь со стороны, где ближе разветвление:
в) перечисляем алкильные заместители, связанные с главной цепью, с указанием номеров (локантов) атомов углерода, при которых они находятся. Одинаковые заместители называем с использованием умножающей приставки три -: 2,3,4-триметилпентан. 5. определяем, сколько углеводородных радикалов можно построить для данного соединения: а) в данном соединении имеется пять первичных атомов углерода, четыре из которых эквивалентны - образуют один и тот же радикал (один), пятый первичный атом углерода не является эквивалентным остальным и образует второй радикал. Следовательно, для данной молекулы можно построить два первичных радикала:
б) в молекуле имеется еще три третичных атома углерода, два из которых эквивалентны и образуют один третичный радикал; третий третичный углерод - второй третичный радикал. Следовательно, для данной молекулы можно построить два третичных радикала:
Вывод. Для метилдиизопропилметана можно построить четыре различных углеводородных радикала: два первичных и два третичных.
II. Приведите формулу соединения 2-фенилбут-1-ен. Назовите его по рациональной номенклатуре. Для данного соединения приведите формулу структурного изомера, отличающегося положением кратной связи. 1. Строим углеродный скелет, который соответствует алкану главной цепи - бутану, и нумеруем атомы углерода:
2. При С-2 ставим заместитель фенил, а после С-1, так как соединение является алкеном, размещаем двойную связь. И добавляем атомы водорода:
3. Называем соединение по рациональной номенклатуре: выделяем основу, характерную для алкенов, - этилен. Перечисляем окружающие основу углеводородные заместители в порядке возрастания их старшинства: этил, фенил. Так как эти заместители находятся при одном атоме углерода основы, то в название добавляем приставку несим. (несимметричный).
Соединение называется: несим. этилфенилэтилен.
4. Для данного соединения приводим формулу структурного изомера, отличающегося положением кратной связи. Двойную связь можно поставить при С-2 или при С-3. Например:
III. Назовите соединение по рациональной и систематической номенклатуре.
1. Данное вещество относится к классу алкадиенов. За основу выбирается этилен, связанный с большим числом заместителей.
Называем окружающие основу заместители в порядке увеличения старшинства (см. табл. 2): изобутил, винил. Так как эти заместители находятся при разных атомах углерода основы, то в название добавляем приставку сим. (симметричный). Соединение называется: сим. изобутилвинилэтилен.
2. Называем полученное соединение по систематической номенклатуре: а) выбираем наиболее длинную углеродную цепь, которая включает семь атомов углерода (гептан), и нумеруем ее со стороны, где ближе находится двойная связь:
б) указываем алкильный заместитель (метил), связанный с главной цепью, и номер атома углерода (С-6), при котором он находится. в) называем углеродную цепь соответствующим алканом, заменяя суффикс - ан на – диен, с указанием номеров атомов углерода, при которых находятся двойные связи. Название соединения: 6-метилгепта-1,3-диен. Пример решения задачи 2 I. Приведите формулу соединения этилпропил- втор -бутилкарбинол. Назовите его по систематической номенклатуре. Для данного соединения приведите формулу структурного изомера, отличающегося положением функциональной группы. Решение Этилпропил- втор -бутилкарбинол – название дано по рациональной номенклатуре. 1. Строим основу соединения карбинол:
С основой связано три алкильных заместителя: этил, пропил и втор - бутил. Присоединяем их к основе:
2. Называем полученное соединение по систематической номенклатуре: а) выбираем наиболее длинную углеродную цепь, которая включает семь атомов углерода (гептан). Положение гидроксильной группы одинаковое с обеих сторон углеродной цепи, поэтому нумерацию начинаем с той стороны, где ближе разветвление:
б) перечисляем алкильные заместители, связанные с главной цепью в алфавитном порядке с указанием номеров атомов углерода, при которых они находятся; в) называем углеродную цепь соответствующим алканом, добавляя суффикс – ол, с указанием номера атома углерода, при котором находится гидроксильная группа. Название соединения: 3-метил-4-этилгептан-4-ол. 3. Для данного соединения приводим формулу структурного изомера, отличающегося положением функциональной группы:
II. Приведите формулу соединения 2-изопропил-2-метилпентаналь. Назовите его по рациональной номенклатуре. Напишите для данного соединения формулу межклассового изомера. 1. Вещество относится к классу альдегидов: а) строим углеродный скелет, который соответствует алкану главной цепи - пентану. Концевой атом углерода изображаем в виде альдегидной группы. Нумеруем главную цепь, начиная с атома углерода карбонильной группы:
б) при С-2 ставим заместители изопропил и метил, добавляем атомы водорода:
2. Называем соединение по рациональной номенклатуре: выделяем основу, характерную для альдегидов - уксусный альдегид. Перечисляем окружающие основу углеводородные заместители в порядке возрастания их старшинства: метил, пропил, изопропил.
Соединение называется: метилпропилизопропилуксусный альдегид. 3. Приводим формулу межклассового изомера. Для альдегидов межклассовыми изомерами являются кетоны.
III. Назовите соединение по рациональной и систематической номенклатуре.
1. Данное вещество относится к классу ненасыщенных кислот. Выделяем основу, характерную для карбоновых кислот - уксусная кислота.
Называем окружающие основу заместители в порядке увеличения старшинства (см. табл. 2): диметил, винил. Соединение называется: диметилвинилуксусная кислота.
2. Называем соединение по систематической номенклатуре: а) выбираем главную цепь, которая включает карбоксильную группу и двойную связь. Нумеруем цепь с атома углерода карбоксильной группы:
б) одинаковые алкильные заместители, связанные с главной цепью, перечисляем с учетом умножающей приставки ди -. Указываем номер атома углерода (С-2), при котором они находятся; в) называем углеродную цепь соответствующим алкеном, добавляя суффикс - овая кислота. Положение двойной связи обозначаем цифрой. Название соединения: 2,2-диметилбут-3-еновая кислота. Пример решения задачи 3 I. Определите тип гибридизации атомов углерода для соединения
Гибридизованными атомными орбиталями образуются s-связи. Каждая одинарная связь атома углерода - это s-связь. Каждая последующая кратная - p-связь. Поэтому тип гибридизации атомов углерода можно определить по количеству s- и p-связей, которые этот атом образует с другими атомами: sp 3 - 4 s-связи (гибридизуются одна s + три p -орбитали), sp 2 - 3 s-связи (гибридизуются одна s + две p -орбитали) и 1 p-связь, sp - 2 s-связи (гибридизуются одна s + одна p -орбиталь) и 2 p-связи. Для каждого атома углерода определяем количество s- и p-связей и, таким образом, тип гибридизации. Например, атом углерода карбоксильной группы образует 3 s-связи (две с атомами кислорода и одну с атомом углерода) и 1 p-связь (кратная связь между углеродом и кислородом). Следовательно, тип гибридизации этого атома углерода sp 2.
II. Учитывая электроотрицательность атомов, выберите наиболее полярную связь для приведенных химических связей. Обозначьте полярность символами (d+ и d–).
Полярность связи – смещение электронной плотности к более электроотрицательному атому. В периодической системе Д. И. Менделеева электроотрицательность (ЭО) атомов увеличивается в периоде слева направо, а в группе уменьшается сверху вниз. Атом, к которому сместилась электронная плотность, приобретает частичный отрицательный заряд d–, а атом, от которого сместилась электронное облако, - d+. Смещение электронной плотности показываем также изображением связи в виде стрелки, направленной в сторону более электроотрицательного атома:
Связь С-С образуют однородные атомы, поэтому электронная плотность будет расположена симметрично. Наиболее полярной будет та связь, атомы которой обладают большей разницей в электроотрицательностях: C-Cl.
Пример решения задачи 4 Определите, какие способы обобществления электронной пары реализуются при образовании следующих соединений и какие типы связей при этом возникают.
Существует два способа обобществления электронной пары при образовании ковалентной связи: коллигация и координация. Коллигация (простая ковалентная связь) - каждый из атомов, участвующий в образовании связи, предоставляет по одному неспаренному электрону. При образовании такой ковалентной связи формальные заряды атомов остаются неизменными. Если атомы, образующие простую ковалентную связь, одинаковы, то истинные заряды атомов в молекуле также одинаковы, поскольку атомы в равной степени владеют обобществленной электронной парой. Такая связь называется неполярной ковалентной. Если связь образуется между двумя атомами с различной электроотрицательностью, то она является ковалентной полярной. Координация (донорно-акцепторная) - оба электрона новой связи предоставляет один из атомов - донор. Второй из атомов, участвующий в образовании связи, называется акцептором. В образовавшейся молекуле формальный заряд донора увеличивается на единицу, а формальный заряд акцептора уменьшается на единицу.
Решение
Образуется ковалентная полярная связь С-Cl
Образуется донорно-акцепторная ковалентная связь О-Н и ионная связь между анионом хлора и катионом метилоксония.
Пример решения задачи 5 I. Классифицируйте приведенные реагенты (радикал, электрофил, нуклеофил).
Приводим классификацию реагентов согласно их определению. Молекулы или частицы, обладающие избытком электронов (анионы и молекулы, содержащие атомы с невалентными электронами), называются нуклеофилами и обозначаются (N). Молекулы или частицы с недостатком электронов (катионы и молекулы, содержащие атомы с вакантными орбиталями), называются электрофилами и обозначаются (Е). Частицы, которые имеют один неспаренный электрон, называются радикалами и обозначаются (R). Классифицируем реагенты в задаче:
II. Укажите тип разрыва для обозначенных парой электронов связей в приведенных соединениях. Напишите и назовите образующиеся частицы.
Разрыв ковалентной связи может происходить двумя способами, обратными механизмам ее образования. Разрыв связи, при котором каждый атом получает по одному электрону из общей пары, называется гомолитическим (гомолизом), или радикальным:
В результате гомолитического разрыва образуются сходные по электронному строению частицы, каждая из которых имеет неспаренный электрон. Такие частицы называются свободными радикалами. Гомолитический разрыв в большей степени характерен для неполярных и слабополярных связей и происходит при воздействии радикальных реагентов. Если при разрыве связи общая электронная пара остается у одного атома, то такой разрыв называется гетеролитическим (гетеролизом), или ионным:
В результате образуются разноименно заряженные ионы - катион и анион. Если заряд иона сосредоточен на атоме углерода, то катион называют карбокатионом, а анион - карбанионом. Гетеролитический разрыв в большей степени характерен для полярных связей и происходит при воздействии ионных реагентов (электрофилов и нуклеофилов). В уравнении 1) связь C®Br полярная, электронная плотность смещена к более электроотрицательному атому брома. Разрыв такой связи под воздействием ионного реагента OH- (N) будет гетеролитическим. В результате образуется новая частица Br- (N).
В уравнении 2) связь C-H малополярная, поэтому разрыв такой связи под воздействием радикального реагента · NO2 (R) будет гомолитическим. В результате образуется новая частица · H (R).
Пример решения задачи 6
Определите, к какому типу относятся приведенные реакции (замещения, присоединения, элиминирования). Укажите субстрат, реагент, символ реакции.
В реакции 1) субстратом является 2-бромпропан (объект превращения, в котором реакционным центром, подвергающимся атаке, является атом углерода), а реагентом - ионное неорганическое вещество - КСN (атакующее вещество). В результате реакции происходит замещение брома в субстрате на нуклеофил СN-. Следовательно, протекает реакция нуклеофильного замещения: символ SN . В реакции 2) субстрат - этилбензол, реагент - молекулярный хлор. В результате реакции происходит замещение водорода в боковой цепи арена на хлор. Реакция протекает при облучении, которое вызывает гомолитический (радикальный) разрыв связей в субстрате и реагенте. Следовательно, представлена реакция радикального замещения: символ SR. В реакции 3 происходит присоединение спирта к двойной связи альдегида. Поэтому субстрат - метаналь, реагент - метанол. Водород (протон Н+) спирта присоединяется к атому кислорода, а анион СН3О- (нуклеофил) - к атому углерода карбонильной группы альдегида (реакционный центр). Так как к реакционному центру присоединяется нуклеофил, то символ реакции AN - нуклеофильное присоединение.
Пример решения задачи 7 Напишите реакции получения триметилметана и 2,2,3,3-тетраметилбутана из соответствующего алкена, соли карбоновой кислоты и галогенопроизводного углеводорода. Способы получения алканов
1. Из непредельных алифатических углеводородов:
2. Из солей карбоновых кислот:
а) электролизом (синтез Кольбе) - для получения симметричных алканов:
б) декарбоксилированием путем сплавления с твердой щелочью - универсальный способ получения алканов:
3. Из галогенопроизводных углеводородов:
а) взаимодействием галогеналканов с металлическим натрием (синтез Вюрца) - для получения симметричных алканов:
б) восстановление галогеналканов каталитическим гидрированием или иодоводородом (для иодалканов) - универсальный способ получения алканов
Решение Триметилметан - несимметричный алкан, который можно получить: - из соответствующего алкена:
- сплавлением со щелочью соответствующей соли карбоновой кислоты:
- восстановлением соответствующего галогеналкана:
2,2,3,3-Тетраметилбутан - алкан симметричного строения, который можно получить: - электролизом соли соответствующей карбоновой кислоты:
- из соответствующего галогеналкана по реакции Вюрца:
Из непредельного углеводорода 2,2,3,3-тетраметилбутан получить невозможно, так как не существует алкенов, алкинов и диенов с соответствующим углеродным скелетом.
Пример решения задачи 8 Выполните схему превращений, назовите образующиеся на каждой стадии продукты реакций.
Пример решения задачи 9 Получите 2-метилпент-1-ен дегидрогалогенированием соответствующего галогенопроизводного углеводорода, дегидратацией соответствующего спирта и дегалогенированием соответствующего дигалогенопроизводного.
Способы получения алкенов Правило Зайцева. Отщепление галогеноводорода или воды происходит от двух соседних атомов углерода, причем водород преимущественно отщепляется от соседнего атома углерода с меньшим числом атомов водорода (наименее гидрогенизированного).
1. Дегидрогалогенирование галогенопроизводных алканов – водород отщепляется по правилу Зайцева:
2. Дегидратация спиртов – водород отщепляется по правилу Зайцева. Кроме оксида алюминия в качестве водоотнимающего средства могут использоваться серная или фосфорная кислоты при 150-200°С.
3. Дегалогенирование вицинальных дигалогеналканов:
Решение Приводим реакцию получения 2-метилпент-1-ена: - из соответствующего галогеналкана:
- из соответствующего спирта:
- из соответствующего дигалогеналкана:
Пример решения задачи 10 Выполните схему превращений, назовите образующиеся на каждой стадии продукты реакций.
Химические свойства алкенов 1. Реакции присоединения электрофилов AE: HHal (HBr, HCl, HI), Br2, Cl2, H2O, H2SO4. Присоединение несимметричных реагентов к несимметричным алкенам идет по правилу Марковникова: водород несимметричных реагентов присоединяется к более гидрогенизированному атому углерода при кратной связи субстрата. Реакция с бромной водой - Br2, H2O - является качественной на открытие алифатической кратной связи. Наблюдается обесцвечивание желтой окраски брома.
2. Реакции присоединения галогеноводородов в присутствии пероксидов AR - присоединение идет против правила Марковникова:
3. Реакции полимеризации алкенов:
4. Реакции окисления алкенов: а) мягкое окисление реактивом Вагнера - образуются вицинальные двухатомные спирты - α-гликоли. Эта реакция является качественной на обнаружение алифатической кратной связи - наблюдается изменение окраски реактива и выпадает бурый осадок MnO2:
б) жесткое окисление перманганатом или дихроматом калия в кислой среде - образуются карбоновые кислоты, если при углероде кратной связи нет углеводородного радикала, и кетоны, если есть заместитель:
в) озонолиз - образуются альдегиды и кетоны:
Решение Выполняем схему превращений:
Пример решения задачи 11 Получите 2,3-диметилгекса-2,4-диен дегидрогалогенированием соответствующего дигалогенопроизводного углеводорода и дегидратацией соответствующего двухатомного спирта (диола).
Реакции дегидрогалогенирования и дегидратации протекают в соответствии с правилом Зайцева. Так как требуется получить алкадиен, то для введения двух двойных связей в реакциях необходимо использовать дигалогеналкан и двухатомный спирт с тем же углеродным скелетом, что и 2,3-диметилгекса-2,4-диен. Галогены и гидроксильные группы следует расположить таким образом, чтобы при отщеплении галогеноводорода или воды реализовывалось правило Зайцева. Получаем 2,3-диметилгекса-2,4-диен из соответствующего дигалогеналкана:
Из соответствующего двухатомного спирта (диола):
Пример решения задачи 12 Приведите для 2,3-диметилгекса-2,4-диена реакции с реагентами Б, В и Г. Назовите продукты реакций.
В зависимости от взаимного расположения двойных связей различают три типа алкадиенов: - с сопряженными связями (двойные связи разделены одной одинарной связью):
- изолированными связями (двойные связи разделены двумя и более одинарными связями); - кумулированными связями (двойные связи находятся при одном атоме углерода):
Решение Приводим реакции 2,3-диметилгекса-2,4-диена с реагентами Б, В и Г.
Пример решения задачи 13 Получите метил втор -бутилацетилен дегидрогалогенированием соответствующего геминального или вицинального дигалогенопроизводного углеводорода. Способы получения алкинов 1. Дегидрогалогенирование геминальных дигалогенопроизводных алканов – водород отщепляется по правилу Зайцева:
2. Дегидрогалогенирование вицинальных дигалогенопроизводных алканов – водород отщепляется по правилу Зайцева:
Решение Получаем метил втор- бутилацетилен: а) из соответствующего геминального дигалогеналкана:
б) из соответствующего вицинального дигалогеналкана:
Пример решения задачи 14 Приведите для соединения метил втор -бутилацетилен реакции с реагентами: 1) H2O, HgSO4, H2SO4, 2) K2Cr2O7, H2SO4, 3) HBr (2 моль). Назовите продукты реакций.
Химические свойства алкинов
1. Реакции присоединения электрофилов (AE) идут в соответсвии с правилом Марковникова, но медленнее, чем для алкенов, так как алкины труднее отдают свои π-электроны электрофилу ввиду того, что атомы углерода в sp -гибридизации сильнее удерживают электроны π-связи, чем в sp 2-гибридизации. Это можно связать с большей электроотрицательностью атома С в sp -гибридизации, чем в sp 2-гибридизации. Присоединение галогенов и галогеноводородов:
2. Реакции присоединения нуклеофилов А N. В качестве нуклеофилов используются: вода, спирты, анионы карбоновых кислот, циановодород. Реакции присоединения нуклеофилов идут в соответствии с правилом Марковникова, но труднее, чем реакции с электрофилами, и требуют применения катализаторов: а) присоединение воды (реакция Кучерова) происходит в кислой среде в присутствии катализатора - солей двухвалентной ртути:
б) присоединение спиртов требует применения щелочного катализа:
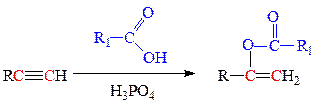
в) присоединение карбоновых кислот требует применения кислотного катализа:
г) присоединение синильной кислоты (циановодорода) в присутствии катализатора медь(I)-цианида:
3. Реакции алкинов по концевой (терминальной) тройной связи (SE). Алкины с концевой тройной связью обладают С-Н кислотностью, т. е. легко отщепляют водород, замещая его на катион одновалентных металлов: Na+, Cu+, Ag+ и др. Это качественные реакции на концевую тройную связь - наблюдается выпадение осадков ацетиленидов серебра (светло-желтый) или меди (красно-бурый). В случае взаимодействия с амидом натрия наблюдается выделение газообразного аммиака:
Ацетилениды металлов – сильные нуклеофильные реагенты. Их используют для введения тройной связи в молекулу галогеналкана, в результате углеродная цепь удлиняется:
4. Реакции окисления алкинов: а) мягкое окисление реактивом Вагнера:
б) жесткое окисление:
Решение Приводим для соединения втор- бутилацетилен реакции с реагентами:
1. Реакция с H2O, HgSO4, H2SO4 идет по правилу Марковникова:
2. Реакция жесткого окисления K2Cr2O7, H2SO4:
3. Реакция с HBr (2 моль) идет по правилу Марковникова:
Пример решения задачи 15 Выполните схему превращений, назовите образующиеся на каждой стадии продукты реакций.
Для выполнения данной схемы необходимо знать основные способы получения и химические свойства непредельных соединений. Выполнение схемы:
Пример решения задачи 17 Решение Приведите для соединения А реакцию с реагентом В, для соединения Б - с реагентом Г. Назовите образующиеся продукты реакций.
Приводим реакцию соединения А с реагентом В. Нитрильная группа СºN - это заместитель II рода, поэтому атакующая кольцо сульфо-группа вступит в мета -положение по отношению к нитрильной группе.
Приводим реакцию соединения Б с реагентом Г. Метокси-группа ОСН3 - это заместитель I рода, поэтому атакующий бензольное кольцо хлор вступит в орто - и пара- положения по отношению к метокси-группе. Одновременно образуются два изомера.
Пример решения задачи 18 Выполните схему превращений, назовите образующиеся на каждой стадии продукты реакций:
Для того чтобы решить схему превращений, необходимо знать не только химические свойства аренов, но и способы их получения.
Способы получения аренов
1. Циклотримеризация ацетилена и его гомологов:
2. Сплавление солей ароматических кислот со щелочами:
3. Реакция Вюрца-Фиттига - взаимодействие галогеналканов и арилгалогенидов с металлическим натрием
4. Алкилирование по Фриделю-Крафтсу - замещение водорода в бензольном кольце на алкильную группу. В качестве алкилирующих средств могут использоваться галогеналканы или алкены:
Решение
Пример решения задачи 19 Предложите схему следующего превращения, используя при этом необходимые реагенты. Назовите образующиеся на каждой стадии продукты реакций:
Проанализируем конечный продукт. В данном соединении присутствуют три группы: углеводородный радикал, нитро- и сульфо-группы. Следовательно, чтобы получить из бензола требуемое соединение, необходимо провести три реакции, последовательность которых зависит от ориентирующего влияния вводимых групп. Так как два заместителя в бензольном кольце находятся в пара -положении относительно друг друга, то первым должен быть введен заместитель I рода (орто-пара- ориентант) - углеводородный радикал СН3:
Далее необходимо вначале просульфировать метилбензол и только потом ввести нитрогруппу в боковую цепь. Если вначале пронитровать боковую цепь, то ориентирующее влияние группировки СН2NO2, содержащей электроноакцепторную группу NO2, будет неоднозначным и при последующем сульфировании увеличится выход мета -изомера:
Нитрогруппу в боковую цепь вводим по реакции Коновалова:
Пример решения задачи 20 Приведите для соединения 2-иод-2-фенилбутан реакции с реагентами NaOH, Н2О,NH3(изб),CH3COO
Решение Приводим для соединения 2-иод-2-фенилбутан реакции с реагентами NaOH, Н2О;NH3(изб);CH3COO
Пример решения задачи 21 Выполните схему превращений и назовите образующиеся на каждой стадии продукты реакций:
Выполнение схемы
Пример решения задачи 22 I. Дайте определение понятиям «кислотность» и «основность» органического соединения. Расположите предложенные вещества в порядке возрастания их кислотных свойств. Дайте необходимые пояснения.
II. Приведите уравнения реакций, которые иллюстрируют кислотные свойства данных веществ. Для наиболее сильного основанияприведите уравнение реакции образования оксониевой соли с H2SO4.
Спиртов и фенолов Спирты являются более слабыми кислотами, чем вода, и обнаружить их кислотность в водных растворах невозможно, рН водного раствора спиртов равно 7. Подтвердить кислотность спиртов можно только в реакциях с активными металлами или очень сильными основаниями в отсутствие воды:
Реакции с активными металлами и их амидами являются качественными на ОН-группу, так как сопровождаются бурным выделением газов. У многоатомных спиртов кислотность по сравнению с одноатомными возрастает, особенно в случае вицинальных диолов и полиолов. В отличие от одноатомных спиртов, они могут проявлять кислотные свойства не только в реакциях с активными металлами и сильными основаниями, но и в реакциях с гидроксидами тяжелых металлов. В частности, с медь(II)-гидроксидом в щелочной среде вицинальные многоатомные спирты образуют растворимую в воде комплексную соль, окрашенную в темно-синий цвет. Это качественная реакция на вицинальную диольную группу:
Фенолы. Благодаря наличию в молекулах фенолов + М -эффекта, электронная плотность на атоме кислорода понижается, полярность связи О-Н увеличивается и снижается энергия ее диссоциации. Поэтому фенолы, в отличие от спиртов, являются достаточно сильными кислотами и способны образовывать соли даже с водными растворами щелочей: | ||||||||||||||||||||||||||
|
| Поделиться: |






























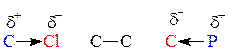









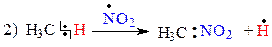










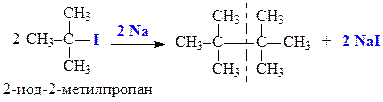







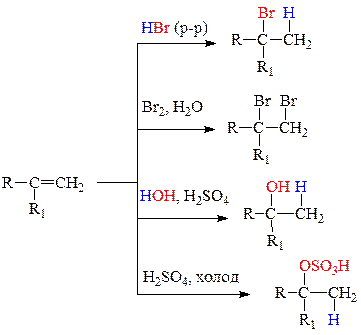














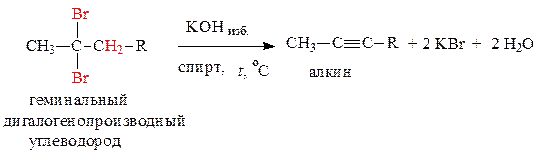
















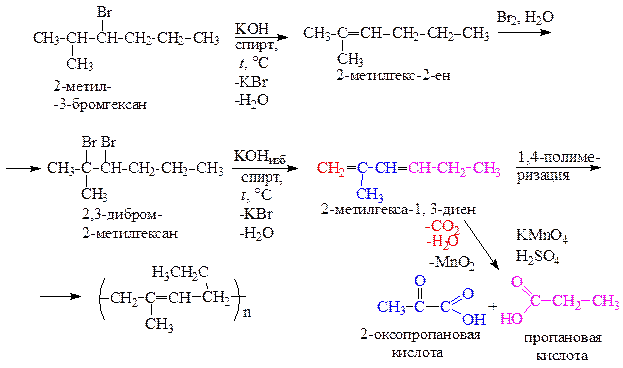
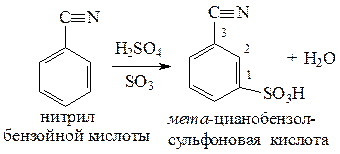





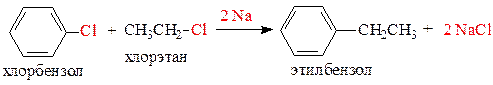



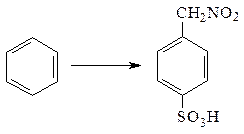



 Na
Na  .Назовите образующиеся продукты реакций.
.Назовите образующиеся продукты реакций.







