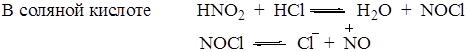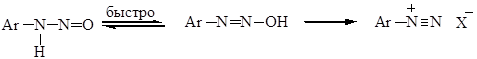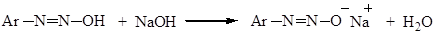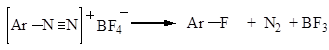Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Важнейшие представители ароматических аминовСодержание книги
Поиск на нашем сайте
Анилин впервые был получен в результате перегонки индиго с известью (1826 г.). В 1842 г.его получил Зинин восстановлением нитробензола. В незначительных количествах содержится в каменноугольной смоле. В промышленности получают из нитробензола каталитическим гидрированием с медным катализатором в газовой фазе. Анилин в больших количествах идет на получение красителей, циклогексиламина, капролактама, пестицидов и др. п-Толуидин широко применяется в производстве красителей, особенно фуксина. N,N-диметиланилин применяется в производстве красителей и взрывчатых веществ. Лекция 28. ДИАЗОСОЕДИНЕНИЯ. АЗОСОЕДИНЕНИЯ Реакция диазотирования, условия проведения, механизм. Влияние заместителей в бензольном кольце на скорость реакции. Строение диазосоеиинений в зависимости от рН, таутомерные превращения. Химические свойства. Реакции, протекающие с выделением азота: нуклеофильное замещение диазониевой группы на гидроксил, алкоксигруппу, галогены. Механизм реакции. Реакции, протекающие без выделения азота. Условия реакции азосочетания с аминами и фенолами. Влияние заместителей на реакционную способность диазосоединения. Понятие об азокрасителях. Реакция первичных ароматических аминов с азотистой кислотой приводит к образованию солей диазония (II. Гриси, 1858 г.). Эти соли имеют общую формулу [Аг-N≡N]+X- (где Х Cl, Br, NO2, HSO4, и т.д.):
Названия солей диазония образуются добавлением окончания -диазоний к названию радикала исходного ароматического соединения с указанием названия аниона, например фенилдиазоний хлорид или хлористый фенилдиазоний. Получение солей диазония Наиболее часто для получения солей диазония используют реакцию диазотирования – взаимодействие первичных ароматических аминов с азотистой кислотой или нитритом натрия в присутствии минеральной кислоты: Ar-NH2 + NaNO2 + 2 HX → ArN2+X- + NaX + H2O Диазотирование проводят действием на водный раствор соли амина азотистой кислоты, при этом используют более двух молей минеральной кислоты на один моль амина. Избыток кислоты служит для стабилизации соли диазония. Так как соли диазония разлагаются при нагревании, а диазотирование является экзотермической реакцией, процесс проводят при охлаждении, поддерживая температуру не выше 5°С.
В реакцию диазотирования вступает амин, находящийся в виде основания, поэтому на скорость реакции оказывает влияние как концентрация протонов в растворе, так и основность используемого амина. Электронодонорные заместители стабилизируют катион анилиния, т.e. способствуют делокализации положительного заряда и увеличивают основность амина. Электроноакцепторные уменьшают электронную плотность бензольного кольца, усиливая положительный заряд иона анилиния, что приводит к дестабилизации по сравнению с амином и уменьшению основности. Таким образом, заместители, увеличивающие основность, активируют ароматический амин по отношению к реакции диазотирования. Азотистая кислота, образующаяся при взаимодействии нитрита натрия с минеральной кислотой, в кислой среде может образовывать несколько диазотирующих частиц. На природу диазотирующей частицы влияет среда:
Все диазотирующие агенты могут быть представлены как производные азотистой кислоты NO-X. Механизм реакции диазотирования может быть представлен как процесс, в котором амин выступает в качестве нуклеофила, передавая свою неподеленную пару электронов электрофильной частице:
Образующийся нитрозамин в кислой среде превращается в соль диазония:
При взаимодействии со щелочью соли диазония переходят в диазогидраты:
Диазогидраты в водных растворах устойчивы и образуют диазотаты:
Таким образом, диазогидраты в зависимости от кислотности среды могут образовывать соли диазония или диазотаты, т.е. проявляют амфотерные свойства.
Б.А. Порай-Кошиц установил, что это равновесие можно смещать изменением рН среды. Химические свойства Многочисленные реакции, в которые вступают соли диазония, можно разделить на два класса: реакции с выделением азота (реакции замещения) и реакции азосочетания и восстановления (без выделения азота). Реакции замещения азота диазогруппы представляют собой наилучший путь введения в ароматическое кольцо таких заместителей, как галогены, ОН, OR, CN, H, F. Замена на ОН, OR, I является нуклеофильной реакцией и протекает по схеме:
Реакции с выделением азота Замещение на гидроксигруппу Соли диазония медленно реагируют с водой с образованием фенолов. Реация протекает даже в ледяном растворе солей диазония, а при повышенных температурах является главной реакцией солей диазония:
Чтобы исключить реакции взаимодействия образовавшегося фенола с солью диазония (реакция азосочетания) для получения фенола соль диазония медленно добавляют к кипящему раствору разбавленной серной кислоты. Замещение на галоген Замещение диазогруппы на йод протекает легко при смешении соли диазония с раствором йодида калия:
Реакцию замещения диазогруппы на хлор и бром проводят с использованием галогенидов одновалентной меди (редокс – катализатор) – реакция Зандмейера – и свежеприготовленных солей диазония:
Реакция проходит при комнатной температуре или при нагревании. Иногда реакцию проводят, используя медный порошок и галогеноводород (реакция Гаттермана). Схема реакции предусматривает образование радикалоподобных частиц или свободных арильных радикалов:
Методом введения фтора в ароматическое кольцо является реакция Шимана – нагревание фторборатных солей диазония:
Замещение на CN Замещение диазогруппы на цианогруппу проходит при взаимодействии солей диазония с цианидом одновалентной меди:
|
||||||
|
Последнее изменение этой страницы: 2016-08-01; просмотров: 280; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.227.21.101 (0.01 с.) |